Дипломная работа: Активность плаценты при гестозах
Дипломная работа: Активность плаценты при гестозах
|
Федеральное агентство по образованию Пензенский государственный педагогический университет им. В.Г. Белинского |
|
|
Факультет Естественно-географический |
Кафедрабиохимии |
|
Дипломная работа АКТИВНОСТЬ ОСНОВНЫХ КАРБОКСИПЕПТИДАЗ ПЛАЦЕНТЫ ПРИ ГЕСТОЗАХ ЛЕГКОЙ СТЕПЕНИ ТЯЖЕСТИ |
|
|
Студент __________________________________________ Козлова Е.В. подпись |
|
|
Руководитель _____________________________________Петрушова О.П. подпись
К защите допустить. Протокол № от «____» ___________200_г. |
|
|
Зав. кафедрой _______________________________________ Генгин М.Т. подпись |
|
| Пенза, 2007 г. | |
СОДЕРЖАНИЕ
СПИСОК СОКРАЩЕНИЙ ………………………………………………………4
ВВЕДЕНИЕ ……………………………………………………………………….6
ГЛАВА 1. ОБЗОР ЛИТЕРАТУРЫ ……………………………………….…….10
1.1. Этиология, патогенез, клиника ОПГ-гестозов…….………………………10
1.2. Гормоны фетоплацентарного комплекса при физиологической и патологической беременности……………………………………….….……...12
1.3. Протеолитические ферменты плаценты при физиологической и патологической беременности ……………………………………….…….…..16
1.4. Пептидгидролазы плаценты……………………………..…………..….….20
1.4.1. Основные карбоксипептидазы …………………………..……..………..20
1.4.1.1. Карбоксипептидаза Н …………………………………………..………20
1.4.1.2 ФМСФ-ингибируемая карбоксипептидаза ….…………………….......22
1.5. Перекисное окисление липидов и антиоксидантная система в плацентарной ткани при гестозах легкой степени тяжести…………..………24
ГЛАВА 2. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ ………..…..........27
2.1. Материалы исследования ………………………………………………….28
2.1.1. Клинические группы…………………………………………………...…28
2.2. Методы исследования………………………………………….………..….28
2.2.1. Методы определения активности основных карбоксипептидаз...……..28
2.2.2. Метод определения активности каталазы……………………………….29
2.3. Метод определения активности церулоплазмина………………………...30
2.2.4. Метод определения уровня диеновых и триеновых конъюгатов…...…30
2.2.5.Метод определения уровня гидроперекисей…………………………….31
2.2.6. Статистическая обработка результатов исследования ………………...31
ГЛАВА 3. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ ………………………………..33
3.1. Активность КПН и ФМСФ-ингибируемой карбоксипептидазы плацентарной ткани в норме и при ОПГ-гестозе легкой степени тяжести…………………………………………………………………………...33
3.2. Исследование активности антиоксидантной системы и показателей перекисного окисления липидов в плацентарной ткани в норме и при ОПГ-гестозе легкой степени тяжести………………………………………….…….35
ГЛАВА 4. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ …………………………….……39
ВЫВОДЫ ………………………………………………………………………..43
ЛИТЕРАТУРА …………………………………………………………………..44
СПИСОК СОКРАЩЕНИЙ
АОА – антиоксидантная активность
АОС – антиоксидантная система
АП – аминопептидаза
АПМЯК – аминопропилмеркаптоянтарная кислота
ГПЯК – гуанидинопропилянтарная кислота
Гт-Рг – гонадотропин-релизинг гормон
ГЭМЯК – гуанидиноэтилмеркаптоянтарная кислота
КП – карбоксипептидаза
ККС – калликреин-кининовая система
Кр – кортизол
КТРФ – кортикотропин-релизинг фактор
ЛАП - лейцинаминопептидаза
ЛГ – лютеинизирующий гормон
НЭП – нейтральная эндопептидаза
ОПГ – отеки, протеинурия, гипертензия
ОФБ – острофазовые белки
Пг – прогестерон
ПЛ – плацентарный лактоген
ПН – плацентарная недостаточность
ПОЛ – перекисное окисление липидов
Прл – пролактин
ПХМБ – п-хлормеркурийбензоат
ПХМФС - п-хлормеркурийфенилсульфонат
РАС – ренин-ангиотензиновая система
СДГ – сукцинатдегидрогеназа
СЭИ – синдром эндогенной интоксикации
ТЩФ – термостабильная щелочная фосфатаза
ФМСФ – фенилметилсульфонилфторид
ФПК – фетоплацентарный комплекс
ФПН – фетоплацентарная недостаточность
ХАКТГ – хорионический адренокортикотропный гормон
ХГЧ – хорионический гонадотропин человека
ВВЕДЕНИЕ
Несмотря на многочисленные исследования, проблема ОПГ(отек, протеинурия, гипертензия)-гестозов остается актуальной. Среди причин материнской смертности 20-25% случаев приходится на долю позднего гестоза, а перинатальная смертность при этом заболевании в 3-4 раза превышает среднюю.
Высокая частота гестоза, тяжесть его клинических проявлений, большая вероятность неблагоприятного исхода беременности при этом осложнении для матери и плода обусловливают повышенный интерес к исследованию патогенетических механизмов данной патологии. Изменения, происходящие в организме женщины при гестозе, изучены намного лучше, чем их причина. Их основу составляет спазм всех кровеносных сосудов, уменьшение объема циркулирующей крови, изменение свертываемости и текучести крови, нарушение микроциркуляции. Всё это приводит к значительному снижению кровоснабжения тканей с развитием в них дистрофических изменений вплоть до гибели ткани. Органами, наиболее чувствительными к недостатку кровоснабжения, являются почки, печень и головной мозг. Плацента, большей частью, состоящая из сосудов, претерпевших характерные для гестоза изменения, не справляется со своей основной функцией обеспечения обмена кислородом и питательными веществами между матерью и плодом, что становится причиной формирования фетоплацентарной недостаточности, которая ведет к хронической внутриутробной гипоксии плода и задержки его развития [40, 45, 53].
В условиях патологии уровень пептидов фетоплацентарного комплекса (ФПК) существенно меняется, при этом они вовлекаются в патогенез ОПГ-гестоза.
Изменение уровня биологически активных пептидов в ФПК при физиологическом и патологическом течении беременности во многом определяется ферментами их обмена, к которым, в частности, относится карбоксипептидаза Н (КПН). Данный фермент участвует в процессинге, следовательно, представляет интерес изучение его активности в плаценте в норме и при ОПГ-гестозе. Недавно в лаборатории ПГПУ в головном мозге была открыта фенилметилсульфонилфторид-ингибируемая карбоксипептидаза (ФМСФ-КП), физико-химические свойства, субстратная специфичность и тканевая локализация, которой позволяют предположить ее участие в процессинге пептидов [11, 12, 13, 14].
В патогенезе ОПГ-гестозов одно из ведущих мест занимает усиление перекисного окисления липидов (ПОЛ) и белков клеточных мембран на фоне снижения антиоксидантной активности (АОА), в частности угнетением активности системы церулоплазмин-трансферрин, которые в норме обезвреживают токсичные продукты метаболизма, образующиеся при ПОЛ [].
Известно, что КПН и ФМСФ-КП представлена во всех органах и тканях как в растворимой, так и в мембраносвязанной формах [дисс-34, 131, 148, 198, 265-ж]. Вероятно, продукты перекисного окисления липидов и белков могут влиять на активность данных ферментов в плацентарной ткани.
Таким образом, исследование активности карбоксипептидазы Н, фенилметилсульфонилфторид-ингибируемой карбоксипептидазы в плацентарной ткани при физиологическом и патологическом течении беременности может способствовать уточнению биологической роли этих ферментов в фетоплацентарном комплексе, а также выяснению механизмов функционирования пептидэргических систем в норме и при осложнениях гестационного процесса. Результаты исследований могут быть использованы при разработке методов коррекции метаболических нарушений в фетоплацентарной системе.
В литературе мало уделяется внимание исследованию патогенетических механизмов при гестозах легкой степени тяжести.
Целью настоящей работы было изучение роли основных карбоксипептидаз (карбоксипептидазы Н, фенилметилсульфонилфторид-ингибируемой карбоксипептидазы) в патогенезе ОПГ-гестозов легкой степени тяжести, а также оценить взаимосвязи активности ферментов с антиоксидантным статусом и показателями перекисного окисления липидов в плаценте при данной патологии.
При выполнении работы были поставлены следующие задачи:
1. Изучить активность основных карбоксипептидаз (карбоксипептидазы Н, фенилметилсульфонилфторид-ингибируемой карбоксипептидазы) в плацентарной ткани при физиологическом течении беременности.
2. Изучить активность основных карбоксипептидаз (карбоксипептидазы Н, фенилметилсульфонилфторид-ингибируемой карбоксипептидазы) в плацентарной ткани при ОПГ-гестозах легкой степени тяжести.
3. Исследовать антиоксидантный статус – активность каталазы и церулоплазмина – в плацентарной ткани при ОПГ-гестозах легкой степени тяжести.
4. Изучить показатели перекисного окисления липидов – уровня диеновых и триеновых конъюгатов, гидроперекисей липидов в плацентарной ткани при ОПГ-гестозах легкой степени тяжести.
5. Исследовать корреляционные взаимосвязи между активностью ферментов в плацентарной ткани в норме и при патологии.
6. Исследовать корреляционные взаимосвязи активности основных карбоксипептидаз с показателями перекисного окисления липидов и антиоксидантного статуса в плацентарной ткани.
Научная новизна и практическая ценность работы. Изучена активность основных карбоксипептидаз (карбоксипептидазы Н, фенилметилсульфонилфторид-ингибируемой карбоксипептидазы) в плацентарной ткани при ОПГ-гестозах легкой степени тяжести. Установлены корреляционные взаимосвязи между активностью ферментов в норме и при патологии, а также выявлены корреляционные взаимосвязи между активностью карбоксипептидаз и показателями антиоксидантного статуса и перекисного окисления липидов плаценты.
Полученные результаты представляют интерес для понимания роли карбоксипептидаз плаценты в норме, а также при ОПГ-гестозах легкой степени тяжести и могут быть использованы для разработки эффективных методов профилактики и коррекции нарушений метаболизма в фетоплацентарной системе в условиях патологии.
Апробация работы. Материалы данной работы представлены на научно-практической конференции студентов ПГПУ.
Глава 1. ОБЗОР ЛИТЕРАТУРЫ
1.1 Этиология, патогенез и клиника ОПГ-гестоза
ОПГ-гестоз - это осложнение беременности, при котором происходит расстройство функции жизненно важных органов, особенно сосудистой системы и кровотока. Под термином гестозы беременности понимаются все патологические состояние, которые возникают только во время беременности, приводят к осложнениям беременности и со стороны матери и со стороны плода, чаще всего прекращаются после беременности (лишь иногда переходят в экстрагенитальную патологию). ОПГ-гестоз — не самостоятельное заболевание — это клиническое проявление неспособности адаптационных механизмов материнского организма адекватно обеспечивать потребности развивающегося плода. Эта неспособность в различной степени выраженности перфузионно-диффузионной недостаточности в системе мать-плацента-плод.
До настоящего времени причина гестозов достоверно не установлена. Среди причин поздних гестозов, особенно тяжелых форм, ведущее место принадлежит экстрагенитальной патологии, аутоиммунным нарушениям, эндокринным заболеваниям, психологической дезадаптации женщины и другим. Предрасполагающее значение могут иметь врожденная и приобретенная недостаточность системы нейроэндокринной регуляции приспособительных реакций (гипоксия, инфекции, интоксикации, гипотрофия в антенатальном периоде, наследственные факторы и т.д.); заболевания сердечно-сосудистой системы (гипертоническая болезнь, ревматические пороки сердца); нарушение деятельности желез внутренней секреции (диабет, гипертиреоз); почек (нефрит, пиелонефрит); патология гепатобилиарной системы (гепатит, холецистит); нарушение обмена веществ (ожирение); выраженные стрессовые ситуации; интоксикации (курение и др.); аллергические и иммунологические реакции.
Существует несколько теорий возникновения гестозов: иммуногенетическая, гормональная, почечная интоксикации и повреждения эндотелия, гемодинамическая, плацентарная (морфологические изменения в плаценте и нарушение продукции гормонов), психогенная, неврологическая, наследственная и другие. Большинство исследователей склоняются к мнению о полиэтиологичности возникновения ОПГ-гестозов.
Поздний гестоз классифицируют по клиническим признакам на 4 формы: водянку, нефропатию (легкая, среднетяжелая, тяжелая), преэклампсию и эклампсию [22, 30, 31, 40, 41, 44, 50]. Различные формы гестоза рассматривают как этапы единого патологического процесса. Кроме того, выделяют чистые и сочетанные (на фоне экстрагенитальных заболеваний) формы данной патологии, а также моносимптомные (отеки, гипертония беременных) и полисимптомные (нефропатия беременных, преэклампсия, эклампсия) [30, 31, 40, 41, 44, 50].
В зарубежной классификации различают гипертензию беременных, преэклампсию и эклампсию беременных [41,46]. Поздний гестоз проявляется триадой основных симптомов: отеки, протеинурия, гипертензия.
Патологический процесс при гестозе начинается с вазоспазма, который ведет к нарушению микроциркуляции и гипоперфузии с развитием дистрофических изменений в жизненно важных органах. В организме беременной женщины происходят генерализованный спазм сосудов, нарушение проницаемости капилляров, выход жидкости и белков в ткани, снижение онкотического давления и объема циркулирующей плазмы, что приводит к развитию отеков, протеинурии и гипертензии [30, 31, 40, 41, 44, 49, 50].
Нарушение микроциркуляции в сосудах маточно-плацентарного кровотока ведет к избыточному отложению фибриноида, которое приводит к формированию хронической фетоплацентарной недостаточности. При этом отмечается нарушение всех функций плаценты, приводящее к гипоксии, внутриутробной задержке развития плода, патологии околоплодных вод, снижению продукции плацентарного лактогена, эстриола, хорионического гонадотропина и других гормонов.
Таким образом, при позднем гестозе происходят выраженные изменения в плаценте, что способствует нарушению различных функций плаценты, в том числе гормональной и ферментативной.
1.2. Гормоны фетоплацентарного комплекса при физиологической и патологической беременности
Во взаимоотношениях между организмами матери и плода плацента выполняет роль железы внутренней секреции. В ней происходят процессы синтеза, секреции и превращения ряда гормонов белковой и стероидной структуры. Местом продукции плацентарных гормонов являются синцитио - и цитотрофобласт, а также децидуальная ткань.
Из числа гормонов белковой природы в плаценте обнаружены тиреотропин, адренокортикотропный гормон (АКТГ), меланостимулирующий гормон, релаксин, лютеинизирующий рилизинг-гормон, соматостатин. Плацента синтезирует хорионический гонадотропин, плацентарный лактоген и пролактин, а также иммунореактивный β-эндорфин, α-меланоцитстимулирующий гормон и пропиомелакортин. Из гормонов стероидной природы синтезируются гестагены и эстрогены.
Физиологическая роль ряда гормонов плаценты еще не изучена полностью, однако уровень их значительно выше в тканях трофобласта, чем в децидуальной ткани. Относительно соматостатина плаценты известно, что он идентичен таковым других тканей и сходен с ним по структуре. Оказывая локальное воздействие на трофобласт, регулирует секрецию плацентарного лактогена.
Большое значение в развитии беременности и нормальных взаимоотношений в системе мать – плод имеет плацентарный лактоген (ПЛ), синтезирующийся в клетках трофобласта. Он обладает активностью пролактина и иммунологическими свойствами гормона роста, оказывает лактогенный и лютеотропный эффект, поддерживая стероидогенез в желтом теле яичника в І триместре беременности, регулирует углеводный и липидный обмены, усиливает синтеза белка в организме плода, от чего в определенной мере зависит масса плода. Влияние на процессы метаболизма плода и организма матери связано также с усилением задержки азота, возрастанием содержания жирных кислот, увеличением толерантности к гипогликемическому действию инсулина.
Концентрация ПЛ прогрессивно возрастает по мере развития беременности, достигая максимума в 35–36 нед. К моменту родов наступает умеренное снижение уровня ПЛ, отражающее начало регрессивных изменений в плаценте. В околоплодных водах уровень ПЛ в 8 – 10 раз ниже, чем в крови матери. Отмечена прямая зависимость между уровнем ПЛ в крови матери и амниотической жидкости, между содержанием гормона в крови и массой плода и плаценты. Это послужило основанием для оценки состояния плаценты и плода по уровню ПЛ в крови и в околоплодных водах (ПЛкр/ПЛв). [56]
Отношение ПЛ в крови к ПЛ в водах от 9:1 до 14:1 отмечается при умеренной перфузии плаценты. Значение его ниже 9:1 указывает на изменения функции плаценты. Об умеренной фетоплацентарной недостаточности свидетельствует уменьшение соотношения ПЛкр/ПЛв до 6:1, о тяжелой – ниже 6:1.
Для развития беременности важен хорионический гонадотропин (ХГ), являющийся продуктом синцитиотрофобласта. В ранние сроки беременности ХГ стимулирует стероидогенез в желтом теле яичника, во второй половине – синтез эстрогенов в плаценте, участвуя в ароматизации андрогенов, усиливает стероидогенез в коре надпочечников плода, а также тормозит сократительную активность миометрия, участвует в механизмах дифференцировки пола плода.
В конце беременности и при некоторых ее осложнениях в крови обнаруживаются особые формы субъединиц ХГ – так называемые свободные субъединицы α-ХГ и β-ХГ. Они являются предшественниками зрелых форм молекулы ХГ, и их появление связывают со старением плаценты, эндокринопатиями и трофобластическими опухолями. ХГ, как и ПЛ, транспортируется преимущественно в кровь матери. В крови плода его уровень в 10 – 20 раз ниже, чем в крови беременной.
В крови беременных женщин ХГ находят сразу после имплантации плодного яйца. С прогрессированием беременности уровень его в крови повышается, удваиваясь в каждые 1,7 – 2,2 дня в течение 30 дней. К 8 – 10-й неделе отмечается максимальная концентрация его в крови, которая варьирует в пределах 60 - 100 МЕ/мл. Во ІІ триместре содержание ХГ в крови постоянно на невысоком уровне (10 МЕ/мл), в ІІІ триместре несколько возрастает. Выделение ХГ с мочой начинается со 2-й недели беременности и достигает наивысшего уровня в 10–12 нед. Далее происходит постепенное снижение количества ХГ в моче.
Снижение выработки ХГЧ в плаценте наблюдается при длительном течении позднего гестоза, истинном перенашивании беременности,
Возрастание содержания в материнской сыворотке ХГЧ отмечено при недлительном позднем гестозе, изосерологическом конфликте, сахарном диабете, острой плацентарной недостаточности, хромосомной патологии плода.
В последние годы установлено, что ткань хориона и децидуальная оболочка продуцируют пролактин. Об этом свидетельствует высокое (в 10 – 100 раз большое, чем в крови) содержание этого гормона в околоплодных водах. Во время беременности, помимо плаценты, пролактин синтезируется гипофизом матери и плода, поэтому в крови матери циркулирует одновременно пролактин и плацентарного, и гипофизарного происхождения.
Физиологическая роль пролактина определяется его структурным сходством с ПЛ. Он играет определенную роль в продукции легочного сурфактанта и фетоплацентарной осморегуляции. Содержание пролактина в сыворотке крови матери прогрессивно возрастает в процессе беременности, особенно в 18 – 20 нед и перед родами.
Из стероидных гормонов плацентарное происхождение имеет прогестерон (Пг). Он участвует в имплантации плодного яйца, подавляет сократительную деятельность миометрия и поддерживает тонус истмико-цервикального отдела, стимулирует рост матки при беременности и участвует в стероидогенезе, оказывает иммунодепрессивное действие.
Прогестерон синтезируется в синцитиотрофобласте уже в ранние сроки беременности. Концентрация гормона прогрессивно растет по мере развития беременности.
Снижение уровня Пг указывает на наличие плацентарной недостаточности, внутриутробной задержки развития плода, хронической внутриутробной гипоксии плода, при перенашивании беременности, анемии [2,3]. Увеличение уровня гормона наблюдается при почечной недостаточности (нарушение его выведения).
К стероидным гормонам плаценты относятся эстрогены (эстрадиол, эстрон и эстриол). Они воздействуют на обменные процессы и рост матки, вызывая гиперплазию и гипертрофию эндометрия и миометрия, принимают активное участие в развитии родового акта. Местом выработки эстрогенов является синциотрофобласт. Продукция их находится в прямой зависимости от состояния маточно-плацентарного кровообращения и наличия предшественников, вырабатываемых в организме матери и плода. Эстрогены по праву относятся к гормонам фетоплацентарного комплекса. В начале беременности, когда масса трофобласта невелика, продукция стероидов в нем недостаточна, основное количество эстрогенов вырабатывается в надпочечниках матери и желтом теле яичника. В 12–15 нед продукция эстрогенов резко возрастает, а среди фракций начинает превалировать эстриол. Позже 20 нед беременности образование эстрогенов осуществляется преимущественно в плаценте при активном участии плода.
Снижение содержания эстрогенов в крови беременной может наблюдаться при анемии, хронической внутриутробной гипоксии плода, внутриутробной задержке развития плода, перенашивании беременности, что объясняется недостаточной секрецией их предшественников в надпочечниках плода, а также нарушением процессов синтеза Е3 в ткани плаценты; при первичном поражении плацентарной ткани вследствие инфарктов и иных сосудистых нарушений; при нарушении элиминирующей функции печени и почек беременной [2,3,4,28].
Таким образом, гормонопродуцирующая функция плаценты определяет физиологические процессы в системе мать-плацента-плод. Однако кроме участия в развитии и поддержании беременности плацентарные гормоны могут быть вовлечены в патогенез нарушений состояния фетоплацентарного комплекса при гестационных осложнения, в том числе при гестозах.
1.3. Протеолитические ферменты фетоплацентарного комплекса при физиологической и осложненной беременности
Многообразные функции в плацентарной ткани выполняют пептидгидролазы. Определенную роль в развитии беременности, особенно в ранние сроки, в период имплантации плодного яйца, играют катепсины, активность которых прогрессивно снижается в процессе развития беременности, особенно при перенашивании. Так, обнаружено, что активность катепсина L в плаценте I триместра беременности выше, чем в плаценте, полученной после срочных родов. Вероятно, эта протеаза участвует в процессах инвазии трофобласта.
В поддержание гомеостаза во время беременности вовлечены различные аминопептидазы. В плацентарном цито- и синцитиотрофобласте обнаружена аминопептидаза А (АП А, ангиотензиназа). Фермент осуществляет превращение ангиотензина II в ангиотензин III [11,16]. По мере развития беременности в сыворотке крови матери наблюдается повышение активности АП А [11,16]. Предполагается участие ангиотензиназы в снижении прессорного ответа сосудов на ангиотензин II при гестационном процессе [11,16]. При преэклампсии обнаружено снижение активности АП А в сыворотке крови беременной. При моделировании гипертонии у крыс выявлено повышение активности ангиотензиназы в плаценте, что, вероятно, связано с вовлечением фермента в ответ на дистресс плода при гипертензионном синдроме.
При позднем гестозе наблюдается увеличение систоло-диастолического отношения (S/D) в маточных артериях и артериях пуповины. При этом отмечена отрицательная корреляция между S/D и активностью ЛАП и АП А.
Важную роль в поддержании и развитии беременности играет цистинаминопептидаза (ЦАП), наибольшая активность которой обнаружена в лизосомальной фракции плацентарной ткани []. Предполагается ее участие в деградации ангиотензина II, благодаря чему ЦАП может вовлекаться в поддержание кровяного давления у матери на нормальном уровне в течение беременности. Снижение активности ЦАП в плазме крови у матери отмечено при преэклампсии; повышение – при многоплодии.
Кроме вышеуказанных ферментов в плаценте обнаружена аминопептидаза М (АП М), которая гидролизует ангиотензин II, окситоцин, энкефалины, β-эндорфин, короткие энкефалинсодержащие пептиды [из реф50]. Предполагается участие АП М в эмбриональном росте.
В регуляцию иммунных процессов во время беременности вовлечена плацентарная аминопептидаза N (АП N). Она участвует в деградации иммуномодулирующих пептидов. Кроме того, АП N гидролизует энкефалины, соматостатин, нейрокинин А, а также лиз-брадикинин, ангиотензин III.
Таким образом, большинство аминопептидаз участвует в обмене вазоактивных пептидов. Вероятно, эти ферменты препятствуют сужению плацентарных сосудов и вовлекаются в перераспределение фето-плацентарного кровотока при гестационных осложнениях.
В микроворсинках плацентарного синцитиотрофобласта в большом количестве содержится ангиотензинпревращающий фермент – компонент ренин-ангиотензиновой системы (РАС) [11,12,13]. Фермент катализирует превращение ангиотензина I в ангиотензин II, участвует в деградации брадикинина, вещества Р []. Активность АПФ в сыворотке крови матери ниже, чем в плазме крови вены пуповины, но выше, чем в плазме крови артерии пуповины []. Показано, что в норме содержание фермента в плазме крови беременных постоянно нарастает к III триместру []. У беременных, с развившейся впоследствии преэклампсией, содержание АПФ в плазме крови во II триместре оказалось значительно ниже нормы. В то же время у беременных с хронической артериальной гипертензией содержание АПФ было значительно выше нормы во все сроки беременности []. При преэклампсии в плаценте обнаружено увеличение активности АПФ [].
Недавно в микроворсинках плаценты человека обнаружена карбоксипептидаза N (кининаза I, КПN) [РЕФ26,40]. Фермент, являясь компонентом калликреин-кининовой системы (ККС), главным образом вовлечен в физиологический контроль за фетоплацентарной циркуляцией []. Участвует в деградации брадикинина в плаценте и сыворотке крови, в связи с этим КПN, вероятно, вносит вклад в градиент брадикинина между беременной и плодом []. Обнаружено, что уровни брадикинина в артериальной и венозной крови сосудов пуповины ниже, чем в крови матери [].
При легких формах поздних гестозов отмечена активация ККС, однако, при прогрессировании данной патологии наступает истощение регулирующих систем [19]. Выявлена положительная корреляция между S/D соотношением и активностью КПN [19].
В плацентарном трофобласте обнаружена также нейтральная эндопептидаза 24.11 (НЭП). Экспрессируется цитотрофобластом, синцитиотрофобластом и клетками стромы хориона. Предполагается, что НЭП 24.11 имеет отношение к обмену веществ между матерью и плодом. Фермент участвует в деградации брадикинина, окситоцина, вещества Р, нейротензина. Указывается также на возможное вовлечение нейтральной эндопептидазы в деградацию ХГЧ. При иммуногистохимических методах исследования было показано увеличение выражения плацентарной НЭП 24.11 при преэклампсии, что позволяет предположить вовлечение фермента в патофизиологические изменения при данном гестационном осложнении. Вероятно, это связано с участием фермента в регуляции местных концентраций биологически активных пептидов в фетоплацентарном комплексе [9].
Таким образом, при гестационных осложнениях отмечаются изменения в функционировании ферментных систем плаценты, в том числе тех, которые участвуют в образовании и инактивации регуляторных пептидов [11, 12, 13,16]. Последние, в свою очередь, могут быть вовлечены в нарушение многочисленных адаптационных реакций. Поэтому очень важным представляется исследование активности ферментов обмена нейропептидов при патологиях беременности.
1.4. Пептидгидролазы плаценты
1.4.1 Основные карбоксипептидазы
Основные карбоксипептидазы - пептидгидролазы, отщепляющие остатки основных аминокислот (аргинина и лизина) с С-конца пептидов. Им принадлежит важная роль в регуляции уровня биологически активных пептидов в организме [11,12] при различных физиологических и патологических процессах [11,12].
1.4.1.1. Карбоксипептидаза H
Карбоксипептидаза Н (карбоксипептидаза Е, энкефалинконвертаза, КФ 3.4.17.10) – впервые выделена и очищена в 1982 году Фрикером и Снайдером из хромаффинных гранул надпочечников быка, как фермент, образующий энкефалины из их предшественников [63]. КПH – одноцепочечный гликопротеин, экзопептидаза секреторных везикул. Фермент представлен во всех органах и тканях как в растворимой, так и в мембраносвязанной формах. Синтезируется в виде неактивного зимогена с Mr 75000, который превращается в активную форму под действием трипсиноподобных ферментов в ходе созревания секреторных везикул.
КПН – тиол-зависимый цинк-металлофермент. pH оптимум соответствует pH внутри секреторных гранул – 5,5–6,0. Активаторами фермента являются ионы Со2+, Ni2+, ингибиторами – Сd2+ , Cu2+, хелатирующие агенты: ЭДТА, о-фенантролин; реагенты на сульфгидрильные группы: ПХМФС, ПХМБ, N-этилмалеимид; органические кислоты, содержащие амино- или гуанидиновую группу: ГЭМЯК, ГПЯК, АПМЯК, АПЯГ, МГТК. Наиболее эффективными ингибиторами являются ГЭМЯК и ГПЯК с Кi 8,8 и 7,5 нМ соответственно.
Высокая активность фермента выявлены в мозге, гипофизе, хромафинных гранулах надпочечников, эндокринных клетках поджелудочной железы, плаценте [20]. Плацентарная КПН локализована в наружных ворсинках трофобласта, утероплацентарных васкулярных эндотелиальных клетках, ворсинках хориона, амниотических эндотелиальных клетках, гладких мышечных клетках пупочных сосудов (вены и артерий) [20]. Ассоциирована со структурными элементами ЭПР (в гладких мышечных клетках сосудов пуповины), комплекса Гольджи и секреторными везикулами, где протекает процессинг предшественников различных биологически активных пептидов. Фермент обнаружен в секреторных везикулах, содержащих энкефалины, атриальный натрийуретический фактор [78,80], глюкагон [77, 81], инсулин, АКТГ, пролактин [65], вещество P, вазопрессин и окситоцин и другие регуляторные пептиды.
Плацента, являясь эндокринным органом, продуцирует белковые гормоны, которые, участвуют в формировании и поддержании гомеостаза матери и плода. Кроме того, пептиды вовлекаются в патогенез гестационных осложнений. Поэтому изучение активности карбоксипептидазы Н в плацентарной ткани ОПГ-гестозах представляет актуальность.
1.4.1.2. ФМФС-ингибируемая карбоксипептидаза
В 1995 г. Генгин, Вернигора и соавт. обнаружили в растворимой фракции серого вещества головного мозга котов основную КП [], активность которой полностью подавляется ФМСФ [42]. Позднее фермент был обнаружен во всех отделах мозга и практически во всех тканях и органах крыс.
По результатам гель-фильтрации, данный фермент имеет Мr 100000 – 110000. pH оптимум – 6,0–6,5. Активность ФМСФ-ингибируемой карбоксипептидазы полностью подавляется ингибитором сериновых протеиназ – ФМСФ и реагентом на сульфгидрильные группы – ПХМБ, примерно на 40% фермент ингибировался иодацетамидом. Фермент почти в 2 раза активировался 50 мМ NaCl, несколько слабее – NaBr, KCl и KJ.
По данным тонкослойной хроматографии было обнаружено, что частично очищенный фермент отщеплял аргинин от лей5-энкефалин-арг6 и дансил-фен-лей-арг с образованием лей5-энкефалин и дансил-фен-лей соответственно. Более глубокого гидролиза субстратов не наблюдалось. Фермент также не расщеплял субстрат КПA – карбобензокси-гли-лей [42, 47]. Таким образом, по субстратной специфичности ФМСФ-ингибируемая карбоксипептидаза сходна с ЛКПB. Вместе с тем физико-химические свойства фермента (ингибирование ФМСФ, нечувствительность к ЭДТА, ГЭМЯК и ионам Co2+) отличают его от ЛКПB. Ингибирование фермента ФМСФ позволяет предположить, что он является сериновой карбоксипептидазой. В тканях млекопитающих обнаружены две сериновые карбоксипептидазы – ЛКПА (КФ 3.4.16.1, катепсин A, лизосомальная карбоксипептидаза L) и карбоксипептидаза C (КФ 3.4.12.4, ангиотензиназа C, пролилкарбоксипептидаза). Но ФМСФ-ингибируемая карбоксипептидаза отличатся от карбоксипептидазы C по молекулярной массе и субстратной специфичности.
В то же время, ФМСФ-ингибируемая карбоксипептидаза имеет сходные с ЛКПA молекулярную массу, оптимум pH, ингибиторный профиль, но отличается от последней по субстратной специфичности и тканевой локализации.
Обращает на себя внимание тот факт, что сродство обнаруженного фермента к дансил-фен-лей-арг (Кm гидролиза – 48 мкМ), выше, чем сродство КПН (Кm гидролиза – 96 мкМ). Это позволяет предположить, что энкефалин-лей5-арг6 может быть лучшим субстратом для ФМСФ-ингибируемой КП, чем для КПН. ФМСФ-КП проявляет существенную активность при значениях рН, соответствующих таковому внутри секреторных везикул. Таким образом, возможно, что обнаруженный фермент вовлекается в процессинг нейропептидов. В связи с этим представляет интерес изучение активности ФМСФ-ингибируемой КП в плацентарной ткани в норме и при патологии.
1.5 Перекисное окисление липидов и антиоксидантная система фетоплацентарного комплекса при физиологической беременности и ОПГ-гестозах
При физиологической беременности скорость инициированного окисления липидов повышается примерно в 3 раза, нет существенной разницы между этими показателями в сроки 3-6 и 8-12 нед беременности. Во время беременности в связи с возрастанием основного обмена и увеличением потребления кислорода в крови происходит ряд значительных биохимических изменений: повышается концентрация нейтрального жира, холестерина и липидов. Наряду с этим увеличивается активность фосфолипазы А2. В результате ее действия в крови увеличивается концентрация ненасыщенных жирных кислот, которые являются непосредственным субстратом для перекисного окисления. Концентрация гидроперекисей липидов при физиологической беременности возрастает примерно в 4,2 раза (в 3-6 нед) и в 4,5 раза (в 8-12 нед).
Нарушение микроциркуляции при ОПГ-гестозах вызывает существенные изменения метаболизма. В клетках происходит активация перекисного окисления липидов (ПОЛ) и фосфолипаз с образованием токсичных радикалов: в крови повышаются продукты пероксидации (гидроперекиси в 3-4 раза, МДА – в 1,5-2 раза соответственно степени тяжести) и концентрация фосфолипазы А2 в 1,2-1,5 раза. Образование токсичных радикалов, а также дефицит ПНЖК нарушают барьерную и матричную функции клеточных мембран. Об этом свидетельствует повышение параметра упорядоченности липидного бислоя мембраны (микровязкости мембран) с 0,685+0,011 отн. ед. при легкой степени заболевания до 0,714+0,002 отн. ед. при эклампсии (при норме 0,673+0,001 отн. ед.). Одновременно с этим отмечено выраженное уменьшение гидрофобности мембран в 1,3-2,1 раз, соответственно тяжести заболевания, а, следовательно, увеличение гидрофилии липидного бислоя, и как следствие – его повышенную проницаемость. Нарушение барьерной функции липидного бислоя мембран сопряжено с изменением функционирования каналов для ионов, в первую очередь Са++, а также – Na+, Ka+, Mg++. Массивный вход Са++ в клетку приводит к необратимым изменениям в ней, в частности к энергетическому голоду и ее гибели, с одной стороны, а с другой – дополнительно к мышечной контрактуре и вазоспазму.
Повреждающее действие свободных радикалов и перекисных соединений на клетки органов и тканей резко ограничивается или вовсе предупреждается сложной многокомпонентной антиоксидантной системой, в которой различают ферментативные (оксидоредуктазные ферменты и антиперекисные ферменты) и неферментативные (низкомолекулярные тиолы, аскорбиновая кислота, токоферол, витамины А, К, Р, убихинон и др.) звенья. По-видимому, защита структурных биологических мембран осуществляется преимущественно липидными биоантиоксидантами. В настоящее время все большее число исследователей полагают, что гестозы возникают вследствие нарушения антиокислительного равновесия [Воскресенский О. Н. Биофизические и физико-химические исследования в витаминологии // М. 1981. 69с.; Грищенко В. И. Современные методы диагностики и лечения позднего токсикоза беременных.// М., Медицина. 1977.186с.; Грищенко В. И., Лупояд В. С., Лікування внутрішньоутробної гіпоксії плода // Клінічна фармація.— 2003.— Т.7.— № 3. С. 37–39. ], которое в норме поддерживается витамином Е (внутриклеточный и циркулирующий в крови), глутатион-пероксидазой, постоянной или индуцированной супероксиддисмутазой и каталазой, а также внутриклеточным и внеклеточным церулоплазмином.
Активность антиоксидантного фермента глутатионпероксидазы в эритроцитах существенно не изменена как при физиологической беременности, так и при риске невынашивания в обоих критических сроках. Активность глюкозо-6-фосфатдегидрогеназы в ранних сроках беременности повышается значительно. Одновременно уровень -токоферола и ретинола снижается в плазме и повышается в плацентарной ткани. Была выявлена связь между гипертензией беременных и снижением концентрации витамина Е в плазме крови [Cerelati L., Massei M. // Acta vitamin.(Milano). 1950. Vol.197.— P.202–211. ].
Важными ферментами АОС являются каталаза и церулоплазмин. Церулоплазмин — медьсодержащая оксидаза, относится к альфа-2-глобулиновой фракции плазмы крови человека. Основные из известных биологических свойств этого белка — участие в транспорте меди, реакциях острой фазы воспаления и стресса, нейроэндокринная регуляция, поддержка кроветворения. Особый интерес вызывают также антиоксидантные, иммунорегулирующие, радиопротективные свойства. Благодаря своей высокой ферроксидазной активности ЦП предотвращает неферментативные реакции, дающие начало свободным радикалам и дальнейшему развитию ПОЛ. При физиологических условиях ЦП крови ингибирует ПОЛ на 50%. Подавление ПОЛ достигается за счет перехвата и инактивации супероксидного ион-радикала О2, иными словами, он выступает как внеклеточная супероксиддисмутаза. Церулоплазмин может выступать как регулятор функции NО-синтетазы в эндотелиальных клетках сосудов, контролируя сосудистый тонус [11Bianchini A., Musci G. and Galabrese L. Inhibition of endothelial nitric-oxide synthase by ceruloplasmin. J Biol Chem 1999;274:20265—20270.].
Выявлено увеличение концентрации ЦП у беременных в сравнении с их значениями у небеременных, что является характерным для физиологически протекающего гестационного процесса [17 Бурмистров С.О., Опарина Т.И., Прокопенко В.М., Арутюнян А.В. Показатели процесса деградации белков и антиокислительной системы при нормальной беременности. Акушерство и гинекология 2001; 6: 12—16). . По-видимому, данный факт объясняется активацией системы ПОЛ при беременности, приводящей в свою очередь к активации антиоксидантной системы защиты организма. Кроме того выявлено достоверное снижение активности ЦП при гестозах и ФПН, что вероятно, может быть объяснено истощением антиоксидантной системы защиты организма в условиях ее напряженного функционирования, вызванного развитием указанных тяжелых осложнений беременности. [15,16Guhrer Orhan H., Ozgunes H., Beksac M.S. Correlation between plasma malondialdehyde and ceruloplasmin activity values in preeclamptic pregnancies. Clin Biochim 2000; 34:505—506. ; Vitoraros N., Salamalekis E., Dalamaga N., Kassanos D., Greatsas G. Defective antioxidants mechanisms via changes in serum ceruloplasmin and total iron binding capacity of serum in women with pre-eclampsia. Eur J Obstet Gynecol 1999;84:63—67.; .( Авторы: Т.А. Крайнева1, Ю.В. Морозова2, Л.М. Ефремова1, Л.А. Шерер1, Т.С. Качалина2 ИССЛЕДОВАНИЕ СПЕЦИФИЧЕСКОЙ ОКСИДАЗНОЙ АКТИВНОСТИ СЫВОРОТОЧНОГО ЦЕРУЛОПЛАЗМИНА У БЕРЕМЕННЫХ ЖЕНЩИН – Выпуск Том 51, Выпуск 6 –нижегородский медицинский журнал)]. Предполагается что при гестозах активность ЦП является отражением общего состояния антиоксидантной ситемы защиты организма, поэтому этот параметр может быть использован в качестве одного из диагностических критериев для оценки степени тяжести гестоза.
Каталаза — фермент класса оксидоредуктаз, катализирующей разложение перекиси водорода на воду и молекулярный кислород. При низкой концентрации перекиси каталаза проявляет также пероксидазную активность, окисляя низшие спирты, полифенолы. Биологическая функция каталазы и сводится к защите клеточных мембран от пероксида водорода, образующегося в больших количествах при перекисном окислении липидов (ПОЛ). В контрольной группе беременных отмечалось увеличение активности каталазы во всех трех триместрах беременности. У беременных с гестозом третьей степени по триместрам активность каталазы достоверно снижается. В 1-ом триместре беременности уровень каталазы составил 9,150,21x10-4 нмоль/минмг; во 2-ом триместре беременности 8,770,23x10-4 нмоль/минмг; в 3-ем триместре беременности 8,300,17x10-4 нмоль/минмг. При гестозе второй степени также были выявлены достоверные отличия по сравнению с контролем: 1-ый триместр беременности - 10,000,17x10-4 нмоль/минмг; 2-ой триместр беременности 9,870,13x10-4 нмоль/минмг; 3-й триместр беременности - 9,690,16x10-4 нмоль/минмг. При гестозе первой степени в 1-ом триместре активность составила 11,40,14x10-4 нмоль/минмг; во 2-ом триместре - 10,80,12x10-4 нмоль/минмг; в 3-ем триместре - 10,20,15x10-4 нмоль/минмг. При сравнении форм гестоза 3-ей степени в 3-ем триместре с осложнениями в (7,60,18x10-4 нмоль/минмг) и без осложнений (8,30,17x10-4 нмоль/минмг) нами было показано, что активность каталазы зависит не только от степени гестоза, но также от наличия или отсутствия сопутствующей патологии. Наши исследования показали, что в целом при физиологически протекающей беременности с увеличением гестационного срока от первого к третьему триместру метаболическая активность плацентарных макрофагов характеризуется: повышением NO-секреторной активности на 83,6% (p<0,001); падением активности супероксиддисмутазы и каталазы на 64,3% (p<0,001) и 49,4% (p<0,05), соответственно, и падением ферментативной генерации перекиси водорода (табл. 1).
Также, в III триместре выявлено снижение содержания ксантина, гипоксантина и мочевой кислоты на 33%, 18,2% и 28,4% (p<0,05), соответственно, достоверное снижение активности аргиназы на 26,9% (p<0,05) и содержания спермидина и агматина на 46% и 51% (p<0,05), соответственно, возрастание активности СОД в 10,5 раз (p<0,01), глутатионпероксидазы и глутатионредуктазы на 52,7% и 117,6% (p<0,01), соответственно (табл. 2, 3). (ШЕСТОПАЛОВ АЛЕКСАНДР ВЯЧЕСЛАВОВИЧ МЕТАБОЛИЧЕСКАЯ АКТИВНОСТЬ ПЛАЦЕНТАРНЫХ МАКРОФАГОВ И МОЛЕКУЛЯРНЫЕ МЕХАНИЗМЫ ФОРМИРОВАНИЯ ПЛАЦЕНТЫ ПРИ РАЗЛИЧНЫХ ВАРИАНТАХ ТЕЧЕНИЯ БЕРЕМЕННОСТИ АВТОРЕФЕРАТ диссертации на соискание ученой степени доктора медицинских наук)
1. Активность СОД в сыворотке крови во II–III триместрах неосложненной беременности выше 5,1 Ед/мл позволяет прогнозировать развитие гестоза в 68,2% случаев [Бандик В. П., Чернокульский С.Т, Яроцкий М. Е., Венцковский Б. М. Ультраструктурные особенности микрососудистого русла терминальных ворсин хориона и плацентарный барьер при поздних токсикозах беременности // ПАГ.— 1994.— № 2.— С. 60–61.].
Глава 2. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
2.1. Материалы исследования
Активность ферментов определяли в плацентарной ткани, полученной сразу после родов при соблюдении холодового режима. Ткани взвешивали, навески гомогенизировали в стеклянном гомогенизаторе с тефлоновым пестиком. Для определения активности КПН, ФМСФ-КП при гомогенизировании использовали 10 мМ натрий-ацетатный буфер (рН 5,6), содержащий 50 мМ NaCl, в соотношении 1:50 (вес:объем), каталазы - , в соотношении 1:5, церулоплазмина - , в соотношении 1:5. В работе использовали реактивы: ацетат натрия («MERCK», Германия), ФМСФ («Serva», США), ГЭМЯК (любезно предоставлена доктором О.Л. Варламовым), субстраты – дансил-фен-ала-арг, дансил-фен-лей-арг, синтезированные к.х.н. В.Н. Калихевичем. Все остальные реактивы были отечественного производства с квалификацией «ХЧ» и «ОСЧ».
2.1.1. Клинические группы
Было обследовано 19 образцов плацентарной ткани женщин в возрасте от 20 до 35 лет. Родильницы были разделены на 2 клинические группы. В І группу (контрольную) вошли женщины с физиологическим течением беременности и родов. У всех женщин беременность закончилась срочными родами (срок родов колебался от 38 до 40 недель). Околоплодные воды были светлые. Все дети родились в удовлетворительном состоянии со средней оценкой по шкале Апгар на 1-й минуте – 8,2, на 5-й минуте жизни – 8,6. При гистологическом исследовании последов отмечены умеренно-выраженные компенсаторно-приспособительные процессы.
ΙΙ группу составили пациентки с ОПГ-гестозом легкой степени тяжести. У всех женщин беременность закончилась срочными родами (срок родов колебался от 38 до 40 недель). Околоплодные воды были светлые. Средняя оценка новорожденных по шкале Апгар на 1-й минуте составила – 8,2, на 5-й минуте жизни – 8,4.
Диагноз поставлен на основании клинических проявлений, клинико-лабораторных данных; оценку степени тяжести гестоза проводили по унифицированной шкале Гоека-Савельевой. При гистологическом исследовании последов в данной группе обнаружены умеренно-выраженные компенсаторно-приспособительные процессы, в некоторых случаях отмечены очаговые нарушения микроциркуляции, инволютивно-дистрофические изменения, признаки инфекции.
2.2. Методы исследования
2.2.1. Метод определения активности основных карбоксипептидаз
Активность КПН определяли флюорометрическим методом Fricker и Snyder [153].
Для определения активности КПН 50 мкл гомогената ткани добавляли к 150 мкл (в случае опытной пробы) 50 мМ натрий-ацетатного буфера, рН 5,6, содержащего 50 мМ NaCl, или к смеси 140 мкл вышеуказанного буфера и 10 мкл 25 мкМ водного раствора ингибитора ГЭМЯК (в случае контрольной пробы). Далее пробы преинкубировали 8 минут при 37˚С. Реакцию начинали прибавлением 50 мкл предварительно нагретого до 37˚С 210 мкМ раствора дансил-фен-ала-арг, приготовленного на воде (конечная концентрация в реакционной смеси 42 мкМ). Пробы инкубировали 60 минут при 37˚С. Реакцию останавливали прибавлением 50 мкл 1М раствора HCl.
Для экстракции продукта реакции дансил-фен-ала к пробам приливали по 1,5 мл хлороформа, интенсивно встряхивали в течение 60 с. Хлороформную и водную фазы разделяли центрифугированием в течение 10 минут при 1000 об/мин.
Измерение флюоресценции хлороформной фазы проводили на флюориметре ФМЦ-2 при λex=360 нм и λem=530 нм в кювете толщиной 1 см. В качестве стандарта использовали 1 мкМ раствор дансил-фен-ала в хлороформе.
Активность фермента определяли как разность прироста флюоресценции в пробах, не содержащих и содержащих ГЭМЯК, и выражали в нмоль дансил-фен-ала, образовавшегося за 1 минуту инкубации в пересчете на 1 мг белка.
Для определения активности ФМСФ-ингибируемой КП 50 мкл гомогената ткани добавляли к 150 мкл (в случае опытной пробы) 50 мМ натрий-ацетатного буфера, рН 5,6, содержащего 50 мМ NaCl, или к смеси 140 мкл вышеуказанного буфера и 10 мкл 25 мМ ингибитора ФМСФ, приготовленного на этаноле, который добавляли после смешивания гомогената ткани с буфером (в случае контрольной пробы). Пробы преинкубировали 8 мин при 37˚С, затем вносили 50 мкл предварительно нагретого до 37˚С 210 мкМ раствора дансил-фен-лей-арг, приготовленного на воде. Далее пробы обрабатывали как описано для КПH. Активность фермента определяли как разницу в приросте флюоресценции в пробах, не содержащих и содержащих ФМСФ и выражали в нмоль дансил-фен-лей, образовавшегося за 1 мин инкубации в пересчете на 1 мг белка.
Концентрацию белка определяли методом Лоури [80].
2.2.2 Метод определения каталазы
В две колбы наливали по 7 мл дистиллированной воды и добавляли в них по 1 мл гомогената. Содержимое кипятили 2 - 3 мин. В обе вносили по 2 мл 1% H2O2 и оставляли на 30 мин при комнатной температуре. Затем приливали по 5 мл 10% H2SO4 и оттитровывали содержимое 0,05н KMnO4 до розового цвета.
Расчет: 1мл 0,05 н KMnO4 — 0,85 г H2O2. Таким образом, разницу в результатах титрования контроля и опыта умножаем на эту величину, получали количество мг перекиси.
2.2.3 Метод определения активности церулоплазмина
Активность церулоплазмина определяли модифицированным методом Ревина, который базируется на окислении p-фенилендиамина при участии этого фермента. Ферментативную реакцию останавливают добавлением фтористого натрия. По оптической плотности образующихся продуктов судят о концентрации церулоплазмина.
В обычные химические пробирки вносили по 0,1 мл гомогената. В одну из пробирок, служащую контрольной, добавляли 2 мл раствора фтористого натрия (с целью инактивации ферментативной активности церулоплазмина). Затем во все пробирки помещали по 8 мл ацетатного буфера и по 1 мл раствора p-фенилендиамина (используемого в качестве субстрата). Пробирки встряхивали и ставили на 1ч в водяную баню с температурой +37˚С. После инкубации во все пробирки, за исключением контрольной, доливали по 2 мл раствора фтористого натрия. Содержимое пробирок перемешивали и переносили в холодильник, где выдерживали в течение 30 мин при +4˚С. Пробы колориметрировали на ФЭКе с зеленым светофильтром (530нм) в кюветах с шириной слоя 10 мм. Результаты сравнивали с данными контрольной пробы (бледно-розовая окраска). Умножали значения оптической плотности на коэффициент пересчета 875, получали величину концентрации церулоплазмина в мг/л.
2.2.4. Метод определения уровня продуктов перекисного окисления липидов (диеновых и триеновых конъюгатов)
Для экстракции липидов брали 1 мл 25% гомогената плацентарной ткани, приливали 3 мл метанола, перемешивали стеклянной палочкой, встряхивали в течение 15 мин, затем центрифугировали при 3000 об/мин в течение 5 мин. Добавляли 3 мл гексана, вновь тщательно перемешивали стеклянной палочкой, встряхивали в течение 15 мин и оставляли отстаиваться на 30 мин. После разделения слоев, верхний (метанол-гексановый слой) отбирали в сухую пробирку и использовали для исследований.
Уровень диеновых конъюгатов определяли спектрофотометрически при длине волны 233 нм, кетодиенов и сопряженных триенов – при длине волны 278 нм, ненасыщенных липидов – при длине волны 220 нм. Рассчитывали содержание диеновых конъюгатов, кетодиенов и сопряженных триенов по отношению к уровню ненасыщенных липидов (E233/E220 и E278/E220).
2.2.5 Метод определения уровня гидроперекисей
Для приготовления гомогената использовали буфер 0,025 М трис HCl (pH 7,4), содержащий 0,175 М хлорида калия. Гомогенат (25%) по 2 мл помещают в центрифужные пробирки и осаждают белок добавлением 0,2 мл 50%-ного раствора ТХУ.
Образующийся осадок отделяют центрифугированием в течение 10 мин. при 4000g. 2 лм надосадочной жидкости доводят 96% этанолом до 27 мл. К равным объемам до 27 мл добавляют 0,2 мл концентрированной соляной кислоты и 0,025 мл 5%-ного раствора соли Мора в 3%-ной соляной кислоте, пробы интенсивно встряхивают. Точно через 30с приливают 1мл 20%-ного раствора роданистого калия, после чего развивается малиновая окраска. В качестве контроля используют пробы, содержащие 96%-ный этанол вместо НЖ. Изменение оптической плотности проводят в течение 10 мин. после добавления роданистого калия при 480 нм.
2.2.6 Статистическая обработка результатов исследования
Достоверность отличий между средними определяли с использованием t-критерия Стьюдента. Корреляционный анализ проводили с помощью программы Statgraphics (версия 3.0) (“STSC, Inc.” США) в режимах Simple Correlation.
Глава 3. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
3.1. Активность КПН и ФМСФ-ингибируемой карбоксипептидазы в плацентарной ткани в норме и при ОПГ-гестозе легкой степени тяжести
Результаты исследования показали достоверное снижение активности КПH и ФМСФ-КП в плацентарной ткани при ОПГ-гестозе легкой степени тяжести в 2 раза по сравнению с нормой (рисунок 1, 2).
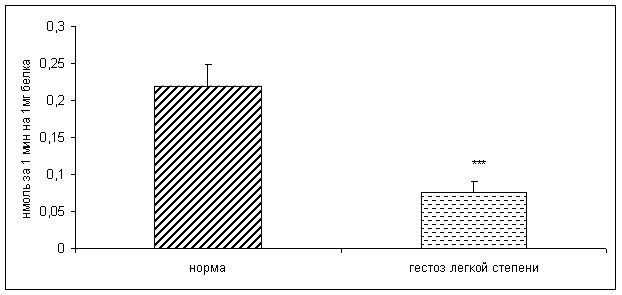
Рисунок 1. Активность карбоксипептидазы H в норме и при ОПГ-гестозе легкой степени тяжести (нмоль продукта, образовавшегося за 1мин инкубации на 1мг белка; M±m; *** - p<0,001 относительно нормы)
По данным корреляционного анализа выявлена положительная взаимосвязь между активностью КПН и ФМСФ-КП в плацентарной ткани. Уменьшение активности КПH согласуется с данными литературы о снижении концентрации белковых гормонов в фетоплацентарном комплексе (ФПК) при ОПГ-гестозах [7,8,9,11,12,13]. Наиболее важными из них являются хорионический гонадотропин, плацентарный лактоген, пролактин, инсулин, инсулиноподобные факторы роста, C – пептид и др.
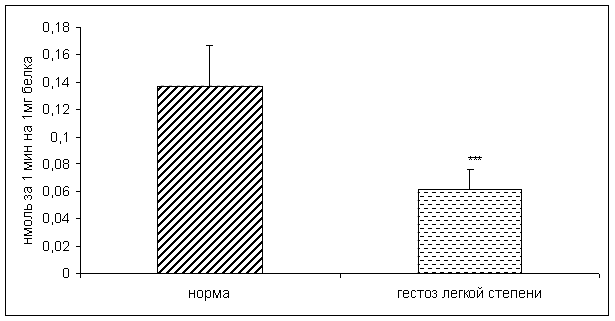
Рисунок 2. Активность ФМСФ-КП в норме и при ОПГ-гестозе легкой степени тяжести (нмоль продукта, образовавшегося за 1мин инкубации на 1мг белка; M±m; *** - p<0,001 относительно нормы)
По данным корреляционного анализа выявлена положительная взаимосвязь между активностью КПН и ФМСФ-КП в плацентарной ткани. Учитывая, что КПH ассоциирована с процессингом пептидных гормонов [5,16], можно предположить участие фермента в образовании выше указанных биологически активных веществ.
Гестоз является стрессом для ФПК. В условиях патологии отмечено повышение уровней кортикотропин-рилизинг-фактор (КТРФ) и опиоидов в плацентарной ткани [5,8,9,10]. КТРФ, в свою очередь, снижает уровень хорионического гонадотропина, что ведет к угнетению синтеза прогестерона и эстрогенов, которые обладают антиоксидантной активностью. Это усугубляет негативное действие ПО липидов и белков на клеточные мембраны, что может приводить к снижению активности КПH и ФМСФ-КП.
Обнаруженная положительная корреляция между активностью КПН и ФМСФ-КП (r (коэффициент корреляции)=0,9255***) позволяет предположить участие ФМСФ-КП в процессинге регуляторных пептидов в плацентарной ткани.
Таким образом, КПH и ФМСФ-КП плаценты играют важную роль в патогенезе ОПГ-гестоза. Возможно, полученные результаты могут быть основой для дальнейшего исследования гомеостаза ФПК и изыскания способов коррекции метаболических изменений в плаценте при патологическом течении беременности.
3.2 Исследование активности антиоксидантной системы и показателей перекисного окисления липидов в плацентарной ткани в норме и при ОПГ-гестозе легкой степени тяжести
Результаты исследования показали достоверное снижение активности каталазы и церулоплазмина в плацентарной ткани при ОПГ-гестозе легкой степени тяжести в 1,2 раза по сравнению с нормой (рисунок 3).
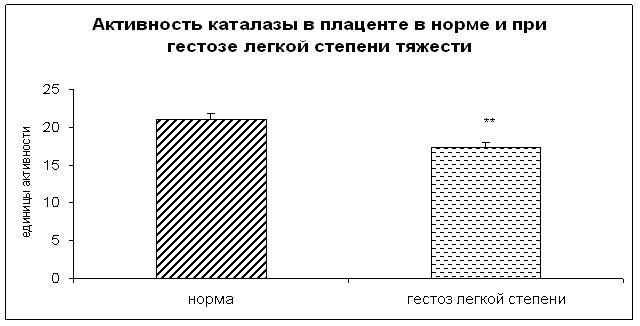
Рисунок 3. Активность каталазы в норме и при ОПГ-гестозе легкой степени тяжести в плацентарной ткани (** - p<0,01 относительно нормы).
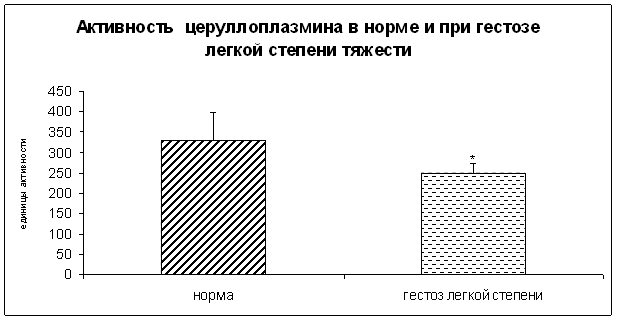
Рисунок 4. Активность церулоплазмина в норме и при ОПГ-гестозе легкой степени тяжести в плацентарной ткани (* - p<0,05 относительно нормы).
Снижение активности этих ферментов можно объяснить начавшимся угнетением антиоксидантной системы фетоплацентарного комплекса в условиях осложненной беременности.
По данным корреляционного анализа обнаружена положительная взаимосвязь активности церулоплазмина с активностью КПH в плацентарной ткани (r=0,4749*).
Результаты исследования показали достоверное повышение уровня гидроперекисей липидов, а также достоверное снижение концентрации диеновых и триеновых коньюгатов в плацентарной ткани при ОПГ-гестозе легкой степени тяжести.
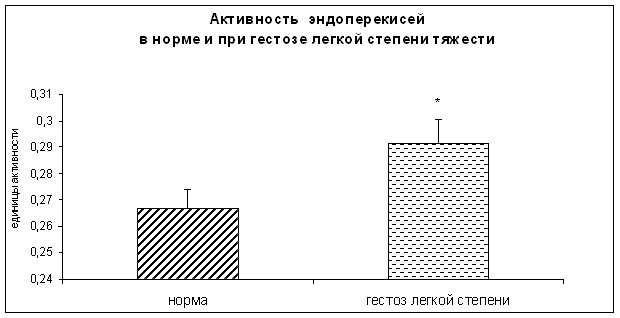
Рисунок 5. Концентрация гидроперекисей в норме и при ОПГ-гестозе легкой степени тяжести в плацентарной ткани (*-p<0,05 относительно нормы).
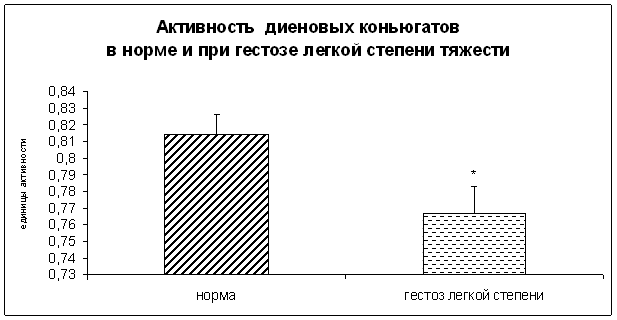
Рисунок 6. Активность диеновых коньюгатов в норме и при ОПГ-гестозе легкой степени тяжести в плацентарной ткани (*-p<0,05 относительно нормы).
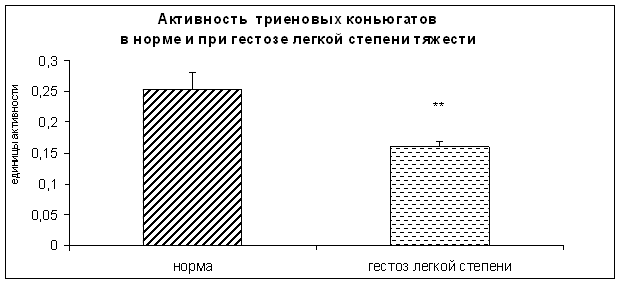
Рисунок 7. Активность триеновых коньюгатов в норме и при ОПГ-гестозе легкой степени тяжести в плацентарной ткани (*-p<0,01 относительно нормы).
По данным корреляционного анализа обнаружены взаимосвязи уровня триеновых коньюгатов с активностью КПН (r=0,6**) и ФМСФ-КП (r=0,5778 **). В патогенезе ОПГ-гестозов ведущую роль играет нарушение структурно-функциональных свойств клеточных мембран плаценты. В условиях патологии усиливается перекисное окисление липидов (ПОЛ) и белков на фоне снижения активности антиоксидантной системы, что является причиной повреждения мембран [6,7,8,9,10,11,12,13].
ГЛАВА 4. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
ОПГ – гестоз (отек, протеинурия, гипертензия) – это осложнение беременности, обусловленное несоответствием возможностей адаптивных систем организма матери и потребностей развивающегося плода.
Несмотря на многочисленные исследования, проблема гестозов (преэклампсия, гипертония, индуцированная беременностью) остается актуальной. Частота их составляет 8-16%. Они занимают 2-3 место в структуре материнской смертности, являясь одновременно основной причиной неблагоприятных перинатальных исходов. При этом материнская смертность достигает 3,5%, а перинатальная — 79% [2,6,7].
До настоящего времени причина гестозов достоверно не установлена. Среди причин поздних гестозов, особенно тяжелых форм, ведущее место принадлежит экстрагенитальной патологии, аутоиммунным нарушениям, эндокринным заболеваниям, психологической дезадаптации женщины и другим. Высокая частота гестоза, тяжесть его клинических проявлений, большая вероятность неблагоприятного исхода беременности при этом осложнении для матери и плода обусловливают повышенный интерес к исследованию патогенетических механизмов данной патологии.
ОПГ-гестозы вызывают нарушения компенсаторно-приспособительных механизмов ФПК на молекулярном, клеточном, тканевом, органном, организменном уровнях [67радз], что реализуется в компенсированной, субкомпенсированной и декомпенсированной формах плацентарной недостаточности (ПН). При этом наблюдается комплекс нарушений транспортной, трофической, эндокринной и метаболической функции плаценты, лежащих в основе патологии плода (нередким клиническим проявлением ПН является задержка внутриутробного развития плода, его гипоксия и гипотрофия) и новорожденного (нарушения мозгового кровообращения, кривошея, снижение мышечного тонуса и угнетение физиологических рефлексов).
ОПГ-гестозы оказывают влияние на синтез белковых веществ в плаценте, который обусловлен особенностями функционирования ферментных систем. Поэтому изучение активности пептидгидролаз в норме и при патологии представляет значительный интерес как для понимания биологической роли самих ферментов, так и для понимания роли регуляторных пептидов в этиологии и патогенезе осложнений беременности.
Результаты исследования показали достоверное снижение активности КПH при ОПГ-гестозе по сравнению с нормой. Уменьшение активности КПН согласуется с данными литературы о снижении концентрации белковых гормонов в фетоплацентарном комплексе []. Наиболее важными из них являются хорионический гонадотропин, плацентарный лактоген, пролактин, а также инсулин, С-пептид и др []. Учитывая, что КПН ассоциирована с процессингом пептидных гормонов [], можно предположить участие фермента в образовании выше указанных биологически активных веществ в плаценте.
Результаты исследования показали снижение активности ФМСФ-ингибируемой карбоксипептидазы в плацентарной ткани при ОПГ-гестозе легкой степени тяжести по сравнению с нормой. Положительная корреляция активности ФМСФ-КП с КПН позволяет предположить участие фермента в процессинге пептидов.
В связи с тем, что ФМСФ-КП существует в мембраносвязанной форме, снижение активности фермента можно также объяснить изменением состояния мембран под действием продуктов ПОЛ.
Как уже отмечалось ранее, при патологическом течении беременности происходит активация ПОЛ. Результаты исследования показали достоверное снижение активности диеновых и триеновых коньюгатов при ОПГ-гестозе по сравнению с нормой. А также достоверное повышение уровня гидроперекисей.
Этот факт может быть объяснен, что на фоне мы рассматриваем гестоз легкой степени тяжести, в случае которого не произошло еще повышение ПОЛ. Но, в пользу начинающегося обострения говорит повышение уровня гидроперекисей.
Токсичные продукты ПОЛ обезвреживает многокомпонентная АОС. Так как, в литературе мало уделяется внимания анализу биохимических показателей АОС при ОПГ-гестозе легкой степени тяжести, то целью нашего исследования было определить активность каталазы и церулоплазмина при данной патологии. Результаты исследования показали достоверное снижение активности каталазы и церулоплазмина при ОПГ-гестозе по сравнению с нормой.
Схема 1. Корреляционные взаимосвязи между активностями ферментов
|
|||
|
|||
![]()
![]()
![]()
![]()
|
|
||||
![]() Указания к схеме 1: –
положительная корреляция
Указания к схеме 1: –
положительная корреляция
ГЛАВА5 ВЫВОДЫ
1. Изучена активность пептид-гидролаз лизосомальной и нелизосомальной локализации в плацентарной ткани при физиологическом и патологическом течении беременности. Обнаружено, что при гестационных осложнениях наблюдаются изменения активности КПН, ФМСФ-КП, каталазы, церулоплазмина в плаценте.
2. Выявлено снижение активности КПН в плаценте при всех исследуемых патологиях.
3. Установлено снижение активности ФМСФ-КП в плаценте ОПГ-гестозе легкой степени тяжести по сравнению с нормой.
4. Обнаружено, что активность каталазы и церулоплазмина снижается в плаценте при ОПГ-гестозе легкой степени тяжести по сравнению с нормой.
5. Выявлено повышение активности гидроперекисей в плаценте при ОПГ - гестозе легкой степени тяжести по сравнению с нормой.
ЛИТЕРАТУРА
1. Айламазян Э.К. Антиоксиданты в комплексной терапии позднего токсикоза и связанной с ним хронической гипоксии плода //Акушерство и гинекология.1991,.№3,С.30–34
2. Анастасьева В.Г. Морфофункциональные нарушения фето-плацентарного комплекса при плацентарной недостаточности. – Новосибирск, 1997. – С. 107
3. Аржанова О.Н., Кошелева Н.Г., Ковалева Т.Г., Громыко Г.Л., Тышкевич О.В. Плацентарная недостаточность: диагностика и лечение // Учебное пособие. Под редакцией Э.К. Айламазяна. – СПб: ИЗДАТ НОРМЕД, 2000. – 32 с.
4. Афанасьева Н.В., Стрижаков А.Н. Исходы беременности и родов при фетоплацентарной недостаточности различной степени тяжести.// Вопросы гинекологии, акушерства и перинатологии. 2004, Т. 3, №2, С. 7–13.
5. Баркаган З.С., Момот А.П. Диагностика и контролируемая терапия нарушений гемостаза. – М.: Издательство «Ньюдиамед», 2001. – 298 с.
6. Беднарский Л.С., Чайка Н.А., Ярославский В.К., Данилова Л.А., Резников Л.Л. Применение эндоваскулярной лазерной терапии в комплексном лечении ОПГ-гестоза // Акушерство и гинекология. – 1995. – № 6. – С. 18-22.
7. Болдырев А.А., Введение в биохимию мембран. — М.:Наука,1986г.—112с 6.
8. Бурлев В. А. Свободно-радикальное окисление в системе мать—плацента—плод при акушерской патологии // Автореф. дис.... д-ра мед. наук.— М., 1992.
9. Бычков В.И., Образцова Е.Е., Шамарин С.В. Диагностика и лечение хронической фетоплацентарной недостаточности // Акушерство и гинекология. – 1999. – № 6. – С. 3-6.
10. Васильева З. В., Тягунова А. В., Дpожжева В. В., Конькова Т. А. Функция почек и показатели эндогенной интоксикации пpи гестозах // Акушерство и гинекология. – 2003. – № 1. – С. 16-20.
11. Вернигора А.Н., Генгин М.Т. Механизмы регуляции активности и биологическая роль карбоксипептидазы H – фермента процессинга нейропептидов // Биохимия. – 1995. – Т. 60, № 12. – С. 1491-1497.
12. Вернигора А.Н., Никишин Н.Н., Генгин М.Т. Частичная характеристика основной фенилметилсульфонилфторид-ингибируемой карбоксипептидазы из головного мозга кошки // Биохимия. – 1995. – Т. 60, № 11. – С. 1860-1866.
13. Вернигора А.Н., Генгин М.Т., Салдаев Д.А., Щетинина Н.В. Распределение активности фенилметилсульфонилфторид-ингибируемой карбоксипептидазы в нервной ткани котов // Нейрохимия. – 1997. – Т. 14, № 4. – С. 423 - 425.
14. Вернигора А.Н., Никишин Н.Н., Генгин М.Т. Влияние глюкортикоидов на активность растворимой и мембраносвязанной форм карбоксипептидазы Н in vivo // Укр. биохим. журн. – 1995. – Т. 67, № 6. – С. 93-98.
15. Вернигора А.Н., Щетинина Н.В., Салдаев Д.А., Генгин М.Т. Распределение активности основных карбоксипептидаз в тканях лабораторных животных разных видов // Жур. эволюц. биохим. физиол. – 2002. – Т. 38, № 1. – С. 25-27.
16. Вернигора А.Н., Генгин М.Т. 40 лет изучения ангиотензинпревращающего фермента: проблемы и достижения // Укр. биохим. журн. – 1998. – 70, № 2. – С. 3-14.
17. Ветров В. В. Гомеостаз у беременных с гестозом // Акуш. и гин.— 1998.— № 2.— С. 12–14.
18. Владимиров Ю. А., Арчаков А. И. Перикисное окисление липидов в биологических мембранах.— М., 1972.
19. Возовик А.В. Коррекция фетоплацентарной недостаточности у беременных с нетоксическим узловым зобом. //Материалы V Российского Форума «Мать и Дитя», Москва,2003, 44–45
20. Габелова К.А., Арутюнян А.В., Зубжицкая Л.Б. Фиксированные иммунные комплексы и NO-синтетазная активность плаценты при гестозе // Вестн. Росс. Ассоц. акуш.-гин. – 2000. – №1. – С. 22-24.
21. Гармашева Н.Л., Константинова Н.Н. Патофизиологические основы охраны внутриутробного развития человека. Л.,1985.,159 с.
22. Грищенко В. И., Щербина Н. А. Совершенствование диагностики и терапии перинатальной патологии // Акушерство и гинекология. 1990, № 10, С. 3–6.
23. Громыко Г.Л., Шпаков А.О. Современные представления о механизмах регуляции кровообращения в плаценте при физиологической и осложненной беременности // Вестник Российской ассоциации акушеров-гинекологов. – 1995. – № 4. – С. 35—41.
24. Губский Ю. И., Сильченко И. А., Селезнева А. И. Роль антиоксидантных витаминов в ограничении токсинов. // В кн.: Биофизические и физико-химические исследования в витаминологии.— М.: Наука, 1981.— С.104–106.
25. Гутикова Л. В. Клинико-биохимическая оценка эффективности применения липорастворимых антиоксидантов при гестозе // Акушерство и гинекология – 2005. – № 1. – С. 10-13.
26. Демидович Е.О., Игнатко И.В. Особенности плодового почечного кровотока при фетоплацентарной недостаточности. //Материалы V Российского Форума «Мать и Дитя», Москва,2003, С.56–57
27. Дмитриев Л. Ф., Давлетина Л. Н., Иванов И. И. Взаимосвязь окислительного фосфорилирования и перекисного окисления липидов // Биологические мембраны — 1985.— Т.2, № 8 — С. 795–799.
28. Лакин Г.Ф. Биометрия. – М.: Высш. шк., 1990. – 352 с.
29. Ломакин М.С., Арцимович Н.Г. Биологически активные вещества, ассоциированные с плацентой // Акушерство и гинекология. – 1991. – № 9. – С. 6-10.
30. Кошелева Н.Г., Аржанова О.Н., Громыко Г.Л. и соавт. Новые подходы к лечению угрожающих преждевременных родов //Вестник Российской ассоциации акушеров гинекологов.1996, №1, С.55–60.
31. Кошелева Н.Г., Никологорская Е.В. Профилактика гипертензивных форм гестоза с помощью магне В6 при невынашивании беременности в анамнезе // Росс. Вестн. Акушера-гинеколога. – 2005. – Т. 5, № 1. – С. 40-42.
32. Кулаков В.И., Мурашко Л.Е., Бурлев В.А. Клинико-биохимические аспекты патогенеза гестозов// Акушерство и гинекология. – 1995. – № 6. – С. 3-5.
33. Кулаков В.И., Бурлев В.А., Коноводова Е.Н., Мурашко Л.Е. и др. Клиническое значение сывороточного железа и ферритина у беременных с железодефицитной анемией и гестозом // Материалы международного симпозиума: "Актуальные вопросы профилактики и лечения гестоза". М. 1998. – С. 66-67.
34.
35. Маркелова Н.Б. Изменения клеточного иммунитета при гестозах беременных и их коррекция // Автореферат дисс. … на соискание ученой степени канд. мед. наук. – Волгоград, 2004.
36. Мерзлякова А.А., Добротина А.Ф., Егорова Н.А. Показатели аутоиммунных антител и состояние системы гемостаза у беременных с рано развившимся гестозом // Нижегородский медицинский журнал. – 2002. – № 4. – С. 16-19.
37. Орджоникидзе Н. В., Клименко П. А., Дживигелова Г. Д. и др. Новое в лечении беременных с синдромом задержки развития плода // Акушерство и гинекология. 1996, № 3, С. 32–36
38. Павлович Л.Л. Патогенетическое обоснование пpименения w-3-полиненасыщенных жиpных кислот пpи осложненном течении беpеменности // Акушерство и гинекология. – 1998. – № 1. – С. 48-52.
39. Паращук Ю. С., Грищенко О. В., Лахно И. В., Шевченко О. И. Фетоплацентарная недостаточность. Учебное пособие. Харьков: ХГМУ, 1999. 45 с.
40. Пестрикова Т. Ю., Чижова Т. В., Петричко М. И. и др. Ведение беременности и родов высокого риска. М.: Сувенир, 1994. 287 с.
41. Подтетенев А.Д., Братчикова Г.В. Тактика ведения родов при гестозе. – М.: РУДН, 2004. – 237 с.
42. Радзинский В.Е., Ордиянц И.М. Плацентарная недостаточность при гестозе // Акушерство и гинекология. – 1999. – № 1. – С.11-16.
43. Радзинский В.Е., Смалько П.Я. Биохимия плацентарной недостаточности. – М: Издательство Российского университета дружбы народов, 2001. – 276 с.
44. Савельева Г.М., Федорова М.В., Клименко П.А., Сичинава Л.Г. Плацентарная недостаточность. – М.: Медицина, 1991. – 272 с.
45. Савельева Г.М., Шалина Р.И., Дживелегова Г.Д., Кашежева А.З., Гандур Д. Принципы профилактики и лечения ОПГ-гестозов // Акушерство и гинекология. – 1992. – № 3-7. – С.14-17.
46. Савельева Г.М., Шалина Р.И. Современные проблемы этиологии, патогенеза, терапии и профилактики гестозов // Акушерство и гинекология. – 1998. – № 5. – С. 6 - 9.
47. Салов И.А., Чеснокова Н.П., Глухова Т.Н. Закономерности развития системных обменных нарушений при гестозе // Росс. Вестн. Акушера-гинеколога. – 2004. – Т. 4, № 3. – С.4-6.
48. Сидельникова В.М. Актуальные проблемы невынашивания беременности. М.,1999, 138 с
49. Трубникова Л. И., Шатохина С. Н., Кузнецова Т. В., Измайлова Ф. А., Таджиева В. Д. Структурные компоненты биологических жидкостей у беременных с гестозом // Акушерство и гинекология. – 2005. – № 2. – С. 35-39.
50. Тютюнник В. Л., Бурлев В. А., Зайдиева З. С. Морфофункциональное состояние системы мать—плацента—плод при плацентарной недостаточности и инфекции // Акушерство и гинекология. – 2003. – № 6. – С. 11-16.
51. Федорова М.В. Плацентарная недостаточность. // Акушерство и гинекология, 1997; 6: 40–3.
52. Федорова М.В., Калашникова Е.П. Плацента и ее роль при беременности. – М.: Медицина, 1986. – 256 с.
53. Хейфец С.Н., Дуда Т.Л., Курасов В.Н. Состояние калликреин-кининовой системы крови при гестозе // Акушерство и гинекология. – 1989. – № 5. – С. 31-33.
54. Шалина Р.И. Мембранные нарушения в патогенезе ОПГ-гестозов // ВРААГ. – 1997. – № 1. – С. 36-43.
55. Шаповаленко С.А. Комплексная диагностика и лечение плацентарной недостаточности у беременных на разных стадиях гестации. // Вестник Российской ассоциации акушеров–гинекологов, 2001, № 2, С.43–7
56. Шехтман М. М. Железодефицитная анемия и беременность // Гинекология. – 2000. – № 6. – С. 164-170.
57. Шмагель К. В., Чеpешнев В. А. Плацентаpный лактоген: функции, клиническое значение // Акушерство и гинекология. – 2003. – № 3. – С. 9-12.
58.
al-Hameri M., Chlabicz M., Gacko M.
Proteolytic activity of placenta with EPH-gestosis determined by casein and
azocasein // Ginekol Pol. – 2001. – Vol. 72, № 6. – P. 478-482.
59. Ahmed I., Glynn B.P., Perkins A.V., Castro M.G., Rowe J., Morrison E., Linton E.A. Processing of Procorticotropin-Releasing Hormone (Pro-CRH): Molecular Forms of CRH in Normal and Preeclamptic Pregnancy // J Clin Endocrinol Metab. – 2000. – Vol. 85, № 2. – P. 755-764.
60. Eipper B.A., Green C.B., Mains R.E. Expression of prohormone processing enzymes in neuroendocrine and non-neuroendocrine cells // Monogr. Natl. Cancer. Inst. – 1992. - № 13. – P. 163-168.
61. Emanuel R.L., Robinson B.G., Seely E.W., Graves S.W., Kohane I., Saltzman D., Barbieri R., Majzoub J.A. Corticotrophin releasing hormone levels in human plasma and amniotic fluid during gestation // Clin Endocrinol (Oxf). – 1994. – Vol. 40, № 2. – P. 257-262.
62. Erdos E.G., Skidgel R.A. The angiotensin-I-converting enzyme // Lab. Invert. – 1987. – V.56. – P.345-348.
63. Evans P., Etherington D.J. Characterisation of cathepsin B and collagenolytic cathepsin from human placenta // Eur J Biochem. – 1978. – Vol. 83, № 1. – P. 87-97.
64. Facchinetti F., Garuti G., Petraglia F., Mercantini F., Genazzani A.R. Changes in beta-endorphin in fetal membranes and placenta in normal and pathological pregnancies // Acta Obstet Gynecol Scand. – 1990. – Vol. 69, № 7-8. – P. 603-607.
65. Fadalti M., Pezzani I., Cobellis L., Springolo F., Petrovec M.M., Ambrosini G., Reis F.M., Petraglia F. Placental corticotropin-releasing factor. An update // Ann N Y Acad Sci. – 2000. – Vol. 900. – P. 89-94.
66. Florio P., Luisi S., Ciarmela P., Severi F.M., Bocchi C., Petraglia F. Inhibins and activins in pregnancy // Mol Cell Endocrinol. – 2004. – Vol. 225, № 1-2. – P. 93-100.
67. Florio P., Imperatore A., Sanseverino F., Torricelli M., Reis F.M., Lowry P.J., Petraglia F. The measurement of maternal plasma corticotropin-releasing factor (CRF) and CRF-binding protein improves the early prediction of preeclampsia // J Clin Endocrinol Metab. – 2004. – Vol. 89, № 9. – P. 4673-4677.
68. Fricker L.D., Plummer T.H., Snyder S.H. Enkephalin convertase: potent, selective and irreversible inhibitors // Biochem. and Biophys. Res. Commun. – 1983. – V. 11, № 3. – P. 994-1000.
69. Hanssens M., Keirse M.J., Spitz B., van Assche F.A. Angiotensin II levels in hypertensive and normotensive pregnancies // Br J Obstet Gynaecol. – 1991. – Vol. 98, № 2. – P. 155-161.
70. Hariyama Y., Itakura A., Okamura M., Ito M., Murata Y., Nagasaka T., Nakazato H., Mizutani S. Placental aminopeptidase A as a possible barrier of angiotensin II between mother and fetus // Placenta. – 2000. – Vol. 21, № 7. – P . 621-627.
71. Jojovic M., Wolf F., Mangold U. Epidermal growth factor, vascular endothelial growth factor and progesterone promote placental development in rat whole-embryo culture // Anat Embryol (Berl). – 1998. – Vol. 198, № 2. – P. 133–139.
72. de Jong C.L., Dekker G.A., Sibai B.M. The renin-angiotensin-aldosterone system in preeclampsia. A review // Clin Perinatol. – 1991. – Vol.18, № 4. –Р. 683-711.
73. Grechura M, Opala G. Changes in central nervous system during preeclampsia//Wiad Lek. 2005; P. 58(7-8): 433-6.
74. Ivanchenko SA. The biochemical mechanisms of the metabolic disorders in gestosis// Lik Sprava. 1999; P. 19 – 21
75. Iwase A., Nomura S., Mizutani S. Characterization of a secretase activity for placental leucine aminopeptidase // Arch Biochem Biophys. – 2001. – Vol. 393, № 1. – P. 163-169.
76. Iwashita M., Kudo Y., Shinozaki Y., Takeda Y. Gonadotropin-releasing hormone increases serum human chorionic gonadotropin in pregnant women // Endocr J. – 1993. – Vol. 40, № 5. – P. 539-544.
77. Kingdom J.C., McQueen J., Connell J.M., Whittle M.J. Fetal angiotensin II levels and vascular (type I) angiotensin receptors in pregnancies complicated by intrauterine growth retardation // Br J Obstet Gynaecol. – 1993. – Vol. 100, № 5. – P. 476-482.
78. Krege J.H., Katz V.L. A proposed relationship between vasopressinase altered vasopressin and preeclampsia // Med Hypotheses. – 1990. – Vol. 31, № 4. – P. 283-287.
79. Kreze A Jr, Kothaj P, Dodakova M, Rohon S. Primary aldosteronism caused by aldosterone-producing adenoma in pregnancy – complicated by EPH gestosis//Wien Klin Wochenschr. 1999; P. 111(20) : 855-7
80. Lowry O.H., Rosebrought N.J., Farr A.G., Randall R.J. Protein measurement with Folin phenol reagent // J Biol. Chem. 1951. –Vol. 193, № 1. – P. 256-275.
81. Makatsariia AD, Genievskaia MG. Thrombophilia and fetal loss syndrome //Vestn Ross Akad Med Nauk, 2001; P. 35 – 40
82. Makrigiannakis A., Zoumakis E., Kalantaridou S., Chrousos G., Gravanis A. Uterine and embryonic trophoblast CRH promotes implantation and maintenance of early pregnancy // Ann N Y Acad Sci. – 2003. – Vol. 997. – P. 85-92.
83.
84. Michalski U, Bauer W, Gojowczyk R, Lochle C, Pross E. A rare differential diagnosis a pregnancy gestosis// Dtsch Med Wochenschr. 1999. P. 124(40): 1164-7
85. Reznik S.E., Salafia C.M., Lage J.M., Fricker L.D. Immunohistochemical, localization of carboypeptidases E and D in the human placenta and umbilical cord // Histochem. Cytochem. – 1998. – Vol. 46, № 12. – P. 1359-1368.
86. Salafia C.M. Placental pathology of fetal growth restriction. // Clin.Obstet. Gynecol, 1997; 40: 740–9.
Перепечатка материалов без ссылки на наш сайт запрещена