Контрольная работа: Механизмы реализации путей гибели клетки
Контрольная работа: Механизмы реализации путей гибели клетки
Омский государственный педагогический университет
Кафедра ботаники, цитологии и генетики
дисциплина "Биология клетки"
Контрольная работа
На тему
По цитологии
"Механизмы реализации путей гибели клеток"
По гистологии
"Структурно-функциональная организация крови"
Работу выполнила студентка 6 курса
химико-биологического факультета
специальность "ООСиП"
Арапова Д. Ю.
Работу проверила д. б. н., профессор
кафедры ботаники, цитологии и генетики
Антонова Е. И.
Омск 2010
Содержание работы по цитологии
1. Функции крови
2. Структурно-функциональная организация крови
2.1 Межклеточное вещество – плазма
2.1 Форменные элементы крови - клетки
2.1.1 Гранулярные лейкоциты
2.2.2 Агранулярные лейкоциты
2.3 Постклеточные структуры
2.3.1 Эритроциты
2.3.2 Тромбоциты\кровяные пластинки
3. Иммунитет
4. Гемопоэз
4.1 Стволовые клетки крови
1. Функции крови
Объем крови взрослого мужчины составляет примерно 75 мл на килограмм веса тела; у взрослой женщины этот показатель равен примерно 66 мл. Соответственно общий объем крови у взрослого мужчины - в среднем около 5 л; более половины объема составляет плазма.
По характеристикам существующих форм и функциям, кровь представляет собой уникальный вид соединительной ткани. Она состоит из форменных элементов и межклеточного вещества - плазмы (рис.1).
К форменным элементам крови относятся:
1. клетки:
лимфоциты (Т, В, О, NK-типы);
моноциты.
2. постклеточные структуры:
эритроциты;
Тромбоциты\кровяные пластинки.
Красный цвет крови определяется наличием в эритроцитах красного пигмента гемоглобина.
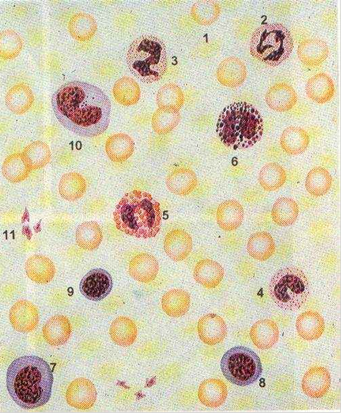
Рис 1. Форменные элементы крови человека в мазке.
1 - эритроцит,
2 - сегментоядерный нейтрофильный гранулоцит,
3 - палочкоядерный нейтрофильный гранулоцит,
4 - юный нейтрофильный гранулоцит,
5 - эозинофильный гранулоцит, 6 - базофильный гранулоцит,
7 - большой лимфоцит,
8 - средний лимфоцит,
9 - малый лимфоцит,
10 - моноцит, 11 - тромбоциты (кровяные пластинки).
Свойства крови:
1. Относительная плотность крови - зависит от количества эритроцитов и белков.
2. Вязкость крови - обусловлена наличием в крови эритроцитов и в меньшей степени белков плазмы.
3. Осмотическое давление крови - сила, с которой растворитель переходит через полунепроницаемую мембрану из менее в более концентрированный раствор. Осмотическое давление крови вычисляют криоскопическим методом путем определения точки замерзания крови (депрессии), которая для нее равна 0,56 - 0,58 С. Осмотическое давление крови в среднем составляет 7,6 атм. Оно обусловлено растворенными в ней осмотически активными веществами, главным образом неорганическими электролитами, в значительно меньшей степени - белками. Около 60% осмотического давления создается солями натрия (NаСl).
Осмотическое давление определяет распределение воды между тканями и клетками. Растворы с более высоким осмотическим давлением, чем давление крови, называются гипертоническими, а имеющие более низкое давление - гипотоническими (рис 2.)
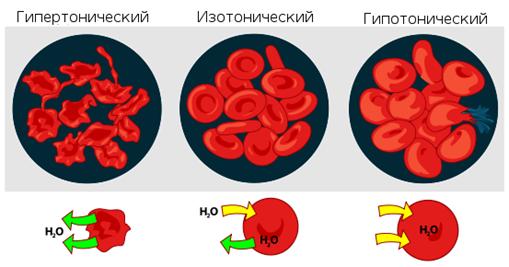
Рис.2. Взаимодействие эритроцитов с растворами в зависимости от их осмотического давления
4. Онкотическое давление крови - часть осмотического давления, создаваемого белками плазмы. Оно равно 0,03 - 0,04 атм, или 25 - 30 мм рт. ст. Онкотическое давление в основном обусловлено альбуминами. Вследствие малых размеров и высокой гидрофильности они обладают выраженной способностью притягивать к себе воду, за счет чего она удерживается в сосудистом русле, При снижении онкотического давления крови происходит выход воды из сосудов в интерстициальное пространство, что приводит к отеку тканей.
5. Кислотно-основное состояние крови (КОС). Активная реакция крови обусловлена соотношением водородных и гидроксильных ионов. Для определения активной реакции крови используют водородный показатель рН - концентрацию водородных ионов, которая выражается отрицательным десятичным логарифмом молярной концентрации ионов водорода. В норме рН - 7,36 (реакция слабоосновная); артериальной крови - 7,4; венозной - 7,35. При различных физиологических состояниях рН крови может изменяться от 7,3 до 7,5. Активная реакция крови является жесткой константой, обеспечивающей ферментативную деятельность. Крайние пределы рН крови, совместимые с жизнью, равны 7,0 - 7,8. Сдвиг реакции в кислую сторону называется ацидозом, который обусловливается увеличением в крови водородных ионов. Сдвиг реакции крови в щелочную сторону называется алкалозом. Это связано с увеличением концентрации гидроксильных ионов ОН и уменьшением концентрации водородных ионов.
В организме человека всегда имеются условия для сдвига активной реакции крови в сторону ацидоза или алкалоза, которые могут привести к изменению рН крови. В клетках тканей постоянно образуются кислые продукты. Накоплению кислых соединений способствует потребление белковой пищи. Напротив, при усиленном потреблении растительной пищи в кровь поступают основания. Поддержание постоянства рН крови является важной физиологической задачей и обеспечивается буферными системами крови. К буферным системам крови относятся гемоглобиновая, карбонатная, фосфатная и белковая.
6. Буферные системы нейтрализуют значительную часть поступающих в кровь кислот и щелочей, тем самым препятствуя сдвигу активной реакции крови.
Гемоглобиновая буферная система на 75% обеспечивает буферную емкость крови. Оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Оксигемоглобин обычно бывает в виде калиевой соли. В капиллярах тканей в кровь поступает большое количество кислых продуктов распада. Одновременно в тканевых капиллярах при диссоциации оксигемоглобина происходит отдача кислорода и появление большого количества щелочно реагирующих солей гемоглобина, Последние взаимодействуют с кислыми продуктами распада, например угольной кислотой. В результате образуются бикарбонаты и восстановленный гемоглобин, В легочных капиллярах гемоглобин, отдавая ионы водорода, присоединяет кислород и становится сильной кислотой, которая связывает ионы калия. Ионы водорода используются для образования угольной кислоты, в дальнейшем выделяющейся из легких в виде Н2О и СО2.
Карбонатная буферная система по своей мощности занимает второе место. Она представлена угольной кислотой (Н2СО3) и бикарбонатом натрия или калия (NaНСО3, КНСО3) в пропорции 1/20. Если в кровь поступает кислота, более сильная, чем угольная, то в реакцию вступает, например, бикарбонат натрия. Образуются нейтральная соль и слабодиссоциированная угольная кислота. Угольная кислота под действием карбоангидразы эритроцитов распадается на Н2О и СО2, последний выделяется легкими в окружающую среду. Если в кровь поступает основание, то в реакцию вступает угольная кислота, образуя гидрокарбонат натрия и воду. Избыток бикарбоната натрия удаляется через почки. Бикарбонатный буфер широко используется для коррекции нарушений кислотно-основного состояния организма.
Фосфатная буферная система состоит из натрия дигидрофосфата (NаН2РО4) и натрия гидрофосфата (Nа2НРО4). Первое соединение обладает свойствами слабой кислоты и взаимодействует с поступившими в кровь щелочными продуктами. Второе соединение имеет свойства слабой щелочи и вступает в реакцию с более сильными кислотами.
Белковая буферная система осуществляет роль нейтрализации кислот и щелочей благодаря амфотерным свойствам: в кислой среде белки плазмы ведут себя как основания, в основной - как кислоты.
7. Кровь состоит из жидкой части плазмы и взвешенных в ней форменных элементов: эритроцитов, лейкоцитов и тромбоцитов. На долю форменных элементов приходится 40 - 45%, на долю плазмы - 55 - 60% от объема крови. Это соотношение получило название гематокритного соотношения, или гематокритного числа. Часто под гематокритным числом понимают только объем крови, приходящийся на долю форменных элементов.
8. В клинике имеет значение не только общее количество лейкоцитов, но и процентное соотношение всех видов лейкоцитов, получившее название лейкоцитарной формулы, или лейкограммы.
Лейкоцитарная формула здорового человека (в %)
| Гранулоциты | Агранулоциты | |||||
| Нейтрофилы |
Палочко- ядерные |
Сегменто- ядерные |
Базофилы | Эозинофилы | Лимфоциты | Моноциты |
| 0-1 | 1-5 | 45-65 | 0-1 | 1-5 | 25-40 | 2-8 |
9. Скорость оседания эритроцитов (СОЭ).
Скорость оседания эритроцитов у здоровых мужчин составляет 2 - 10 мм в час, у женщин - 2 - 15 мм в час (табл.1). СОЭ зависит от многих факторов: количества, объема, формы и величины заряда эритроцитов, их способности к агрегации, белкового состава плазмы.
В большей степени СОЭ зависит от свойств плазмы, чем эритроцитов. СОЭ увеличивается при беременности, стрессе, воспалительных, инфекционных и онкологических заболеваниях, при уменьшении числа эритроцитов, при увеличении содержания фибриногена. СОЭ снижается при увеличении количества альбуминов.
Многие стероидные гормоны (эстрогены, глюкокортикоиды), а также лекарственные вещества (салицилаты) вызывают повышение СОЭ.
Таблица 1.
Показатели СОЭ в норме
| Возраст | СОЭ, мм/ч |
| Новорожденные | 0-2 |
| Младенцы (до 6 мес) | 12-17 |
| Женщины (моложе 60 лет) | До 12 |
| Женщины (старше 60 лет) | " 20 |
| Мужчины (моложе 60 лет) | " 8 |
| Мужчины (старше 60 лет) | " 15 |
| При определении по Вестергрену | " 20 |
10. Одно из важнейших свойств крови - текучесть - составляет предмет изучения биореологии. В кровеносном русле кровь в норме ведёт себя как не Ньютоновская жидкость, меняющая свою вязкость в зависимости от условий течения. В связи с этим вязкость крови в крупных сосудах и капиллярах существенно различается, а приводимые в литературе данные по вязкости носят условный характер. Закономерности течения крови (реология крови) изучены недостаточно. Неньютоновское поведение крови объясняется большой объёмной концентрацией клеток крови, их асимметрией, присутствием в плазме белков и другими факторами. При патологии и травмах текучесть крови существенно изменяется вследствие действия определённых факторов свёртывающей системы крови.
Измеряемая на капиллярных вискозиметрах (с диаметром капилляра несколько десятых миллиметра) вязкость крови в 4-5 раз выше вязкости воды. В основном работа этой системы заключается в ферментативном синтезе линейного полимера - фабрина, образующего сетчатую структуру и придающего крови свойства студня. Этот "студень" имеет вязкость, в сотни и тысячи превышающую вязкость крови в жидком состоянии, проявляет прочностные свойства и высокую адгезивную способность, что позволяет сгустку удерживаться на ране и защищать её от механических повреждений.
Образование сгустков на стенках кровеносных сосудов при нарушении равновесия в свёртывающей системе является одной из причин тромбозов. Образованию сгустка фибрина препятствует противосвёртывающая система крови; разрушение образовавшихся сгустков происходит под действием фибринолитической системы. Образовавшийся сгусток фибрина вначале имеет рыхлую структуру, затем становится более плотным, происходит ретракция сгустка.
Функции крови.
Функции крови значительно сложнее, чем просто транспорт питательных веществ и отходов метаболизма. С кровью переносятся также гормоны, контролирующие множество жизненно важных процессов; кровь регулирует температуру тела и защищает организм от повреждений и инфекций в любой его части.
Кровь выполняет следующие функции:
1) трофическую - перенос питательных веществ ко всем клеткам и тканям;
2) дыхательную - газообменную, или транспорт кислорода к тканям и удаление из организма углекислоты;
3) защитную (обеспечение гуморального и клеточного иммунитета, свертывание крови при травмах - фагоцитоз, выработка антител);
В осуществлении этой функции крови особую роль играют лейкоциты двух типов: полиморфноядерные нейтрофилы и моноциты. Они устремляются к месту повреждения и накапливаются вблизи него, причем большая часть этих клеток мигрирует из кровотока через стенки близлежащих кровеносных сосудов. К месту повреждения их привлекают химические вещества, высвобождаемые поврежденными тканями. Эти клетки способны поглощать бактерии и разрушать их своими ферментами. Таким образом, они препятствуют распространению инфекции в организме. Лейкоциты принимают также участие в удалении мертвых или поврежденных тканей. Процесс поглощения клеткой бактерии или фрагмента мертвой ткани называется фагоцитозом, а осуществляющие его нейтрофилы и моноциты - фагоцитами. Активно фагоцитирующий моноцит называют макрофагом, а нейтрофил - микрофагом.
В борьбе с инфекцией важная роль принадлежит белкам плазмы, а именно иммуноглобулинам, к которым относится множество специфических антител. Антитела образуются другими типами лейкоцитов - лимфоцитами и плазматическими клетками, которые активируются при попадании в организм специфических антигенов бактериального или вирусного происхождения (либо присутствующих на клетках, чужеродных для данного организма). Выработка лимфоцитами антител против антигена, с которым организм встречается в первый раз, может занять несколько недель, но полученный иммунитет сохраняется надолго. Хотя уровень антител в крови через несколько месяцев начинает медленно падать, при повторном контакте с антигеном он вновь быстро растет. Это явление называется иммунологической памятью. При взаимодействии с антителом микроорганизмы либо слипаются, либо становятся более уязвимыми для поглощения фагоцитами. Кроме того, антитела мешают вирусу проникнуть в клетки организма хозяина.
4) регуляторную - транспорт гормонов и других гуморальных факторов регуляции;
Кровь играет ключевую роль в поддержании постоянной температуры тела у гомойотермных, или теплокровных, организмов. Температура человеческого тела в нормальном состоянии колеблется в очень узком интервале около 370 С. Выделение и поглощение тепла различными участками тела должны быть сбалансированы, что достигается переносом тепла с помощью крови. Центр температурной регуляции располагается в гипоталамусе - отделе промежуточного мозга. Этот центр, обладая высокой чувствительностью к небольшим изменениям температуры проходящей через него крови, регулирует те физиологические процессы, при которых выделяется или поглощается тепло. Один из механизмов состоит в регуляции тепловых потерь через кожу посредством изменения диаметра кожных кровеносных сосудов кожи и соответственно объема крови, протекающей вблизи поверхности тела, где тепло легче теряется. В случае инфекции определенные продукты жизнедеятельности микроорганизмов либо продукты вызванного ими распада тканей взаимодействуют с лейкоцитами, вызывая образование химических веществ, стимулирующих центр температурной регуляции в головном мозге. В результате наблюдается подъем температуры тела, ощущаемый как жар.
5) гомеостатическую - поддержание физико-химического постоянства состава внутренней среды организма, в том числе иммунного гомеостаза рН крови. pH - это показатель концентрации водородных (H) ионов, численно равный отрицательному логарифму (обозначаемому латинской буквой "p") этой величины. Кислотность и щелочность растворов выражают в единицах шкалы рН, имеющей диапазон от 1 (сильная кислота) до 14 (сильная щелочь). В норме рН артериальной крови составляет 7,4, т.е. близок к нейтральному. Венозная кровь из-за растворенного в ней диоксида углерода несколько закислена: диоксид углерода (СО2), образующийся в ходе метаболических процессов, при растворении в крови реагирует с водой (Н2О), образуя угольную кислоту (Н2СО3).
Поддержание рН крови на постоянном уровне, т.е., другими словами, кислотно-щелочного равновесия, исключительно важно. Так, если рН заметно падает, в тканях снижается активность ферментов, что опасно для организма. Изменение рН крови, выходящее за рамки интервала 6,8-7,7, несовместимо с жизнью. Поддержанию этого показателя на постоянном уровне способствуют, в частности, почки, поскольку они по мере надобности выводят из организма кислоты или мочевину (которая дает щелочную реакцию). С другой стороны, рН поддерживается благодаря присутствию в плазме определенных белков и электролитов, обладающих буферным действием (т.е. способностью нейтрализовать некоторый избыток кислоты или щелочи).
6) выделительная (удаление и транспортировка в почки продуктов обмена веществ);
Конечные продукты обмена (шлаки), которые не могут быть использованы, подлежат удалению из организма. Важнейшие из них - это двуокись углерода, мочевина, мочевая кислота, креатинин, билирубин и аммиак. Все эти вещества, кроме углекислого газа, содержат азот и выводятся почками. При нарушении функции почек уровень азотсодержащих продуктов обмена в крови увеличивается.
7) Транспортная функция. С кровью и кровоснабжением тесно связаны практически все процессы, имеющие отношение к пищеварению и дыханию - двум функциям организма, без которых жизнь невозможна. Связь с дыханием выражается в том, что кровь обеспечивает газообмен в легких и транспорт соответствующих газов: кислорода - от легких в ткани, диоксида углерода (углекислого газа) - от тканей к легким. Транспорт питательных веществ начинается от капилляров тонкого кишечника; здесь кровь захватывает их из пищеварительного тракта и переносит во все органы и ткани, начиная с печени, где происходит модификация питательных веществ (глюкозы, аминокислот, жирных кислот), причем клетки печени регулируют их уровень в крови в зависимости от потребностей организма (тканевого метаболизма). Переход транспортируемых веществ из крови в ткани осуществляется в тканевых капиллярах; одновременно в кровь из тканей поступают конечные продукты, которые далее выводятся через почки с мочой (например, мочевина и мочевая кислота). Кровь переносит также продукты секреции эндокринных желез - гормоны - и тем самым обеспечивает связь между различными органами и координацию их деятельности.
Вещества переносимые плазмой: Электролиты и белки плазмы оказывают влияние на ее функции. Кроме того, существует группа веществ, для которых плазма является просто переносчиком и которые в физиологических концентрациях мало влияют на ее свойства. Эта неоднородная группа включает: питательные вещества, витамины и микроэлементы; продукты промежуточного обмена; гормоны и ферменты; вещества, подлежащие выведению (конечные продукты обмена).
2. Структурно-функциональная организация крови 2.1 Межклеточное вещество – плазма
Плазма крови является средой, в которой взвешены форменные элементы; она содержит ряд неорганических ионов и органических веществ, обеспечивающих трофическую, регуляторную, защитную, гомеостатическую функции крови, а так же обуславливающих ее свертывание, участвует в газообмене, содержит буферные системы, способствующие (вместе с буферной системой гемоглобина) поддержанию стабильных значений рН (около 7,36) (табл.1).
Состав плазмы крови: 90% воды, 9% органических веществ и 1 % неорганических. Главные органические компоненты плазмы - белки (более 200 видов), которые обеспечивают ее вязкость, онкотическое давление, свертываемость, переносят различные вещества и выполняют защитные функции. Содержание белков в плазме крови составляет 6,5 - 8 г/дл. Их молекулярные веса варьируют от 44 000 до 1 300 000, а диаметр молекул - от 1 до 100 нм.
Основные белки плазмы:
альбумины - количественно преобладающие белки плазмы крови (по содержанию в 1,3 - 2,2 раза превосходят глобулины) - переносят ряд метаболитов, гормонов, ионов, поддерживают онкотическое давление крови;
Альбумин составляет примерно 60% от общего количества белков плазмы крови, т.е.3,5 - 4,5 г/дл. Молекулярный вес его - 69 000. Так как концентрация альбумина высока, а размеры молекулы невелики, этот белок на 80% определяет коллоидно-осмотическое давление плазмы. Общая площадь поверхности множества молекул альбумина очень велика, и поэтому они очень хорошо подходят для выполнения функции переносчиков многих транспортируемых кровью веществ, таких как билирубин, уробилин, жирные кислоты, соли желчных кислот и некоторые экзогенные вещества: пенициллин, сульфонамиды, ртуть и др. Одна молекула альбумина может одновременно связать 25 - 50 молекул билирубина. При многих патологических состояниях содержание альбумина снижается.
Неферментативное гликозилирование белков, обусловленное гипергликемией, приводит к образованию гликозилированных белков: гемоглобина, альбумина, коллагена, белков хрусталика, липопротеидов.
глобулины (α - и β-) переносят ионы металлов и липиды в форме липопротеинов; γ - глобулины представляют собой фракцию антител (иммуноглобулинов);
Глобулинами называется целая группа белков, которые могут быть разделены электорофоретически. В порядке убывания электорофоретической подвижности различают альфа-1-глобулин, альфа-2-глобулин, бета-глобулин и гамма-глобулин. Однако даже эти субфракции не состоят из однородных белков, каждую из них можно разделить при помощи других методов, например, иммуноэлектрофореза.
В составе фракции альфа-1-глобулинов мигрирует ряд конъюгированных белков, простетической группой которых являются углеводы - преимущественно гексозы и гексозамины. Эти белки называются гликопротеинами. Около 2/3 всей глюкозы плазмы циркулирует в составе гликопротеинов. Эту связанную глюкозу невозможно определить клиническими пробами на сахар в плазме, лишенной белков, она может быть измерена лишь после ее отделения от белков методом кислотного гидролиза. К субфракции гликопротеинов относится еще одна группа углеводсодержащих белков - мукопротеины, в состав которых входят мукополисахариды.
Фракция альфа-2-глобулинов включает гаптоглобины, относящиеся по химическому строению к мукопротеинам, и медьсодержащий белок церулоплазмин. На каждую молекулу его приходится 8 атомов меди, он связывает около 90% всей меди, содержащейся в плазме. К другим белкам из фракции альфа-2-глобулинам относятся тироксинсвязывающий белок, витамин В-12 - связывающий глобулин (транскобаламин), билирубинсвязывающий глобулин и кортизолсвязывающий глобулин (транскортин).
К бета-глобулинам относятся важнейшие белковые переносчики липидов и белковые переносчики полисахаридов. Важное значение липопротеинов состоит в том, что они удерживают в растворе нерастворимые в воде жиры и липоиды и обеспечивают тем самым их перенос кровью. Около 75% всех жиров и липоидов плазмы входят в состав липопротеинов. Небольшие количества липопротеинов обнаруживаются и в альфа-1 - фракции глобулинов, однако большинство их принадлежит к бета-глобулинам, самый главный из них - бета-1-липопротеин, молекула которого на 77% состоит из липидов. Кроме липопреотеинов к бета - глобулинам относится группа металсодержащих белков, один из которых - трансферин - является белком - переносчиком меди и белком - переносчиком железа. Каждая молекула трансферина содержит два атома трехвалентного железа, именно трансферин обеспечивает транспорт железа кровью.
К неоднородной группе гамма-глобулинов относятся белки с самой низкой электрофоретической подвижностью. К ним относится большинство защитных веществ крови, многие из которых обладают ферментативной активностью. Так как потребности в белках, выполняющих такие специальные функции, бывают различны, размеры и состав фракции гамма-глобулинов может значительно изменяться. Почти при всех заболеваниях, особенно воспалительных, содержание гамма-глобулинов в плазме крови повышается. В то же время общее количество белков в плазме обычно остается примерно одинаковым, так как повышение содержания гамма-глобулинов сопровождается уменьшением фракции альбумина, в результате снижается так называемый альбумин-глобулиновый коэффициент.
К гамма-глобулинам относятся также альфа-агглютинины и бета - агглютинины крови.
фибриноген - обеспечивает свертывание крови, превращаясь в нерастворимый белок фибрин под действием тромбина;
Фибриноген выявляется в виде узкой отдельной полоски между фракциями бета-глобулинов и гамма-глобулинов. Этот белок представляет собой растворимый предшественник фибрина, который участвует в образовании сгустка крови.
Молекула фибриногена вытянута, соотношение осей (длина/ширина) составляет 17:
1. Высокая вязкость растворов фибриногена обусловлена способностью его молекул образовывать агрегаты в виде четок.
компоненты комплемента - участвуют в неспецифических защитных реакциях.
Выработка белков плазмы осуществляется клетками печени (за исключением γ - глобулинов, которые продуцируются плазматическими клетками).
При нормальном питании в организме человека за сутки вырабатывается около 15 г альбумина и 5 г глобулина. Период полураспада альбумина составляет 10 - 15 дней, а глобулина - 5 дней (т.е. за это время 50% общего количества белка сменяется новосинтезированным).
Сыворотка крови - жидкость, остающаяся после свертывания крови. По своему составу она сходна с плазмой крови, однако в ней отсутствуют фибриноген и факторы свертывания.
Сыворотка является сложной смесью множества биологических молекул с различными физиологическими активностями. К основным компонентам сыворотки, необходимым для выживания и роста клеток млекопитающих в культуре относятся: белки плазмы (альбумины, фибронектин, альфа 2-макроглобулин, фетуин, трансферрин; полипептидные факторы роста (инсулин, инсулиноподобные факторы роста I и II (IGF), PDGF, EGF); глютатион; непептидные гормоны (кортизол, гидрокортизон), эстрогены, андрогены, тиреоидные гормоны (T3, T4); липиды (линоевая кислота, холестерин, лизофосфатидная кислота, простагландины); метаболиты (аминокислоты, альфа-кетокислоты (пируват), полиамины); минеральные вещества (Fe2+, Zn2+, Cu2+, Mn2+, SeO32+, Co2+, VO3-, Mo-) (Maurer H. R., 1986).
Важнейшие функции сыворотки обеспечиваются:
1) факторами, стимулирующими клеточный рост;
2) факторами прикрепления и распластывания (матрикс);
3) транспортными белками, переносящими некоторые гормоны, минеральные вещества, липиды и т.д. (Barnes D., Sato G., 1980).
Большинство факторов роста присутствует в сыворотке в очень малых концентрациях (порядка 10-10 M). Некоторые из них оказывают влияние лишь на клетки строго определенного типа дифференцировки, например гематопоэтические факторы роста. Другие же обладают широким спектром действия. Эпидермальный фактор роста, например, стимулирует пролиферацию фибробластов, эпидермальных и глиальных клеток.
Среди гормонов инсулин является наиболее существенным для роста почти всех типов клеток в культуре. Так как он имеет короткое время полужизни и чувствителен к инактивации цистеином, его обычно вносят в среду в высоких концентрациях.
Глюкокортикоиды (гидрокортизон, дексаметазон) могут стимулировать или ингибировать размножение клеток в культуре в зависимости от типа клеток и плотности культуры. Они могут модулировать клеточную пролиферацию путем изменения ответа на факторы роста.
Некоторые клеточные линии требуют для роста особых стероидных гормонов (эстрадиола, тестостерона, прогестерона).
Сыворотка содержит также белки, функцией которых является связывание молекул с низким молекулярным весом. Альбумин связывает витамины, липиды (жирные кислоты, холестерин), стероидные гормоны и т.д. Железонасыщенный трансферрин необходим для большинства клеток в культуре, многие из которых обладают специфичными трансферриновыми рецепторами на поверхности.
Сыворотка является также источником различных липидов, необходимых для выживания и роста культивируемых клеток. Клеточные линии различаются по их потребности в жирных кислотах, фосфолипидах, лецитине и холестерине.
Роль различных неорганических элементов, содержащихся в сыворотке в следовых количествах (Cu, Zn, Co, Mn, Mo, Va, Se) выяснена не до конца, но известно, что многие из них действуют как кофакторы ферментов. SeO32 - требуется для активации ряда ферментов, участвующих в метаболической детоксикации. Селен участвует также в инактивации свободных радикалов.
Таблица 2.
Белковые фракции плазмы крови человека
| Белковая фракция | Белковая фракция | Средняя концентрация |
Мол. вес Х 1000 |
Изоэлек-трическая точка | Физиологическое значение |
|
Электрофо- ретическая |
Иммунофо-ретическая | ||||
| Альбумин | Преальбумин | 30 | 61 | 4,7 | Частичное связывание тироксина, онкотическое давление, транспортная функция, белковый резерв |
| Альбумин | Альбумин | 4000 | 69 | 4,9 | Частичное связывание тироксина, онкотическое давление, транспортная функция, белковый резерв |
| альфа - глобулины |
Кислый альфа1 - гликопротеин |
80 | 44 | 2,7 | Продукт распада тканей |
| - " - | альфа1 - Липо | 350 | 200 | 5,1 | Транспорт липидов (в частности, фосфолипидов) |
| альфа2-Глобу - лины | Церулоплазмин | 30 | 160 | 4,4 | Обладает оксидазной активностью |
| альфа2-Глобу - лины | альфа2 - Макроглобулин | 250 | 820 | 5,4 | Ингибирует плазмин и протеиназы |
| альфа2-Глобу - лины | альфа2 - Гаптоглобулин | 100 | 85 | 4,1 | Связывает гемоглобин и препятствует его выведению с мочой |
| бета-Глобу - лины | Трансферин | 300 | 90 | 5,8 | Транспорт железа |
| бета-Глобу - лины | бета-Липо - протеин | 550 | 3000-20000 | - | Транспорт липидов (в частности, холестерина) |
| Фибриноген | 400 | 340 | 5,8 | Свертывание крови | |
| гамма-Глобу - лины | гамма-Глобу - лины | 1200 | 156 | 5,8 | Иммуноглобулины: антитела протиы бактериальных антигенов и инородных белков. |
| гамма-Глобу - лины | гаммаА-Глобу - лин | 240 | 150 | 7,3 | |
| гамма-Глобу - лины | гаммаМ-Глобу - лин | 125 | 960 | "Естественные антитела" (напр., изогемагглютинины) | |
| гамма-Глобу - лины | гаммаЕ-Глобу - лин | 0,03 | 190 | Антитела |
Функции плазмы крови.
1. Питательная функция:
В организме человека содержится около 3 л плазмы, в которой растворено примерно 200 г белка. Это вполне достаточный запас питательных веществ. Обычно клетки захватывают не столько белки, сколько аминокислоты, однако некоторые клетки могут захватывать белки плазмы и расщеплять их при помощи собственных внутриклеточных ферментов. Высвобождающиеся при этом аминокислоты поступают в кровь, где сразу же могут использоваться другими клетками для синтеза новых белков.
2. Транспортная функция:
Многие небольшие молекулы при переносе их от кишечника или депо к месту потребления связываются со специфическими белками плазмы.
Все белки плазмы связывают катионы крови и переводят их в недифффундирующую форму. Так, около 2/3 кальция плазмы неспецифически связано с белками. Связанный кальций находится в равновесии со свободно растворенным в плазме ионизированным физиологически активным кальцием.
2.1 Форменные элементы крови - клетки 2.1.1 Гранулярные лейкоцитыЛейкоциты (leucocytus), или белые кровяные клетки, в свежей крови бесцветны, что отличает их от окрашенных эритроцитов. Число их составляет в среднем 4-9 109/л, т.е. в 1000 раз меньше, чем эритроцитов. Лейкоциты в кровяном русле и лимфе способны к активным движениям, могут переходить через стенку сосудов в соединительную ткань органов, где они выполняют основные защитные функции. По морфологическим признакам и биологической роли лейкоциты подразделяют на две группы: зернистые лейкоциты, или гранулоциты (granulocytus), и незернистые лейкоциты, или агранулоциты (agranulocytus).
К гранулоцитам относятся нейтрофильные, эозинофильные и базофильные лейкоциты. Они образуются в красном костном мозге, содержат специфическую зернистость в цитоплазме и сегментированные ядра.
У зернистых лейкоцитов при окраске крови по Романовскому - Гимзе смесью кислого (эозин) и основного (азур II) красителей в цитоплазме выявляются специфическая зернистость (эозинофильная, базофильная или нейтрофильная) и сегментированные ядра. В соответствии с окраской специфической зернистости различают нейтрофильные, эозинофильные и базофильные гранулоциты. Группа незернистых лейкоцитов (лимфоциты и моноциты) характеризуется отсутствием специфической зернистости и несегментированными ядрами. Процентное соотношение основных видов лейкоцитов называется лейкоцитарной формулой.
Общее число лейкоцитов и их процентное соотношение у человека могут изменяться в норме в зависимости от употребляемой пищи, физического и умственного напряжения, при различных заболеваниях. Поэтому исследование показателей крови является необходимым для установления диагноза и назначения лечения. Концентрация лейкоцитов в крови у взрослого в норме составляет 4000-8000 клеток/мкл (по некоторым данным верхняя граница нормы достигает 10000). Концентрация лейкоцитов у детей в норме меняется в зависимости от возраста: у новорожденных она равняется 10000-30000 клеток/мкл, на 4 день снижается до 12000, к 4-м годам составляет 8000 клеток/мкл. Уровня, характерного для взрослого, этот показатель достигает примерно к 12-14 годам. С возрастом происходят изменения не только количества, но и качественного состава лейкоцитов.
Все лейкоциты способны к активному перемещению путем образования псевдоподий, при этом у них изменяются форма тела и ядра. Они способны проходить между клетками эндотелия сосудов и клетками эпителия, через базальные мембраны и перемещаться по основному веществу (матриксу) соединительной ткани. Скорость движения лейкоцитов зависит от следующих условий: температуры, химического состава, рН, консистенции среды и др. Направление движения лейкоцитов определяется хемотаксисом под влиянием химических раздражителей - продуктов распада тканей, бактерий и др. Лейкоциты выполняют защитные функции, обеспечивая фагоцитоз микробов (гранулоциты, макрофаги), инородных веществ, продуктов распада клеток (моноциты - макрофаги), участвуя в иммунных реакциях (лимфоциты, макрофаги).
Нейтрофилы (нейтрофильные лейкоциты, или нейтрофилы) - самая многочисленная группа лейкоцитов, составляющая 2,0-5,5 109/л крови D8-78 % от общего числа лейкоцитов (рис.3). Их диаметр в мазке крови 10-12 мкм, а в капле свежей крови 7-9 мкм. В зрелом сегментоядерном нейтрофиле ядро содержит 3-5 сегментов, соединенных тонкими перемычками. В ядре гетерохроматин занимает широкую зону по периферии ядра, а эухроматин расположен в центре. Для женщин характерно наличие в ряде нейтрофилов полового хроматина (Х-хромосома) в виде барабанной палочки - тельца Барра. В популяции нейтрофилов крови могут находиться клетки различной степени зрелости - юные, палочкоядерные и сегментоядерные. Первые два вида - молодые клетки. Юные клетки в норме не превышают 0,5 % или отсутствуют, они характеризуются бобовидным ядром. Палочкоядерные составляют 1-6%, имеют несегментированное ядро в форме буквы S, изогнутой палочки или подковы. Увеличение в крови количества юных и палочкоядерных форм нейтрофилов свидетельствует о наличии кровопотери или воспалительного процесса в организме, сопровождаемых усилением гемопоэза в костном мозге и выходом молодых форм.

Рис.3. Нейтрофильный гранулоцит
Цитоплазма нейтрофилов при окраске по Романовскому - Гимзе окрашивается слабооксифильно, в ней видна очень мелкая зернистость розово-фиолетового цвета (окрашивается кислыми и основными красками), поэтому называется нейгрофильной или гетерофильной. В поверхностном слое цитоплазмы зернистость и органеллы отсутствуют. Здесь расположены гранулы гликогена, актиновые филаменты и микротрубочки, обеспечивающие образование псевдоподий для движения клетки. Сокращение актиновых филаментов обеспечивает передвижение клетки по соединительной ткани.
Во внутренней части цитоплазмы расположены органеллы (аппарат Гольджи, гранулярный эндоплазматический ретикулум, единичные митохондрии), видна зернистость. Число зерен в каждом нейтрофиле варьирует и составляет 50-200.
В нейтрофилах можно различить два типа гранул: специфические и азурофильные, окруженные одинарной мембраной. Специфические гранулы, более светлые, мелкие и многочисленные, составляют 80-90 % всех гранул. Их размер около 0,2 мкм, они электронно-прозрачны, но могут содержать кристаллоид; содержат бактериостатические и бактерицидные вещества - лизоцим (муромидаза) и щелочную фосфатазу, а также белок лактоферрин. Лактоферрин связывает ионы железа, что способствует склеиванию бактерий (бактериальная мультипликация). Он также инициирует отрицательную обратную связь, обеспечивая торможение продукции нейтрофилов в костном мозге. Азурофильные гранулы более крупные (~ 0,4 мкм), окрашиваются в фиолетово-красный цвет; их количество составляет 10-20 % всей популяции гранул. Они являются первичными лизосомами, имеют электронно-плотную сердцевину, содержат лизосомальные ферменты (кислая фосфатаза, р-глюкуронидаза и др.) и миелопероксидазу. Миелопероксидаза из перекиси водорода продуцирует молекулярный кислород, обладающий бактерицидным действием. Азурофильные гранулы в процессе дифференцировки нейтрофилов в костном мозге появляются раньше, поэтому называются первичными в отличие от вторичных - специфических. Основная функция нейтрофилов - фагоцитоз микроорганизмов, поэтому их называют микрофагами. В процессе фагоцитоза бактерий сначала (в течение 0,5-1 мин) с образующейся фагосомой (захваченная бактерия) сливаются специфические гранулы, ферменты которой убивают бактерию, при этом образуется комплекс, состоящий из фагосомы и специфической гранулы. Позднее с этим комплексом сливается лизосома, гидролитические ферменты которой переваривают микроорганизмы. В очаге воспаления убитые бактерии и погибшие нейтрофилы образуют гной.
Фагоцитоз усиливается при опсонизации с помощью иммуноглобулинов (Ig) или комплемента плазмы. Это так называемый рецепторопосредованный фагоцитоз. Если у человека имеются антитела IgG для конкретного вида бактерий, то бактерия обволакивается этим специфическим IgG, имеющим специальную область Fc, которая распознается Fc-рецептором на плазмолемме нейтрофила и присоединяется к нему. Образующееся соединение [IgG - Fc-рецептор] на поверхности нейтрофила запускает фагоцитоз. В популяции нейтрофилов здоровых людей в возрасте 18-45 лет фагоцитирующие клетки составляют 69-99 %. Этот показатель называют фагоцитарной активностью. Фагоцитарный индекс - другой показатель, которым оценивается число частиц, поглощенных одной клеткой. Для нейтрофилов он равен 12-23. Продолжительность жизни нейтрофилов составляет 5-9 суток.
Эозинофилы (оксифильные или ацидофильные лейкоциты, эозинофилы). Количество эозинофилов в крови составляет 0,02 - 0,3 ¦ 10*/л, или 0,5-5 % от общего числа лейкоцитов (рис.4). Их диаметр в мазке крови 12-14 мкм, в капле свежей крови - 9-10 мкм. Ядро эозинофилов имеет, как правило, 2 сегмента, соединенных перемычкой. В цитоплазме расположены органеллы - аппарат Гольджи (около ядра), немногочисленные митохондрии, актиновые филаменты в кортексе цитоплазмы под плазмолеммой и гранулы. Среди гранул различают азурофильные (первичные) и эозинофильные (вторичные), являющиеся модифицированными лизосомами. Они электронно-плотные, содержат гидролитические ферменты (см. рис.70, Б в приложении).
Специфические эозинофильные гранулы заполняют почти всю цитоплазму, имеют размер 0,6-1 мкм. Характерно наличие в центре гранулы кристаллоида, который содержит главный основной белок, богатый аргинином (что обусловливает оксифилию гранул), лизосомные гидролитические ферменты, пероксидазу и другие белки - эозинофильный катионный белок, гистаминазу.
Электронно - микроскопически в экваториальной плоскости эозинофильных гранул выявляются единичные или множественные кристаллоидные структуры, имеющие пластинчатое строение, погруженные в тонкозернистый матрикс гранулы. Кристаллоиды эозинофильных гранул содержат главный основной белок, который участвует в антипаразитарной функции эозинофилов.
Плазмолемма имеет рецепторы: Fc-рецептор для иммуноглобулина Е (IgE) (участвует в аллергических реакциях), для IgG и igM, а также С3 - и С4-рецепторы. Эозинофилы являются подвижными клетками и способны к фагоцитозу, однако их фагоцитарная активность ниже, чем у нейтрофилов.
Эозинофилы обладают положительным хемотаксисом к гистамшу, выделяемому тучными клетками (особенно при воспалении и аллергических реакциях), к лимфокинам, выделяемым стимулированными Т-лимфоцитами, и иммунным комплексам, состоящим из антигенов и антител.
Рис.4. Эозинофильный гранулоцит
Установлена роль эозинофилов в реакциях на чужеродный белок, в аллергических и анафилактических реакциях, где они участвуют в метаболизме гистамина, вырабатываемого тучными клетками. Гистамин повышает проницаемость сосудов, вызывает развитие отека тканей; в больших дозах может вызвать шок со смертельным исходом.
Эозинофилы способствуют снижению содержания гистамина в тканях различными путями. Они разрушают гистамин с помощью фермента гистаминазы, фагоцитируют гистаминсодержащие гранулы тучных клеток, адсорбируют гистамин на плазмолемме, связывая его с помощью рецепторов, и, наконец, вырабатывают фактор, тормозящий дегрануляцию и освобождение гистамина из тучных клеток. Специфической функцией эозинофилов является антипаразитарная. При паразитарных заболеваниях (гельминтозы, шистосомоз и др.) наблюдается резкое увеличение числа эозинофилов - до 90 % от общего числа лейкоцитов. Эозинофилы убивают личинки паразитов, поступившие в кровь или органы (например, в слизистую оболочку кишки).
Они привлекаются в очаги воспаления хемотаксическими факторами и прилипают к паразитам благодаря наличию на них обволакивающих компонентов комплемента. При этом происходят дегрануляция эозинофилов и выделение главного основного белка, оказывающего антипаразитарное действие.
Таким образом, эозинофилы являются первой линией защиты против паразитов. Они участвуют в убийстве этих агентов при выделении содержимого гранул после активации антителами и комплементом. Активация сочетается со слиянием гранул, их выделением, повышением скорости метаболизма и экспрессией рецепторов Fc и комплемента. Эозинофилы находятся в периферической крови менее 12 ч и потом переходят в ткани. Их мишенями являются такие органы, как кожа, легкие и гастроинтестинальный тракт. Изменение содержания эозинофилов может наблюдаться под действием медиаторов и гормонов: например, при стресс-реакции отмечается падение числа эозинофилов в крови, обусловленное увеличением содержания гормонов надпочечников.
Базофилы (базофильные лейкоциты, или базофилы).
Количество базофилов в крови составляет 0-0,06 109/л, или 0-1 % от общего числа лейкоцитов. Их диаметр в мазке крови равен 11-12 мкм, в капле свежей крови - около 9 мкм (рис.5). Ядра базофилов сегментированы, содержат 2-3 дольки; в цитоплазме выявляются все виды органелл - эндоплазматическая сеть, рибосомы, аппарат Гольджи, митохондрии, актиновые филаменты. Характерно наличие специфических крупных метахроматических гранул, часто закрывающих ядро, размеры которых варьируют от 0,5 до 1,2 мкм.

Рис.5. Базофильный гранулоцит.
Базофилы опосредуют воспаление и секретируют эозинофильный хемотаксический фактор. Гранулы содержат протеогликаны, ГАГ (в том числе гепарин), вазоактивный гистамин, нейтральные протеазы и другие энзимы. Как и нейтрофилы, базофилы образуют биологически активные метаболиты арахидоновой кислоты - лейкотриены, простагландины. Часть гранул представляет собой модифицированные лизосомы. Дегрануляция базофилов происходит в реакциях гиперчувствительности немедленного типа (например, при астме, анафилаксии, сыпи, которая может ассоциироваться с покраснением кожи). Пусковым механизмом анафилактической дегрануляции является IgE-рецептор для иммуноглобулина Е. Метахромазия обусловлена наличием гепарина - кислого гликозаминогликана. Базофилы образуются в костном мозге. Они так же, как и нейтрофилы, находятся в крови около 1-2 суток. При электронно-микроскопическом исследовании видны окружающая гранулы мембрана и кристаллическая область. Гранулы неоднородны по электронной плотности. Помимо специфических гранул, в базофилах содержатся и азурофильные гранулы (лизосомы). Базофилы так же, как и тучные клетки соединительной ткани, выделяя гепарин и гистамин, участвуют в регуляции процессов свертывания крови и проницаемости сосудов. Базофилы участвуют в иммунологических реакциях организма, в частности в реакциях аллергического характера.
2.2.2 Агранулярные лейкоцитыК этой группе лейкоцитов относятся лимфоциты и моноциты. В отличие от гранулоцитов они не содержат в цитоплазме специфической зернистости, а их ядра не сегментированы.
Т-, В, О - и NK-лимфоциты (lymphocytus). В крови взрослых людей они составляют 20-35% от общего числа лейкоцитов A,0-4,0109/л). Величина лимфоцитов в мазке крови значительно варьирует - от 4,5 до 10 мкм. Среди них различают малые лимфоциты (диаметром 4,5-6 мкм), средние (диаметром 7-10 мкм) и большие (диаметром 10 мкм и более). Большие лимфоциты встречаются в крови новорожденных и детей, у взрослых они отсутствуют. Для всех видов лимфоцитов характерно наличие интенсивно окрашенного ядра округлой или бобовидной формы, содержащего компактный гетерохроматин, и относительно узкого ободка базофильной цитоплазмы. В цитоплазме некоторых лимфоцитов содержится небольшое количество азурофильных гранул (лизосомы). Малые лимфоциты составляют большую часть (85-90 %) всех лимфоцитов крови человека. При электронной микроскопии в их ядрах выявляются небольшие впячивания; гетерохроматин расположен преимущественно по периферии ядра. В цитоплазме обнаруживаются везикулы, лизосомы, свободные рибосомы, полисомы, митохондрии, аппарат Гольджи, центриоли, небольшое количество элементов гранулярной эндоплазматической сети (рис.6).
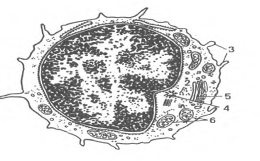
Рис.6. Ультрамикроскопическое строение лимфоцита (схема по Н.А. Юриной, Л.С. Румянцевой). I - ядро; 2 - рибосомы; 3 - микроворсинки; 4 - центриоль; 5 - аппарат Гольджи; 6 - митохондрии.
Среди малых лимфоцитов различают светлые и темные. Малые темные лимфоциты меньше светлых, имеют более плотное ядро, более узкий ободок базофильной цитоплазмы, обладающей высокой электронной плотностью. В цитоплазме расположено большое количество рибосом. Средние лимфоциты составляют около 10-12 % лимфоцитов крови человека. Ядра этих клеток округлые, иногда бобовидные с пальцевидным впячиванием ядерной оболочки. Хроматин более рыхлый, ядрышко хорошо выражено. В цитоплазме расположены удлиненные канальцы гранулярной эндоплазматической сети, элементы агранулярной сети, свободные рибосомы и полисомы, лизосомы. Центросома и аппарат Гольджи расположены рядом с областью инвагинации кариолеммы.
Кроме типичных лимфоцитов, в крови человека в небольшом количестве могут встречаться лимфоплазмоциты (около 1-2 %), которые отличаются концентрическим расположением вокруг ядра канальцев гранулярной эндоплазматической сети.
Основной функцией лимфоцитов является участие в иммунных реакциях. Однако популяция лимфоцитов гетерогенна по характеристике поверхностных рецепторов и роли в реакциях иммунитета.
Среди лимфоцитов различают три основных функциональных класса: В - лимфоциты, Т-лимфоциты и нулевые лимфоциты.
В-лимфоциты впервые были обнаружены в фабрициевой сумке птиц (bursa Fabricius), поэтому и получили соответствующее название. Они образуются у эмбриона человека из стволовых клеток - в печени и костном мозге, а у взрослого - в костном мозге. В-лимфоциты составляют около 30 % циркулирующих лимфоцитов. Их главная функция - участие в выработке антител, т.е. обеспечение гуморального иммунитета. Плазмолемма В - лимфоцитов содержит множество иммуноглобулиновых рецепторов. При действии антигенов В-лимфоциты способны к пролиферации и дифференцировке в плазмоциты - клетки, способные синтезировать и секретировать защитные белки - иммуноглобулины (Ig), которые поступают в кровь, обеспечивая гуморальный иммунитет.
Т-лимфоциты, или тимусзависимые лимфоциты, образуются из стволовых клеток костного мозга, а созревают в тимусе (вилочковая железа), что и обусловило их название. Они преобладают в популяции лимфоцитов, составляя около 70 % циркулирующих лимфоцитов. Для Т-клеток, в отличие от В-лимфоцитов, характерен низкий уровень поверхностных иммуноглобулиновых рецепторов в плазмолемме. Но Т-клетки имеют специфические рецепторы, способные распознавать и связывать антигены, участвовать в иммунных реакциях. Основными функциями Т-лимфоцитов являются обеспечение реакций клеточного иммунитета и регуляция гуморального иммунитета (стимуляция или подавление дифференцировки В-лимфоцитов). Т-лимфоциты способны к выработке лимфокинов, которые регулируют деятельность В-лимфоцитов и других клеток в иммунных реакциях. Среди Т-лимфоцитов выявлено несколько функциональных групп: Т-хелперы, Т-супрессоры, Т-киллеры.
Т-хелперы (от англ. helper - помощник) - их главной функцией является усиление адаптивного иммунного ответа (рис.7). Активируют Т-киллеры, В-лимфоциты, моноциты, NK-клетки, презентируя им фрагменты чужеродного антигена при прямом контакте, а также гуморально, выделяя цитокины. Основным фенотипическим признаком Т-хелперов служит наличие на поверхности клетки молекулы CD4. Т-хелперы распознают антигены при взаимодействии их Т-клеточного рецептора (TCR) с антигеном, связанным с молекулами главного комплекса гистосовместимости 2 класса (MHC-II). Выделяют несколько подтипов Т-хелперов:
Т-хелперы 0 (Th0) - "наивные" недифференцированные Т-хелперы; Т-хелперы 1 (Th1) - преимущественно способствуют развитию клеточного иммунного ответа, активируя Т-киллеры; основной выделяемый цитокин - интерферон-гамма;
Т-хелперы 2 (Th2) - активируют В-лимфоциты, способствуя развитию гуморального иммунного ответа; продуцируют интерлейкины 4, 5 и 13;
Т-хелперы 3 (Т-reg, Т-регуляторы, Т-супрессоры) - экспрессируют на поверхности молекулы CD25 и Foxp3, секретируют интерлейкин-10 и трансформирующий фактор роста-beta (TGF-beta) и супрессируют иммунный ответ:
Т-хелперы 17 (Th17) - подтип Т-хелперов, который характеризуется продуцирует в больших количествах провоспалительный цитокин - IL-17. Показана роль Th17-клеток в развитии аутоиммуной патологии.
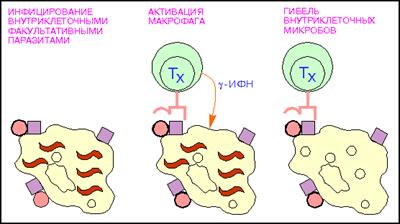
Рис.7: Активация макрофагов Т - хелпетами (кружки - поверхностный микробный антиген; красные квадраты - молекулы MHC класса II, волнистые линии - внутриклеточные паразиты.).
Регуляторные Т-лимфоциты, Т-супрессоры (англ. regulatory T cells, suppressor T cells, Treg) - центральные регуляторы иммунного ответа. Основная их функция - контролировать силу и продолжительность иммунного ответа через регуляцию функции Т-эффекторных клеткок (Т-хелперов и Т-цитотоксических клеток).
Эти клетки экспрессируют FOXP3 - транскрипционный фактор, регулирующий транскрипцию генов, ответственных за дифференцировку Т-клеток и экспрессию цитокинов и других факторов, участвующих в супрессии иммунного ответа. Часто эти клетки так и обозначают, как FOXP3+ регуляторные Т-клетки (FOXP3+ Treg cells). Кроме того, важным маркером Т-регуляторных клеток является экспрессия на их поверхности рецептора к цитокину IL-2 - CD25, соответственно это обозначают как CD25+ клетки. Помимо этих основных маркёров Treg клетки на своей мембране экспрессируют CD62L, различные изоформы мембрано-связанной фосфатазы CD45. Различают несколько разных типов регуляторных Т-клеток: естественные Т-регуляторные клетки (T-reg1) и индуцибельные Т-регуляторные клетки (iT-reg). Индуцибельные Т-регуляторные клетки образуются под влиянием различных факторов на периферии, например, в региональных лимфатических узлах.
Для супрессии иммуного ответа Тreg клетки выделяют цитокины: TGF-beta, IL-10, IFNgamma, IL-35, а также экспрессируют на своей поверхности рецептор CTLA-4. Существуют несколько механизмов супрессии: прямой, при непосредственном контакте между клетками, и дистантный, осуществляющийся на расстоянии - например, через растворимые цитокины. Мишенями действия Тreg клеток являются как Т-эффекторные клетки, так и дендритные клетки, ответственные за презентацию антигена и активацию Т-клеток. При дистантном механизме цитокины, выделяемые Тreg клетками, например, трансформирующий ростовой фактор бета (TGF-beta), связываются со своими рецепторами на поверхности Т-эффекторных клеток и ингибирует их активацию, тем самым супрессируя иммунный ответ. Важным механизмом также служит захват IL-2 при помощи CD25 - рецептора к IL-2 и секвестрация рецептора у эффекторных Т-клеток, что препятствует активации после связывания комплекса MHC с антигеном, так как известно, что IL-2 является основным аутокринным стимулирующим фактором, поддерживающим диффернцировку и клональную экспансию Т-клеток.
Тreg клетки, взаимодействуя с рецептором CD86 на дендритных клетках при помощи CTLA-4, способны ингибировать функцию активации дендритными клетками Т-клеток.
При прямом механизме супрессии Treg взаимодействуют с эффекторными Т-клетками и гранзим B действует через перфорины, образующие канал, вызывая апоптоз в этих клетках, тем самым элиминируя активные Т-клетки.
Цитотоксические Т-лимфоциты непосредственно контактируют с чужеродными клетками и разрушают их. Клеточный иммунитет опосредован цитотоксическими Т-лимфоцитами и Т-хелперами. Многие микроорганизмы живут внутри клеток в недосягаемости для гуморальных антител. Чтобы справиться с внутриклеточными паразитами, возникла обособленная система приобретенного имунитета, основанная на функционировании отдельной субпопуляции лимфоцитов, а именно, цитотоксических T-лимфоцитов (T-киллеров). Эти клетки отличаются очень широкой специфичностью. Поскольку T-лимфоциты должны взаимодействовать с содержащими паразитов клетками, они могут узнать антиген только в том случае, если он экспрессирован на поверхности инфицированной клетки. Как и B-лимфоциты, каждая T-клетка имеет специфический рецептор, который распознает этот антиген. (Рецептор T-лимфоцита структурно отличается от молекулы мембраного иммуноглобулина - рецептора B-лимфоцитов). При этом T-лимфоциты узнают антиген на поверхности клетки в комплексе с клеточным маркером: молекулами MHC класса I. В процессе распознавания поверхностного антигена цитотоксический T-лимфоцит вступает в теснейший контакт со своей мишенью и уничтожает ее до начала репликации. Кроме того, он продуцирует гамма-интерферон, который ограничивает проникновение вируса в соседние клетки, особенно в тех случаях, когда вирус является слабым индуктором альфа-интерферона и бета-интерферона Цитотоксические T-лимфоциты относятся к субпопуляции T8 (или Ly2) и представляют популяцию T-эффекторов и играют важнейшую роль в уничтожении клеток, зараженных вирусами, бактериями, а возможно, участвуют и в предполагаемом надзоре за появлением опухолевых клеток.
Большинство цитотоксических T-клеток (Tц) относится к субпопуляции CD8+ и распознает антиген, презентированный в ассоциации с молекулами MHC класса I, но меньшая их часть (примерно 10%), относящаяся к субпопуляции CD4+, способна распознавать антиген в ассоциации с молекулами MHC класса II.
Для активации и поражения мишени Tц обладают несколькими механизмами воздействия. Один из них - это передача сигналов при непосредственном клеточном контакте через поверхностные структуры, другой - непрямая сигнализация с помощью цитокинов. Кроме того в цитоплазме многих цитотоксических клеток обнаружены гранулы с белками, высвобождение которых вблизи цитоплазматической мембраны клетки-мишени вызывает ее повреждение.
Цитотоксические T-лимфоциты развиваются из предшественников. Предшественники цитотоксических клеток активируются комплексом антигена и молекул MHC класса I, размножаются и созревают под действием IL-2, а также еще плохо идентифицированных факторов дифференцировки, продуцируемых T-хелперами.
Нулевые лимфоциты не имеют поверхностных маркеров на плазмолемме, характерных для В - и Т-лимфоцитов. Их расценивают как резервную популяцию недифференцированных лимфоцитов.
В настоящее время оценка иммунного статуса организма в клинике проводится с помощью иммунологических и иммуноморфологических методов выявления различных видов лимфоцитов.
Продолжительность жизни лимфоцитов варьирует от нескольких недель до нескольких лет. Т-лимфоциты являются "долгоживущими" (месяцы и годы) клетками, а В-лимфоциты относятся к "короткоживущим" (недели и месяцы). Для Т-лимфоцитов характерно явление рециркуляции, т.е. выход из крови в ткани и возвращение по лимфатическим путям снова в кровь. Таким образом они осуществляют иммунологический надзор за состоянием всех органов, быстро реагируя на внедрение чужеродных агентов. Среди клеток, имеющих морфологию малых лимфоцитов, следует назвать циркулирующие стволовые клетки крови (СКК), которые поступают в кровь из костного мозга. Впервые эти клетки были описаны А.А. Максимовым и обозначены им как "подвижный мезенхимный резерв". Из СКК, поступающих в кроветворные органы, дифференцируются различные клетки крови, а из СКК, поступающих в соединительную ткань, - тучные клетки, фибробласты и др.
Моноциты. Система мононуклеарных фагоцитов (СМФ).
В капле свежей крови эти клетки лишь немного крупнее других лейкоцитов (9-12 мкм), в мазке крови они сильно распластываются по стеклу и размер их достигает 18-20 мкм. В крови человека количество моноцитов колеблется в пределах 6-8 % от общего числа лейкоцитов.
Ядра моноцитов разнообразной и изменчивой конфигурации: встречаются бобовидные, подковообразные, редко - дольчатые ядра с многочисленными выступами и углублениями. Гетерохроматин рассеян мелкими зернами по всему ядру, но обычно в больших количествах он располагается под ядерной мембраной. В ядре моноцита содержится одно или несколько маленьких ядрышек (рис.8).
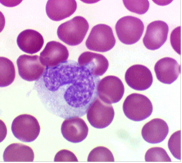
Рис.8. Моноцит.
Цитоплазма моноцитов менее базофильна, чем цитоплазма лимфоцитов. При окраске по методу Романовского - Гимзы она имеет бледно-голубой цвет, но по периферии окрашивается несколько темнее, чем около ядра; в ней содержится различное количество очень мелких азурофильных зерен (лизосом). Характерны наличие пальцеобразных выростов цитоплазмы и образование фагоцитарных вакуолей. В цитоплазме расположено множество пиноцитозных везикул. Имеются короткие канальцы гранулярной эндоплазматической сети, а также небольшие по размеру митохондрии. Моноциты относятся к макрофагической системе организма, или к так называемой мононуклеарной фагоцитарной системе (МФС). Клетки этой системы характеризуются происхождением из промоноцитов костного мозга, способностью прикрепляться к поверхности стекла, активностью пиноцитоза и иммунного фагоцитоза, наличием на мембране рецепторов для иммуноглобулинов и комплемента. Моноциты циркулирующей крови представляют собой подвижный пул относительно незрелых клеток, находящихся на пути из костного мозга в ткани. Время пребывания моноцитов в крови варьирует от 36 до 104 ч. Моноциты, выселяющиеся в ткани, превращаются в макрофаги, при этом у них появляются большое количество лизосом, фагосом, фаголизосом.
Из крови в ткани за 1 ч уходит 7,0-106 моноцитов. В тканях моноциты дифференцируются в органо - и тканеспецифичные макрофаги. Внесосудистый пул моноцитов в 25 раз превышает циркулирующий.
Система мононуклеарных фагоцитов является центральной, объединяющей различные типы клеток, участвующих в защитных реакциях организма. Макрофагам принадлежит важнейшая роль в процессах фагоцитоза. Они удаляют из организма отмирающие клетки, остатки разрушенных клеток, денатурированный белок, бактерии и комплексы антиген-антитело. Макрофаги участвуют в регуляции кроветворения, иммунном ответе, гемостазе, метаболизме липидов и железа. Содержание моноцитов в крови в норме отражено в табл.2.
Таблица 3.
Содержание лимфоцитов (абсолютное и относительное - процентное количество) в крови в норме
| Возраст | Предел колебаний, 10 /л | Моноциты, % |
| 12мес | 0,05-1,1 | 2-7 |
| 4 года | 0-0,8 | 2-7 |
| 10 лет | 0-0,8 | 1-6 |
| 21 год | 0-0,8 | 1-8 |
| Взрослые | а-0,8 | 1-8 |
Моноцитоз - увеличение числа моноцитов в крови (>0,8109/л) - сопровождает целый ряд заболеваний (табл.1.28). При туберкулезе появление моноцитоза считается доказательством активного распространения туберкулезного процесса. При этом важным показателем является отношение абсолютного числа моноцитов к лимфоцитам, которое в норме составляет 0,3-1,0. Это отношение бывает более 1,0 в активную фазу заболевания и снижается при выздоровлении, что позволяет оценить течение туберкулеза.
При септических эндокардитах, вялотекущем сепсисе возможен значительный моноцитоз, который нередко встречается в отсутствие лейкоцитоза. Относительный или абсолютный моноцитоз отмечается у 50 % больных с системными васкулитами.
Кратковременный моноцитоз может развиться у больных с острыми инфекциями в период реконвалесценции. Моноцитопения - уменьшение числа моноцитов (< 0,09109/л). При гипоплазии кроветворения количество моноцитов в крови снижено.
2.3 Постклеточные структуры 2.3.1 ЭритроцитыЭритроциты, или красные кровяные тельца, человека и млекопитающих представляют собой безъядерные клетки, утратившие в процессе фило - и онтогенеза ядро и большинство органелл. Эритроциты являются высокодифференцированными постклеточными структурами, неспособными к делению.
Функции эритроцитов осуществляются в сосудистом русле, которое они в норме никогда не покидают:
1) дыхательная - транспортировка кислорода и углекислоты. Эта функция обеспечивается благодаря тому, что эритроциты заполнены железосодержащим кислород - связывающим пигментом - гемоглобином (составляет 33% их массы), который определяет их цвет (желтоватый у отдельных элементов и красный у их массы)
2) Регуляторные и защитные функции обеспечиваются благодаря способности эритроцитов переносить на своей поверхности ряд биологически активных веществ, в том числе иммуноглобулины, компоненты комплемента, иммунные комплексы.
3). Кроме того, эритроциты участвуют в транспорте аминокислот, антител, токсинов и ряда лекарственных веществ, адсорбируя их на поверхности плазмолеммы.
Форма и строение. Популяция эритроцитов неоднородна по форме и размерам (рис.9). В нормальной крови человека основную массу (80-90 %) составляют эритроциты двояковогнутой формы - дискоциты. Кроме того, имеются планоциты (с плоской поверхностью) и стареющие формы эритроцитов - шиловидные эритроциты, или эхиноциты (~ 6 %), куполообразные, или стоматоциты (~ 1-3 %), и шаровидные, или сфероциты (~ 1 %)
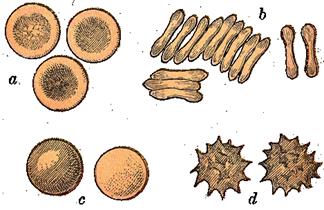
Рис.9. Формы эритроцитов.
Средняя продолжительность жизни эритроцитов составляет около 120 дней. В организме ежедневно разрушается около 200 млн эритроцитов. Процесс старения эритроцитов идет двумя путями - кренированием (образование зубцов на плазмолемме) или путем инвагинации участков плазмолеммы. При кренировании образуются эхиноциты с различной степенью формирования выростов плазмолеммы, впоследствии отпадающих, при этом формируется эритроцит в виде микросфероцита. При инвагинации плазмолеммы эритроцита образуются стоматоциты, конечной стадией которых также является микросфероцип. Одним из проявлений процессов старения эритроцитов является их гемолиз, сопровождающийся выхождением гемоглобина; при этом в крови обнаруживаются "тени" (оболочки) эритроцитов. Обязательной составной частью популяции эритроцитов являются их молодые формы A - 5 %, называемые ретикулоцитами, или полихроматофильными эритроцитами. В них сохраняются рибосомы и эндоплазматическая сеть, формирующие зернистые и сетчатые структуры (substantia granulofilamentosa), которые выявляются при специальной суправитальной окраске. При обычной гематологической окраске азур П-эозином они в отличие от основной массы эритроцитов, окрашивающихся в оранжево-розовый цвет (оксифилия), проявляют полихроматофилию и окрашиваются в серо-голубой цвет.
При заболеваниях могут появляться аномальные формы эритроцитов, что чаще всего обусловлено изменением структуры гемоглобина (Но). Замена даже одной аминокислоты в молекуле НЬ может быть причиной изменения формы эритроцитов. В качестве примера можно привести появление эритроцитов серповидной формы при серповидно-клеточной анемии, когда у больного имеет место генетическое повреждение в р-цепи гемоглобина. Процесс нарушения формы эритроцитов при заболеваниях получил название пойкилоцитоз.
кровь клетка эритроцит тромбоцит
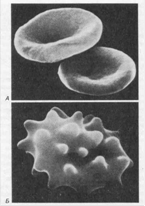
Рис.10.
А. Нормальные эритроциты в форме двояковогнутого диска.
Б. Сморщенные эритроциты в гипертоническом солевом растворе
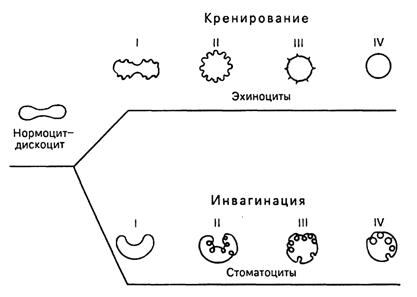
Рис.11. Изменение формы эритроцитов в процессе старения (схема). I, II, III, IV - стадии развития эхиноцитов и стоматоцитов (по Т. Фуджии).
Размеры эритроцитов в нормальной крови также варьируют. Большинство эритроцитов (~ 75 %) имеют диаметр около 7,5 мкм и называются нормоцитами. Остальная часть эритроцитов представлена микроцитами (~ 12,5 %) и макроцитами ( - 12,5 %). Микроциты имеют диаметр <7,5 мкм, а макроциты >7,5 мкм. Изменение размеров эритроцитов встречается при заболеваниях крови и называется анизоцитозом.
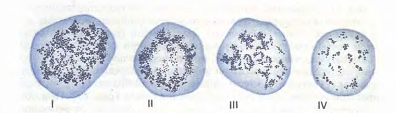
Рис.12. Ретикулоциты (по Г.А. Алексееву и И.А. Кассирскому). Зернисто-сетчатая субстанция имеет вид клубка (I), отдельных нитей, в виде розетки (II, III), зернышек (IV).
Большинство липидных молекул, содержащих холин (фосфатидилхолин, сфингомиелин), расположены во внешнем слое плазмолеммы, а липиды, несущие на конце аминогруппу (фосфатидилсерин, фосфатидилэтаноламин), лежат во внутреннем слое. Часть липидов (~ 5 %) наружного слоя соединены с молекулами олигосахаров и называются гликолипидами. Распространены мембранные гликопротеины - гликофорины. С ними связывают антигенные различия между группами крови человека.
В плазмолемме эритроцита идентифицировано 15 главных белков с молекулярной массой 15-250 КД. Более 60 % всех белков составляют примембранный белок спектрин, мембранные белки - гликофорин и полоса спектрин составляет 25 % массы всех мембранных и примембранных белков эритроцита, является белком цитоскелета, связанным с цитоплазматической стороной плазмолеммы, участвует в поддержании двояковогнутой формы эритроцита Молекула спектрина имеет вид палочки длиной 100 нм, состоящей из 2 полипептидных цепей: а-спектрина B40 КД) и р-спектрина B20 КД). Концы сформированных из них тетрамеров связаны с короткими актиновыми филаментами цитоплазмы и белком полосы 4.1, образуя "узловой комплекс" (рис.13).
Цитоскелетный белок полосы 4.1, связывающий спектрин и актин, одновременно соединяется с белком гликофорином. На внутренней цитоплазматической поверхности плазмолеммы образуется гибкая сетевидная структура, которая поддерживает форму эритроцита и противостоит давлению при прохождении его через тонкий капилляр (см. рис.14).
Доказано, что при наследственной аномалии спектрина эритроциты имеют сферическую форму. При недостаточности спектрина в условиях анемии эритроциты также принимают сферическую форму. Соединение спектринового цитоскелета с плазмолеммой обеспечивает внутриклеточный белок анкирин. Анкирин связывает спектрин с трансмембранным белком плазмолеммы (полоса 3). Гликофорин - трансмембранный белок C0 КД), который пронизывает плазмолемму в виде одиночной спирали, и его большая часть выступает на наружной поверхности эритроцита, где к нему присоединены 15 отдельных цепей олигосахаридов, которые в сумме составляют 60 % массы гликофорина и несут отрицательные заряды.
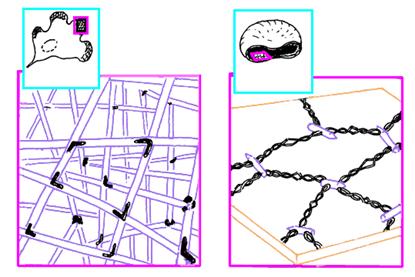
Рис.13. Цитоскелет фибробласта и эритроцит
Гликофорины относятся к классу мембранных гликопротеинов, которые выполняют рецепторные функции. Гликофорины обнаружены только в эритроцитах. Полоса 3 представляет собой-трансмембранный гликопротеид A00 КД), полипептидная цепь которого много раз пересекает бислой липидов. Этот гликопротеид участвует в обмене О2 и СО2, которые связывают гемоглобин - основной белок цитоплазмы эритроцита. Эритроциты в легких отдают СО2 путем замены анионов НСО" на СГ. Белок полосы 3 обеспечивает этим анионам трансмембранный проход через гидрофильные "поры", окруженные гидрофобными липидными зонами. Таким образом формируются водные ионные каналы.
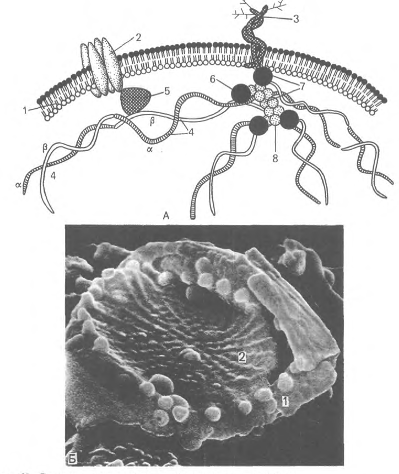
Рис.14. Строение плазмолеммы и цитоскелета эритроцита. А - схема: 1 - плазмолемма; 2 - белок полосы 3; 3 - гликофорин; 4 - сттектрин {а - и р - цепи); 5 - анкирин; 6 - белок полосы 4.1; 7 - узловой комплекс; 8 - актин; Б - плазмолемма и цитоскелет эритроцита в сканирующем электронном микроскопе. - плазмолемма: 2 - сеть спектрина.
Олигосахариды гликолипидов и гликопротеидов образуют гликокаликс. Они определяют антигенный состав эритроцитов, т.е. наличие в них агглютиногенов. На поверхности эритроцитов выявлены агглютиногены А и В, в состав которых входят полисахариды, содержащие амнносахара и глюкуроновую кислоту. Они обеспечивают агглютинацию (склеивание) эритроцитов под влиянием соответствующих белков плазмы крови - а - и р-агглютининов, находящихся в составе фракции у-глобулинов.
По содержанию агглютиногенов и агглютининов различают 4 группы крови: в крови А (0) группы отсутствуют агглютиногсны А и В, но имеются а - и р-агтлютинины; в крови А (П) группы имеются агглютиноген А и р-агглютинин; в крови В (Ш) группы содержатся В-агглютиноген и а-агглютинин; в крови AB (IV) группы имеются агглютиногены А и В и нет агглютининов. При переливании крови для предотвращения гемолиза (разрушение эритроцитов) нельзя допускать вливания реципиентам эритроцитов с агглютиногенами А или В, имеющим а - или р-агглютинины. Поэтому лица с (0) A группой крови являются универсальными донорами, т.е. их кровь может быть перелита всем людям с другими группами крови.
Соответственно лица с AB (FV) группой крови являются универсальными реципиентами, т.е. им можно перелить любую группу крови.
На поверхности эритроцитов имеется также резус-фактор (Rh-фактор) - агглютиноген. Он присутствует у 86 % людей; у 14 % отсутствует (резус-отрицательные). Переливание резус-положительной крови резус-отрицательному пациенту вызывает образование резус-антител и гемолиз эритроцитов. Агглютинация эритроцитов свойственна нормальной свежей крови, при этом образуются так называемые "монетные столбики".
Это явление связано с потерей заряда плаэмолеммы эритроцитов. Скорость оседания (агглютинации) эритроцитов (СОЭ) в 1 ч у здорового человека составляет 4-8 мм у мужчин и 7-10 мм у женщин. СОЭ может значительно изменяться при заболеваниях, например при воспалительных процессах, и поэтому служит важным диагностическим признаком. В движущейся крови эритроциты отталкиваются из-за наличия на их плазмолемме одноименных отрицательных зарядов. Поверхность плазмолеммы одного эритроцита составляет около 130 мкм2 крови. При окрашивании мазка крови азур И-эозином по Романовскому - Гимзе большинство эритроцитов приобретают оранжево-розовый цвет (оксифильны), что обусловлено высоким содержанием в них гемоглобина.
В небольшой части эритроцитов A-5 %), являющихся более молодыми формами, сохраняются остатки органелл (рибосомы, гранулярный, эндоплазматический ретикулум), которые проявляют базофилию. Такие эритроциты окрашиваются как кислыми красителями (эозин), так и основными (азур II) и называются полихроматофилъными. При специальной суправитальной окраске (бриллиант-крезилфиолетовым) в них выявляются зернисто-нитчатые структуры, поэтому их называют ретикулоцитами. Эритроциты различаются по степени насыщенности гемоглобином.
Среди них выделяются нормохромные, гипохромные и гиперхромные, соотношение между которыми значительно изменяется при заболеваниях. Количество гемоглобина в одном эритроците называют цветным показателем. Электронно-микроскопически гемоглобин выявляется в гиалоплазме эритроцита в виде многочисленных плотных гранул диаметром 4-5 нм.
Гемоглобин - это сложный белок F8 КД, состоящий из 4 полипептидных цепей глобина и гема (железосодержащий порфирин), обладающий высокой способностью связывать кислород. В норме у человека содержится два типа гемоглобина - НЬА и HbF. Эти гемоглобины различаются составом аминокислот в глобиновой (белковой) части.
У взрослых людей в эритроцитах преобладает НЬА, (от англ. adult - взрослый), составляя 98 %. Он содержит две а-глобиновые цепи и две C-глобиновые цепи, включающие 574 аминокислоты.
HbF, или фетальный гемоглобин (от англ. foetus - плод), составляет у взрослых около 2 % и преобладает у плодов. К моменту рождения ребенка HbF составляет около 80 %, а НЬА только 20 %. Эти гемоглобины отличаются составом аминокислот в глобиновой (белковой) части.
Железо (Fe2+) в геме может присоединять О2 в легких (в таких случаях образуется оксигемоглобин - НЬО2) и отдавать его в тканях путем диссоциации НЬО, на кислород (О2) и НЬ; валентность Fe2+ не изменяется.
При ряде заболеваний (гемоглобинозы, гемоглобинопатии) в эритроцитах появляются другие виды гемоглобинов, которые характеризуются изменением аминокислотного состава в белковой части гемоглобина.
В настоящее время выявлено более 150 видов аномальных гемоглобинов. Например, при серповидно-клеточной анемии имеет место генетически обусловленное повреждение в C-цепи гемоглобина - глютаминовая кислота, занимающая 6-е положение в полипептидной цепи, заменена на аминокислоту валин. Такой гемоглобин обозначается как HbS (от англ. sickle - серп), так как в условиях понижения парциального давления О2 он превращается в тектоидное тело, придавая эритроциту форму серпа. В ряде стран тропического пояса определенный контингент людей являются гетерозиготными для серповидных генов, а дети двух гетерозиготных родителей по законам наследственности дают либо нормальный тип B (5%), либо бывают гетерозиготными носителями, и 25 % страдают серповидноклеточной анемией.
Гемоглобин способен связывать О2 в легких, при этом образуется оксигемоглобин, который транспортируется ко всем органам и тканям и там отдает О2. В тканях выделяемая СО поступает в эритроциты и соединяется с НЬ, образуя карбоксигемоглобин. При разрушении эритроцитов (старых или при воздействии различных факторов - токсины, радиация и др.) гемоглобин выходит из клеток, и это явление называется гемолизом. Старые эритроциты разрушаются макрофагами главным образом в селезенке, а также в печени и костном мозге, при этом НЬ распадается, а высвобождающееся из железосодержащего гема железо используется для образования новых эритроцитов.
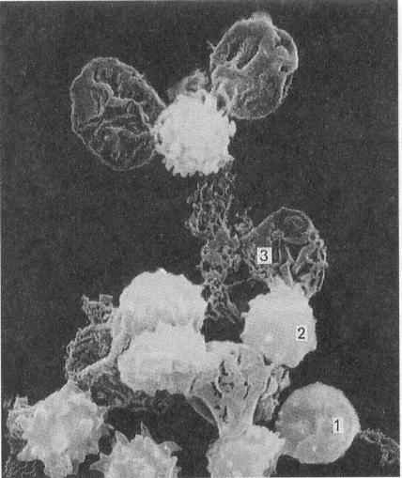
Рис 15. Электронная микрофотография гемолиза эритроцитов и образование их “теней”
В макрофагах НЬ распадается на пигмент билирубин и гемосидерин - аморфные агрегаты, содержащие железо. Железо гемосидерина связывается с трансферрином - негеминовым белком плазмы, содержащим железо, и захватывается специальными макрофагами костного мозга. В процессе образования эритроцитов (эритропоэз) эти макрофаги передают трансферрин в формирующиеся эритроциты, что послужило основанием назвать их клетками-кормилками.
В цитоплазме эритроцитов содержатся ферменты анаэробного гликолиза, с помощью которых синтезируются АТФ и НАДН, обеспечивающие энергией главные процессы, связанные с переносом О2 и СО2, а также поддержание осмотического давления и перенос ионов через плазмолемму эритроцита. Энергия гликолиза обеспечивает активный транспорт катионов через плазмолемму, поддержание оптимального соотношения концентрации К+ и Na+ в эритроцитах и плазме крови, сохранении формы и целостности мембраны эритроцита. НАДН участвует в метаболизме НЬ, предотвращая окисление его в метгемоглобин.
Эритроциты участвуют в транспорте аминокислот и полипептидов, регулируют их концентрацию в плазме крови, т.е. выполняют роль буферной системы. Постоянство концентрации аминокислот и полипептидов в плазме крови поддерживается с помощью эритроцитов, которые адсорбируют их избыток из плазмы, а затем отдают различным тканям и органам. Таким образом, эритроциты являются подвижным депо аминокислот и полипептидов.
Сорбционная способность эритроцитов связана с состоянием газового режима (парциальное давление О2 и СО2 - Ро, Рсо): в частности, при действии О2 наблюдаются выход аминокислот из эритроцитов и увеличение их содержания в плазме.
2.3.2 Тромбоциты\кровяные пластинкиМелкие дисковидные двояковыпуклые безъядерные постклеточные структуры диаметром 2-4 мкм, циркулирующие в крови. Они образуются в красном костном мозге в результате фрагментации участков цитоплазмы мегакариоцитов (гигантских клеток костного мозга), поступают в кровь, в которой находятся в течение 5-10 дней, после чего фагоцитируются макрофагами, преимущественно в селезенке и легком. Часть тромбоцитов разрушается за пределами сосудистого русла, куда они попадают при повреждении стенки сосудов. Общее количество тромбоцитов в крови взрослого человека 0,8-2,4 *1012; из этого числа около 15 % обновляются ежедневно. В норме в крови циркулирует 2/3 общего числа тромбоцитов, а 1/3 находится вне циркуляции в красной пульпе селезенки. На мазках крови тромбоциты вследствие агрегации обычно выявляются в виде скоплений. Концентрация тромбоцитов в крови равна 200-400 тыс. /мкл (200-400 *109 /л) крови.
Функции тромбоцитов осуществляются как внутри сосудистого русла, так и вне его. К ним относятся:
1) Остановка кровотечения при повреждении стенки сосудов (первичный гомеостаз) - основная функция тромбоцитов;
2) Обеспечение свертывания крови - (гемокоакуляция) - вторичный гомеостаз (совместно с эндотелием кровеносных сосудов и плазмой крови);
3) Участие в реакциях заживления ран (в первую очередь, повреждений сосудистой стенки) и воспаления;
4) Обеспечение нормальной функции сосудов, в частности, их эндотелиальной выстилки (ангиотрофическая функция).
Строение тромбоцитов.
Тромбоцит окружен плазмолеммой и включает
1. светлую прозрачную наружную часть, называемую гиаломером,
2. центральную окрашенную часть, содержащую аэурофильные гранулы - грануломер.
3. В некоторых случаях выявляются небольшие псевдоподии, выступающие из периферической части гиаломера.
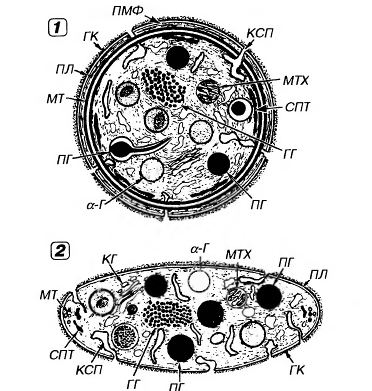
Рис.16. Ультраструктура тромбоцита.1 - сечение в экваториальной плоскости, 2 - поперечный разрез, ПЛ - плазмолемма, ГК - гликокалис, КСП - канальцы, связанные с поверхностью, СПТ - система плотных трубочек, МТ - микротрубочки, ПМФ - подмембранные микрофиламенты, ГГ - гликоген, КГ - комплекс Гольджи, МТХ - митохондрия, α-Г - α-гранулы, ПГ - плотные гранулы.
4. Плазмолемма тромбоцитов покрыта снаружи толстым (от 50 до 150-200 нм) слоем гликокалиса с высоким содержанием гликозаминогликанов и гликопротеинов (см. рисунок 17).
5. Она содержит многочисленные рецепторы, посредующие действие веществ, активирующих и ингибирующих функции тромбоцитов, обуславливающие их прикрепление (адгезию) к эндотелию сосудов и агрегацию (склеивание друг с другом).
6. Наиболее важными из них в функциональном отношении являются рецепторные гликопротеины Ib (GP Ib), IIb (GP IIb), IIIa (GP IIIa), рецепторы к АДФ, адреналину, тромбину, фактору Ха, фактору агрегации тромбоцитов (ФАТ), коллагену.
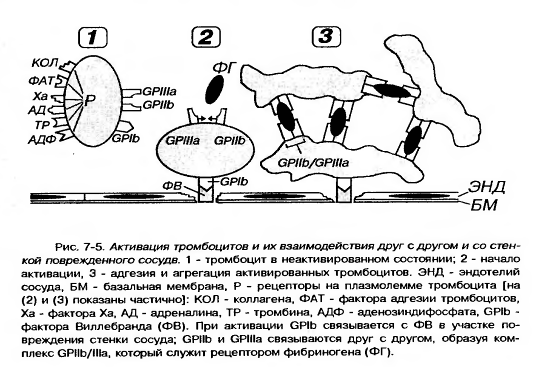
Гиаломер содержит две системы трубочек (канальцев) и большую часть элементов цитоскилета (см. рисунок 17):
1. Система канальцев, связанных с поверхностью (открытая система канальцев), представлена гладкими анастомозирующими трубочками, которые открываются в инвагинации, образованные плазмалеммой. Функция этой системы канальцев, скорее всего, связана с процессами поглощения и выведения веществ, в частности, она облегчает экзоцитоз содержимого гранул тромбоцитов.
2. Система плотных трубочек образуется комплексом Гольджи мегакариоцитов. Она представлена узкими мембранными трубочками заполненными плотным зернистым содержимым, которые располагаются непосредственно под кольцом микротрубочек. Или разбросаны по цитоплазме. Предполагают, что они накапливают и выделяют Са2+, т.е. являются аналогом саркоплазматической сети мышечных клеток. Их связывают так же с выработкой простагландинов.
Цитоскелет тромбоцитов представлен микротрубочками, микрофиламентами и промежуточными филаментами.
Микротрубочки в количестве 4-15 располагаются по перефирии цитоплазмы и формируют мощный пучек (краевое кольцо), служащий жестким каркасом и способствующий поддержанию формы тромбоцитов.
Микрофиламенты, образованные актином, многочисленны (актин составляет 25% белка тромбоцитов), располагаются по всей цитоплазме в виде коротких нитей; в гиаломере они концентрируются между пучком микротрубочек и плазмалеммой и образует подмембранный аппарат. Последний участвует в образовании выпячиваний цитоплазмы при движении и агрегации тромбоцитов. Актиновые филаменты связаны в единую систему посредством белков α - актина, миозина и тропомиозина, а с плазмалеммой - с помощью белка филамина.
Промежуточные филаменты образованы белком виментином и располагаются примущественно под плазмалеммой.
Грануломер содержит митохондрии, частицы гликогена, отдельные рибосомы, единичные короткие цистерны грЭПС, элементы комплекса Гольджи и гранулы нескольких типов.
α - гранулы - самые крупные (диаметр 300-500 нм), с умеренно плотным матриксом, в котором содержаться: фибриноген, фибронектин, тромбоспондин (белок сходный с актомиозином), тромбоглобулин, тромбоцитарный фактор роста (ТРФР), ЭФР, ТФРβ, фактор свертывания V и фактор Виллебанда (белок переносчик фактора VIII свертывания), а так же ряд других белков. Составляют большую часть гранул, окрашивающихся азуром.
δ - гранулы (плотные гранулы или тельца) - немногочисленные (до 5) мембранные пузырьки диаметром 250-300 нм с плотным матриксом, который иногда располагается в них эксцентрично. Матрикс содержит АДФ, АТФ, Са2+, Mg2+, пирофосфат, гистамин, серотонин. Последний не синтезируется тромбоцитами, а поглощается ими из крови.
γ - гранулы мелкие (диаметр 200-250 нм) пузырьки, содержащие гидролитические ферменты. Рассматриваются как лизосомы.
3. Иммунитет
Под иммунитетом понимается невосприимчивость, слабовосприимчивость, сопротивляемость организма инфекциям и инвазиям чужеродных организмов (в том числе - болезнетворных микроорганизмов) и относительная устойчивость к вредным веществам. В более широком смысле это - способность организма противостоять изменению его нормального функционирования под воздействием внешних факторов. Иммунитет - это внутренняя система организма, которая обеспечивает его защиту от вредных воздействий внешней среды. Эта система защищает как основные как внешние его параметры, так и функции жизнедеятельности его органов и тканей.
У большинства живых организмов существуют механизмы неспецифической резистентности, которую также называют врождённым, конституциональным или видовым иммунитетом. У челюстноротых позвоночных появляется качественно новая система приобретённого иммунитета, позволяющая реагировать на конкретный чужеродный биоматериал и запоминать его, существенно усиливая интенсивность ответной реакции на вторжение при повторном контакте с этим же материалом. Различают два типа иммунитета: специфический и неспецифический. Специфический иммунитет носит индивидуальный характер и формируется на протяжении всей жизни человека в результате контакта его иммунной системы с различными микробами и антигенами. Специфический иммунитет сохраняет память о перенесенной инфекции и препятствует ее повторному возникновению. Неспецифический иммунитет носит видоспецифический характер, то есть практически одинаков у всех представителей одного вида. Неспецифический иммунитет обеспечивает борьбу с инфекцией на ранних этапах ее развития, когда специфический иммунитет еще не сформировался. Состояние неспецифического иммунитета определяет предрасположенность человека к различным банальным инфекциям, возбудителями которых являются условно патогенные микробы.
Невосприимчивость организма к инфекционным заболеваниям бывает специфической и неспецифической (неспецифическая резистентность). Специфическая невосприимчивость = иммунитет.
Неспецифическая резистентность бывает обусловлена:
1. Видовой невосприимчивостью (например, невосприимчивость человека к болезням животных);
2. Бактерицидными факторами организма (фагоцитоз и воспаление, лизоцим, показатель pH, лихорадочные реакции)
· Стерильный иммунитет (выздоровление сопровождается полным устранением микробов)
· Нестерильный иммунитет (формируется т. н. носительство).
· Иммуноглобулины типа M (IgM) (выделяются в первое время после контакта с инфекцией, обусловливают первичный иммунный ответ).
· Антитела типа G (IgG) (защищает организм на протяжении длительного времени, участвует во вторичном иммунном ответе, при первичном заражении, пик их концентрации приходится на 2 неделю болезни).
· Иммуноглобулины типа Е (IgE) обусловливают аллергические реакции - гиперчувствительность немедленного типа (ГНТ).
· Иммуноглобулин типа А (защищает организм от проникновения инфекции через кожу и слизистые оболочки, в большом количестве содержится в грудном молоке).
На первом этапе столкновения с чужеродным антигеном запускается неспецифический патологический защитный процесс - воспаление, сопровождающийся фагоцитозом, выделением медиаторов воспаления - гистамина, серотонина, цитокинов и т.п. Фагоциты (макрофаги) поглощают антигены и контактируют с лимфоцитами Т-хелперами, представляя им на поверхности антигенные детерминанты. Т-хелперы запускают размножение (выделяя специфические белковые вещества - интерлейкины) специфических для данного антигена клонов Т-киллеров и В-лимфоцитов из предсуществующих стволовых клеток, которые прошли проверку на толерантность в эмбриональном периоде (клонально-селекционная теория Бернета).
У млекопитающих сформировались два типа иммунитета: клеточные и гуморальный. Это происходит из-за того, что у млекопитающих развивается 2 типа лимфоцитов - Т - и В-клеток. Эти лимфоциты образуются из стволовых клеток-предшественников в костном мозге.
Специфический и неспецифический иммунитет.
Неспецифический (врожденный) иммунитет обуславливает однотипные реакции на любые чужеродные антигены. Главным клеточным компонентом системы неспецифического иммунитета служат фагоциты, основная функция которых - захватывать и переваривать проникающие извне агенты. Для возникновения подобной реакции чужеродный агент должен иметь поверхность, т.е. быть частицей (например, заноза).
Если же вещество молекулярно-дисперсное (например: белок, полисахарид, вирус), и при этом не токсичное и не обладает физиологической активностью - оно не может быть нейтрализовано и выведено организмом по вышеописанной схеме. В этом случае реакцию обеспечивает специфический иммунитет. Он приобретается в результате контакта организма с антигеном; имеет приспособительное значение и характеризуется формированием иммунологической памяти. Его клеточными носителями служат лимфоциты, а растворимыми - иммуноглобулины (антитела).
Первичный и вторичный иммунный ответ.
Специфические антитела продуцируются специальными клетками - лимфоцитами. Причем для каждого вида антител существует свой тип лимфоцитов (клон).
Первое взаимодействие антигена (бактерии или вируса) с лимфоцитом вызывает реакцию, названную первичным иммунным ответом, в ходе которого лимфоциты начинают развиваться (пролиферировать) в виде клонов, претерпевая затем дифференцировку: некоторые из них становятся клетками памяти, другие превращаются в зрелые клетки, продуцирующие антитела. Главные особенности первичного иммунного ответа - существование латентного периода до появления антител, затем выработка их лишь в небольшом количестве.
Вторичный иммунный ответ развивается при последующем контакте с тем же самым антигеном. Основная особенность - быстрая пролиферация лимфоцитов с дифференцировкой их в зрелые клетки и быстрая выработка большого количества антител, которые высвобождаются в кровь и тканевую жидкость, где могут встретиться с антигеном и эффективно побороть болезнь.
Естественный и искусственный иммунитет.
К факторам естественного иммунитета относят иммунные и неиммунные механизмы. К первым относятся гуморальные (система комплемента, лизоцим и др. белки). Ко вторым относятся барьеры (кожа, слизистая), секрет потовых, сальных, слюнных желез (содержит разнообразные бактерицидные вещества), желез желудка (соляная кислота и протеолитические ферменты), нормальная микрофлора (антагонисты патогенных микроорганизмов).
Искусственный иммунитет вырабатывает при введении в организм вакцины или иммуноглобулина.
Активный и пассивный иммунитет.
Активная иммунизация стимулирует собственный иммунитет человека, вызывая выработку собственных антител. Вырабатывается у человека в ответ на возбудитель. Образуются специализированные клетки (лимфоциты), которые продуцируют антитела к конкретному возбудителю. После инфекции в организме остаются "клетки памяти", и в случае последующих столкновений с возбудителем начинают снова (уже быстрее) продуцировать антитела.
Активный иммунитет может быть естественным и искусственным. Естественный приобретается в результате перенесенного заболевания. Искусственный вырабатывается при введении вакцин.
Пассивный иммунитет: в организм вводятся уже готовые антитела (гамма-глобулин). Введенные антитела в случае столкновения с возбудителем "расходуются" (связываются с возбудителем в комплекс "антиген-антитело"), если встречи с возбудителем не произошло, они имеют некий период полужизни, после чего распадаются. Пассивная иммунизация показана в тех случаях, когда необходимо в короткие сроки создать иммунитет на непродолжительное время (например, после контакта с больным).
Когда ребенок появляется на свет, он обычно имеет иммунитет (невосприимчивость) к некоторым инфекциям. Это заслуга борющихся с болезнями антител, которые передаются через плаценту от матери к будущему новорожденному. Передаются антитела против возбудителей тех болезней, которыми мать переболела или против которых была иммунизирована. Впоследствии, вскармливаемый грудью младенец постоянно получает дополнительную порцию антител с молоком матери. Это естественный пассивный иммунитет. Он также носит временный характер, угасая к концу первого года жизни.
Стерильный и нестерильный иммунитет
После заболевания в некоторых случаях иммунитет сохраняется пожизненно. Например корь, ветряная оспа. Это стерильный иммунитет. А в некоторых случаях иммунитет сохраняется только до тех пор, пока в организме есть возбудитель (туберкулез, сифилис) - нестерильный иммунитет.
4. Гемопоэз 4.1 Стволовые клетки крови
Стволовыми клетками называют клетки-предшественники, из которых образуются при необходимости все другие типы клеток, составляющие различные органы и ткани человека. Термин "стволовая клетка" впервые ввел в 1908 году русский гематолог из Санкт-Петербурга А. Максимов. Значительный объем исследований стволовых клеток проведен биологами А. Фриденштейном и И. Чертковым в России, в 60-х годах прошлого века. Именно они открыли мезенхимальные стволовые клетки (МСК) в костном мозге, обладающие уникальной регенерационной способностью. Отличие эмбриональных и мезенхимальных стволовых клеток заключается в том, что первые могут быть получены на ранней стадии развития эмбриона человека (из внутренней массы бластоцисты - оплодотворенной яйцеклетки - или из зачатков половых органов на самых ранних этапах развития, буквально в первые дни), а вторые встречаются в течение всей жизни человека во всех его органах и тканях. Эмбриональные СК значительно активнее мезенхимальных, обладают более высокой способностью размножения, большим потенциалом дифференцировки. Помимо мезенхимальных СК выделяют еще гемопоэтические клетки - предшественники клеток крови. Они встречаются в кровеносном русле в отличие от мезенхимальных, которые в крови циркулируют только при серьезных повреждениях организма.
Стволовые клетки способны восстанавливать кроветворение у облученных животных (радиозащитное действие), длительно поддерживать кроветворение и образовывать колониеобразующие единицы селезенки (двенадцатидневные селезеночные колонии), дающие начало гранулоцитарным, моноцитарным, эритроидным, мегакариоцитарным и лимфоидным колониям. Все клетки гемопоэтического происхождения образуются из примитивных стволовая кроветворная клеток (пСКК), локализованных в костном мозге и дающих начало клеткам четырех основных направлений дифференцировки:
мегакариоцитарного (тромбоциты),
миелоидного (гранулоциты и моноядерные фагоциты)
Дивергенция общего стволового элемента происходит на самом раннем этапе костномозговой дифференцировки.
Антигенпрезентирующие клетки в основном, но не исключительно, развиваются из миелоидных клеток-предшественников.
Клетки миелоидного и лимфоидного ряда наиболее важны для функционирования иммунной системы.
Лимфопоэтическая своловая клетка определяет две самостоятельные линии развития, приводящие к образованию Т-клеток и В-клеток.
Первая образующаяся из ГСК клетка-предшественник представляет собой колониеобразующуюся единицу (КОЕ) , которая определяет линии развития, приводящие к образованию гранулоцитов, эритроцитов, моноцитов и мегакариоцитов. Созревание этих клеток происходит под влиянием колониестимулирующих факторов (КСФ) и ряда интерлейкинов, в том числе ИЛ-1, ИЛ-3, ИЛ-4, ИЛ-5 и ИЛ-6. Все они играют важную роль в положительной регуляции (стимуляции) гемопоэза и продуцируются, главным образом, стромальными клетками костного мозга, но также и зрелыми формами дифференцированных миелоидных и лимфоидных клеток. Другие цитокины (например, ТРФ-бета) могут осуществлять понижающую регуляцию (подавление) гемопоэза).
У всех клеток как лимфоидного, так и миелоидного ряда время жизни ограничено, и все они непрерывно образуются.
У млекопитающих в период внутриутробного развития ГСК присутствуют в желточном мешке, печени, селезенке и костном мозге. Во взрослом организме гемопоэтические стволовые клетки находятся в основном в костном мозге, где они в норме довольно редко делятся, производя новые стволовые клетки (самообновление). Животное можно спасти от последствий облучения в летальных дозах введением клеток костного мозга, которые заселяют его лимфоидную и миелоидную ткани.
Плюрипотентные стволовые клетки дают начало коммитированным клеткам-предшественницам, которые уже необратимо определились как предки кровяных клеток одного или нескольких типов. Полагают, что коммитированные клетки делятся быстро, но ограниченное число раз, при этом делятся они под воздействием факторов микроокружения: соседних клеток и растворимых или мембраносвязанных цитокинов. В конце такой серии делений клетки эти становятся терминально дифференцированными, обычно больше не делятся и погибают через несколько дней или недель. Плюрипотентные стволовые клетки малочисленны, их трудно распознавать, и все еще неясно, как они выбирают свой путь среди разных вариантов развития. Программирование клеточных делений и выведение клеток на определенный путь дифференцировки (коммитирование), видимо, включают в себя и случайные события. Стволовая клетка плюрипотентна, т.к. дает начало многим видам терминально дифференцированных клеток. Что касается клеток крови, то эксперименты показывают, что все классы клеток крови - и миелоидных и лимфоидных - происходят от общей гемопоэтической стволовой клетки.
Гемопоэтическая стволовая клетка развивается следующим образом. У эмбриона гемопоэз начинается в желточном мешке, но по мере развития эта функция переходит к печени плода и, наконец, к костному мозгу, где и продолжается в течение всей жизни. Гемопоэтическая стволовая клетка, дающая начало всем элементам крови, плюрипотентна и заселяет другие гемо - и лимфопоэтические органы и самовоспроизводится, превращаясь в новые стволовые клетки. Животное можно спасти от последствий облучения в летальных дозах введением клеток костного мозга, которые заселяют его лимфоидную и миелоидную ткани.
Во взрослом организме гемопоэтические стволовые клетки находятся главным образом в костном мозге, где они в норме довольно редко делятся, производя новые стволовые клетки (самообновление).
Клетку-предшественницу, дающую в культуре клеток начало колонии эритроцитов, называют колониеобразующей единицей эритроидного ряда, или КОЕ-Э, и она дает начало зрелым эритроцитам после шести или даже меньшего числа циклов деления. КОЕ-Э еще не содержит гемоглобин.
Гемопоэзом (haemopoesis) называют развитие крови. Различают эмбриональный гемопоэз, который происходит в эмбриональный период
и приводит к развитию крови как ткани, и постэмбриональный гемопоэз, который представляет собой процесс физиологической регенерации крови. Развитие эритроцитов называют эритропоэзом, развитие гранулоцитов - гранулоцитопоэзом, тромбоцитов - тромбоцитопоэзом, развитие моноцитов - моноцитопоэзом, развитие лимфоцитов и иммуноцитов - лимфоцито - и иммуноцитопоэзом.
Эмбриональный гемопоэз.
В развитии крови как ткани в эмбриональный период можно выделить 3 основных этапа, последовательно сменяющих друг друга:
1) мезобластический, когда начинается развитие клеток крови во внезародышевых органах - мезенхиме стенки желточного мешка, хориона и стебля (с 3-й по 9-ю неделю развития зародыша человека) и появляется первая генерация стволовых клеток крови (СКК);
2) печеночный, который начинается в печени с 5-6-й недели развития плода, когда печень становится основным органом гемопоэза, в ней образуется вторая генерация СКК.
Кроветворение в печени достигает максимума через 5 месяцев и завершается перед рождением. СКК печени заселяют тимус (здесь, начиная с 7-8-й недели, развиваются Т-лимфоциты), селезенку (гемопоэз начинается с 12-й недели) и лимфатические узлы (гемопоэз отмечается с 10-й недели);
3) медуллярный (костномозговой) - появление третьей генерации СКК в костном мозге, где гемопоэз начинается с 10-й недели и постепенно нарастает к рождению, а после рождения костный мозг становится центральным органом гемопоэза.
Кроветворение в стенке желточного мешка. У человека оно начинается в конце 2-й - начале 3-й недели эмбрионального развития. В мезенхиме стенки желточного мешка обособляются зачатки сосудистой крови, или кровяные островки. В них мезенхимные клетки округляются, теряют отростки и преобразуются в стволовые клетки крови. Клетки, ограничивающие кровяные островки, уплощаются, соединяются между собой и образуют эндотелиальную выстилку будущего сосуда. Часть СКК дифференцируется в первичные клетки крови (бласты), крупные клетки с базофильной цитоплазмой и ядром, в котором хорошо заметны крупные ядрышки. Большинство первичных кровяных клеток митотически делится и превращается в первичные эритробласты, характеризующиеся крупным размером (мегалобласты). Это превращение совершается в связи с накоплением эмбрионального гемоглобина в цитоплазме бластов, при этом сначала образуются полихроматофильные эритробласты, а затем оксифилъные эритробласты с большим содержанием гемоглобина. В некоторых первичных эритробластах ядро подвергается кариорексису и удаляется из клеток, в других ядро сохраняется. В результате образуются безъядерные и ядросодержащие первичные эритроциты, отличающиеся большим размером по сравнению с нормоцитами и поэтому получившие название мегалоцитов. Такой тип кроветворения называется мегалобластическим. Он характерен для эмбрионального периода, но может появляться в постнатальном периоде при некоторых заболеваниях (злокачественное малокровие). Наряду с мегалобластическим в стенке желточного мешка начинается нормобластическое кроветворение, при котором из бластов образуются вторичные эритробласты; сначала они превращаются в полихроматофильные эритробласты, далее в нормобласты, из которых образуются вторичные эритроциты (нормоциты); размеры последних соответствуют эритроцитам (нормоцитам) взрослого человека. Развитие эритроцитов в стенке желточного мешка происходит внутри первичных кровеносных сосудов, т.е. интраваскулярно. Одновременно экстраваскулярно из бластов, расположенных вокруг сосудистых стенок, дифференцируется небольшое количество гранулоцитов - нейтрофилов и эозинофилов. Часть СКК остается в недифференцированном состоянии и разносится током крови по различным органам зародыша, где происходит их дальнейшая дифференцировка в клетки крови или соединительной ткани. После редукции желточного мешка основным кроветворным органом временно становится печень.
Кроветворение в печени. Печень закладывается примерно на 3-4-й неделе эмбриональной жизни, а с 5-й недели она становится центром кроветворения. Кроветворение в печени происходит экстраваскулярно, по ходу капилляров, врастающих вместе с мезенхимой внутрь печеночных долек. Источником кроветворения в печени являются стволовые клетки крови, из которых образуются бласты, дифференцирующиеся во вторичные эритроциты. Процесс их образования повторяет описанные выше этапы образования вторичных эритроцитов. Одновременно с развитием эритроцитов в печени образуются зернистые лейкоциты, главным образом нейтрофильные и эозинофильные. В цитоплазме бласта, становящейся более светлой и менее базофильной, появляется специфическая зернистость, после чего ядро приобретает неправильную форму. Кроме гранулоцитов, в печени формируются гигантские клетки - мегакариоциты. К концу внутриутробного периода кроветворение в печени прекращается.
Кроветворение в тимусе. Тимус закладывается в конце 1-го месяца внутриутробного развития, и на 1-8-й неделе его эпителий начинает заселяться стволовыми клетками крови, которые дифференцируются в лимфоциты тимуса. Увеличивающееся число лимфоцитов тимуса дает начало Т-лимфоцитам, заселяющим Т-зоны периферических органов иммунопоэза.
Кроветворение в селезенке. Закладка селезенки происходит в конце 1-го месяца эмбриогенеза. Из вселяющихся сюда стволовых клеток происходит экстраваскулярное образование всех видов форменных элементов крови, т.е. селезенка в эмбриональном периоде представляет собой универсальный кроветворный орган. Образование эритроцитов и гранулоцитов в селезенке достигает максимума на 5-м месяце эмбриогенеза. После этого в ней начинает преобладать лимфоцитопоэз.
Кроветворение в лимфатических узлах. Первые закладки лимфатических узлов человека появляются на 7-8-й неделе эмбрионального развития. Большинство лимфатических узлов развивается на 9-10-й неделе. В этот же период начинается проникновение в лимфатические узлы стволовых клеток крови, из которых на ранних стадиях дифференцируются эритроциты, гранулоциты и мегакариоциты. Однако формирование этих элементов быстро подавляется образованием лимфоцитов, составляющих основную часть лимфатических узлов. Появление единичных лимфоцитов происходит уже в течение 8-15-й недели развития, однако массовое "заселение" лимфатических узлов предшественниками Т - и В-лимфоцитов начинается с 16-й недели, когда формируются посткапиллярные венулы, через стенку которых осуществляется процесс миграции клеток. Из клеток-предшественников дифференцируются лимфобласты (большие лимфоциты), а далее средние и малые лимфоциты. Дифференцировка Т - и В-лимфоцитов происходит в Т - и В-зависимых зонах лимфатических узлов.
Кроветворение в костном мозге. Закладка костного мозга осуществляется на 2-м месяце эмбрионального развития. Первые гемопоэтические элементы появляются на 12-й неделе развития; в это время основную массу их составляют эритробласты и предшественники гранулоцитов. Из СКК в костном мозге формируются все форменные элементы крови, развитие которых происходит экстраваскулярно. Часть СКК сохраняется в костном мозге в недифференцированном состоянии, они могут расселяться по другим органам и тканям и являться источником развития клеток крови и соединительной ткани. Таким образом, костный мозг становится центральным органом, осуществляющим универсальный гемопоэз, и остается им в течение постнатальной жизни. Он обеспечивает стволовыми кроветворными клетками тимус и другие гемопоэтические органы.
Постэмбриональный гемопоэз. Постэмбриональный гемопоэз представляет собой процесс физиологической регенерации крови (клеточное обновление), который компенсирует физиологическое разрушение дифференцированных клеток.
Миелопоэз происходит в миелоидной ткани (textus myeloideus), расположенной в эпифизах трубчатых и полостях многих губчатых костей.
Здесь развиваются форменные элементы крови: эритроциты, гранулоциты, моноциты, кровяные пластинки, предшественники лимфоцитов.
В миелоидной ткани находятся стволовые клетки крови и соединительной ткани.
Предшественники лимфоцитов постепенно мигрируют и заселяют такие органы, как тимус, селезенка, лимфатические узлы и др.
Лимфопоэз происходит в лимфоидной ткани (textus lymphoideus), которая имеет несколько разновидностей, представленных в тимусе, селезенке, лимфатических узлах. Она выполняет основные функции: образование Т - и В-лимфоцитов и иммуноцитов (плазмоцитов и др.).
Миелоидная и лимфоидная ткани являются разновидностями соединительной ткани, т.е. относятся к тканям внутренней среды. В них представлены две основные клеточные линии - клетки ретикулярной ткани и гемопоэтические.
Ретикулярные, а также жировые, тучные и остеогенные клетки вместе с межклеточным веществом (матрикс) формируют микроокружение для
гемопоэтических элементов. Структуры микроокружения и гемопоэтические
клетки функционируют в неразрывной связи. Микроокружение оказывает
воздействие на дифференцировку клеток крови (при контакте с их рецепторами или путем выделения специфических факторов).
Для миелоидной и всех разновидностей лимфоидной ткани характерно
наличие стромальных ретикулярных и гемопоэтических элементов,
образующих единое функциональное целое. В тимусе имеется сложная строма, представленная как соединительнотканными, так и ретикулоэпителиальными клетками. Эпителиальные клетки секретируют особые вещества - тимозины, оказывающие влияние на дифференцировку из СКК Т-лимфоцитов. В лимфатических узлах и селезенке специализированные ретикулярные клетки создают микроокружение, необходимое для пролиферации и дифференцировки в специальных Т - и В-зонах Т - и В-лимфоцитов и плазмоцитов.
СКК являются плюрипотентными (полипотентными) предшественниками всех клеток крови и относятся к самоподдерживающейся популяции клеток. Они редко делятся. Впервые представление о родоначальных клетках крови сформулировал в начале XX в.А. А. Максимов, который считал, что по своей морфологии они сходны с лимфоцитами. В настоящее время это представление нашло подтверждение и дальнейшее развитие в новейших экспериментальных исследованиях, проводимых главным образом на мышах. Выявление СКК стало возможным при применении метода колониеобразования.
Экспериментально (на мышах) показано, что при введении смертельно облученным животным (утратившим собственные кроветворные клетки) взвеси клеток красного костного мозга или фракции, обогащенной СКК, в селезенке появляются колонии клеток - потомков одной СКК. Пролиферативную активность СКК модулируют колониестимулирующие факторы (КСФ), интерлейкины (ИЛ-3 и др.). Каждая СКК в селезенке образует одну колонию и называется селезеночной колониеобразующей единицей (КОЕ-С).
Подсчет колоний позволяет судить о количестве стволовых клеток, находящихся во введенной взвеси клеток. Таким образом, было установлено, что у мышей на 105 клеток костного мозга приходится около 50 стволовых клеток, из селезенки - 3,5 клетки, среди лейкоцитов крови - 1,4 клетки.
Исследование очищенной фракции стволовых клеток с помощью электронного микроскопа позволяет считать, что по ультраструктуре они очень близки к малым темным лимфоцитам.
Исследование клеточного состава колоний позволило выявить две линии их дифференцировки. Одна линия дает начало мультипотентной клетке - родоначальнице гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного рядов гемопоэза (КОЕ-ГЭММ). Вторая линия дает начало мультипотентной клетке - родоначальнице лимфопоэза (КОЕ-Л). Из мультипотентных клеток дифференцируются олигопотентные (КОЕ-ГМ) и унипотентные родоначальные (прогениторные) клетки.
Методом колониеобразования определены родоначальные унипотентные клетки для моноцитов (КОЕ-М), нейтрофильных гранулоцитов (КОЕ-Гн), эозинофилов (КОЕ-Эо), базофилов (КОЕ-Б), эритроцитов (БОЕ-Э и КОЕ-Э), мегакариоцитов (КОЕ-МГЦ), из которых образуются клетки-предшественники (прекурсорные). В лимфопоэтическом ряду выделяют унипотентные клетки - предшественницы для В-лимфоцитов и соответственно для Т - лимфоцитов. Полипотентные (плюрипотентные и мультипотентные), олигопотентные и унипотентные клетки морфологически не различаются.
Все приведенные выше стадии развития клеток составляют четыре основных компартмена: I - стволовые клетки крови (плюрипотентные, полипоте нтные); II - коммитированные родоначальные клетки (мультипотентные); III - коммитированные родоначальные (прогенторные) олигопотентные и унипотентные клетки; IV - клетки-предшественники (прекурсорные).
Дифференцировка полипотентных клеток в унипотентные определяется действием ряда специфических факторов - эритропоэтинов (для эритробластов), гранулопоэтинов (для миелобластов), лимфопоэтинов (для лимфобластов), тромбопоэтинов (для мегакариобластов) и др.
Из каждой клетки-предшественницы происходит образование конкретного вида клеток. Созревание каждого вида клеток проходит ряд стадий, которые в совокупности образуют компартмент созревающих клеток (V).
Зрелые клетки представляют последний компартмент (VI). Все клетки V и VI компартментов морфологически можно идентифицировать.
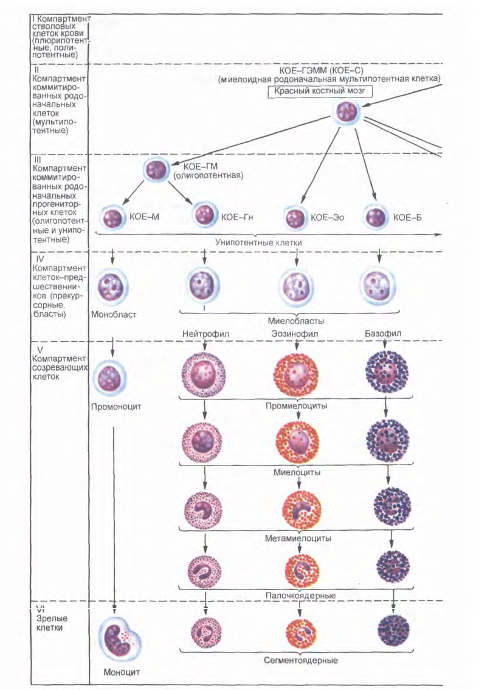
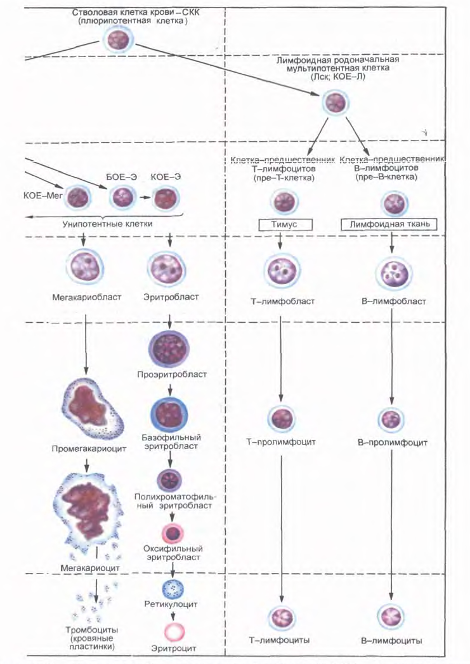
Рис.18. Постэмбриональный гемопоэз, окраска азур 11-эозином (схема по НАЮриной). Стадии дифферениировки крови: I-IV - морфологически неидентифицируемые клетки; V - VI - морфологически идентифицируемые клетки. Б - базофил; БОЕ - бурстобраэуюшая единица; Г - гранулоциты; Гн - гранулоцит нейтрофильный; КОЕ - колониеобразующ! единицы; КОЕ-С - селезеночная колониеобразующая единица; Л - лимфоцит; Лек - mt фоидная стволовая клетка; М - моноцит; Мет - мегакариошгг; Эо - эозинофил; Э - эритроцит.
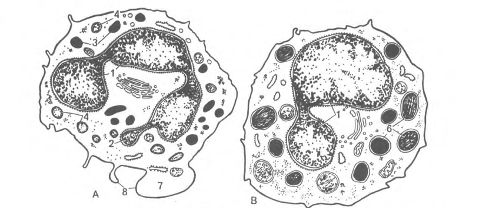
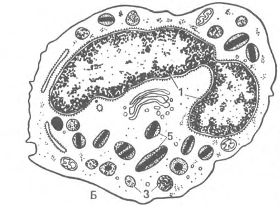
Рис. 19. Ультрамикроскопическое строение гранулоцитов (схема по НА. Юриной и Л.С. Румянцевой).
А - сегментоядерный нейтрофильный гранулоцит; Б – эозинофильный (ацидофильный) гранулоиит; В - базофильный фанулоцит: 1 - сегменты ядра; 2 - тельце полового хроматина; 3 – первичные (азурофильные) гранулоциты; 4 - вторичные (специфические) гранулы; 5 - зрелые специфические гранулы эозинофила, содержащие кристаллоиды; б - гранулы базофила различной величины и плотности; 7 - периферическая зона, не содержащая органелл; 8 – микроворсинки и псевдоподии.
Рис. 20. Эмбриональный гемоппэп (по А.А. Максимову).
А - кроветворение в стенке желточного мешка зародыша морской свинки: 1 - меэенхималыгые клетки; 2 - эндотелий стенки сосудов; 3 - первичные кровяные клетки-бласты; 4 - митотическос деление бластов; Б - поперечный срез кровяного островка зародыша кролика S'/j сут: I - полость сосуда; 2 - эндотелий; 3 - интраваскулярные кровяные клетки; 4 - делящаяся кровяная клетка; 5 - формирование первичной кровяной клетки; 6 - энтодерма; 7 - висцеральный листок мезодермы. В - развитие вторичны); эритробластов в сосуде зародыша кролика 13'Д сут: 1 - эндотелий; 2 - проэритробласты; 3 - базофильные эритробласты; 4 - полихроматофильные эритробласты; 5 - оксифильные эритробласты (нормобласты); 6 - оксифильный эритробласт с пикнотическим ядром; 7 - обособление ядра от оксифильного эритробласта (нормобласта); 8 - вытолкнутое ядро нормобласта; 9 - вторичный эритроцит. Г - кроветворение в костном мозге зародыша человека с длиной тела 77 мм. Экстра во скул я рное развитие клеток крови: 1 - эндотелий сосуда; 2 - бласты; 3 - нейтрофильные гранулоциты; 4 - эоэинофильный миелоцит.
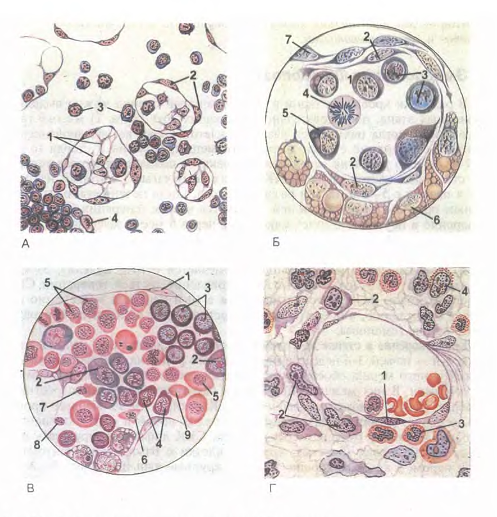
Механизмы реализации путей гибели клеток.
Перепечатка материалов без ссылки на наш сайт запрещена