Реферат: Дыхание растений
Реферат: Дыхание растений
Введение
Дыхание — процесс универсальный. Оно является неотъемлемым свойством всех организмов, населяющих нашу планету, и присуще любому органу, любой ткани, каждой клетке, которые дышат на протяжении всей своей жизнедеятельности. Дыхание всегда связано с жизнью, тогда как прекращение дыхания — с гибелью живого.
Жизнь организма в целом, как и каждое проявление жизнедеятельности, необходимо связаны с расходованием энергии. Клеточное деление, рост, развитие и размножение, поглощение и передвижение воды и питательных веществ, разнообразные синтезы и все другие процессы и функции осуществимы лишь при постоянном удовлетворении обусловленных ими потребностей в энергии и пластических веществах, которые служат клетке строительным материалом.
Источником энергии для живой клетки служит химическая (свободная) энергия потребляемых ею питательных веществ. Распад этих веществ, происходящий в акте дыхания, сопровождается освобождением энергии, которая и обеспечивает удовлетворение жизненных потребностей организма.
Сам же процесс дыхания представляет собой сложную многозвенную систему сопряженных окислительно-восстановительных процессов, в ходе которых имеет место изменение химической природы органических соединений и использование содержащейся в них энергии.
1. Дыхание. Определение. Уравнение. Значение дыхания в жизни растительного организма. Специфика дыхания у растений
Клеточное дыхание — это окислительный, с участием кислорода распад органических питательных веществ, сопровождающийся образованием химически активных метаболитов и освобождением энергии, которые используются клетками для процессов жизнедеятельности.
Суммарное уравнение процесса дыхания:
С6Н12О6 + 602 ► 6С02 + 6Н20 + 2875 кДж/моль
Не вся энергия, высвобождаемая при дыхании, может быть использована в процессах жизнедеятельности. Используется организмом в основном та энергия, которая аккумулируется в АТФ. Синтезу АТФ во многих случаях предшествует образование разности электрических зарядов на мембране, что, в свою очередь, связано с разностью концентраций ионов водорода по разные стороны от мембраны. Согласно современным представлениям, е только АТФ, но и протонный градиент служат источником энергии для различных процессов жизнедеятельности клетки. Обе формы энергии могут быть использованы на процессы синтеза, процессы поступления, передвижения питательных веществ и воды, создание разности потенциалов между цитоплазмой и внешней средой. Энергия, не накопленная в протонном градиенте и АТФ, в основном рассеивается в виде тепла или света и является для растения бесполезной.
Значение дыхания в жизни растения.
Дыхание — один из центральных процессов обмена веществ растительного организма. Выделяющаяся при дыхании энергия тратится как на процессы роста, так и нa поддержание в активном состоянии уже закончивших рост органов растения. Вместе с тем значение дыхания не ограничивается тем, что это процесс, поставляющий энергию. Дыхание, подобно фотосинтезу, сложный окислительно_восстановительный процесc, идущий через ряд этапов. На его промежуточных стадиях образуются органические соединения, которые затем используются в различных метаболических реакциях. К промежуточным соединениям относят органические кислоты и пентозы образующиеся при разных путях дыхательного распада. Таким образом, процесс дыхания — источник многих метаболитов. Несмотря на то что процесс дыхания в суммарном виде противоположен фотосинтезу, в некоторых случаях они могут дополнять друг друга. Оба процесса являются поставщиками как энергетических эквивалентов (АТФ, НАДФ-Н), так и метаболитов. Как видно из суммарного уравнения, в процессе дыхания образуется также вода. Эта вода в крайних условиях обезвоживания может быть использована растением и предохранить его от гибели. В некоторых случаях, когда энергия дыхания выделяется в виде тепла, дыхание ведет к бесполезной потере сухого вещества. В этой связи при рассмотрении процесса дыхания надо помнить, что не всегда усиление процесса дыхания является полезным для растительного организма.
2. Основные этапы становления учения о дыхании растений
Научные основы учения о роли кислорода в дыхании были заложены трудами А.Л.Лавуазье. В 1774 г. кислород независимо открыли Пристли и Шееле, а Лавуазье дал название этому элементу. Изучая одновременно процесс дыхания животных и горение, Лавувзье в 1773-1783 гг. пришел к выводу, что при дыхании, как и при горении, поглощается кислород и образуется углекислый газ, причем в том и другом случаях выделяется тепло. На основании своих опытов он заключил, что процесс горения состоит в присоединении кислорода к субстрату и что дыхание есть медленно текущее горение питательных веществ в живом организме.
Я.Ингенхауз в 1778-1780 гг. показал, что зеленые растения в темноте, а незеленые части растений и в темноте, и на свету поглощают кислород и выделяют углекислый газ. В своей работе, опубликованной в 1779 г. он писал:
«Когда солнце, поднявшееся над горизонтом, разбудит своими лучами заснувшие за ночь растения, оно сделает их способными исполнять свою целительную функцию – исправлять воздух для животных; во мраке ночи эта деятельность совсем прекращается; днем же совершается с тем большим оживлением, чем светлее день и чем выгоднее расположено растение в отношении солнечных лучей. Затененные высокими зданиями или другими растениями, они не исправляют воздух, а, наоборот, выделяют вредный для дыхания животных воздух. К концу дня выработка очищенного воздуха ослабевает и при заходе солнца совершенно прекращается».
Первые точные исследования процесса дыхания у растений принадлежат Соссюру (1804). Он брал свежие листья и помещал их на ночь в сосуд, наполненный воздухом. При этом кислород воздуха поглощался и выделялся углекислый газ. Если на следующий день листья снова выставлялись на солнечный свет, то они выделяли почти такое же количество кислорода, какое поглотили ночью. Свои исследования Соссюр распространил и на незеленые части растений: стебли древесных растений, цветки, корни, плоды, и доказал, что дыхание наблюдается также в клетках этих органов. Он обнаружил, что при дыхании потеря в весе растения равна весу выделенного углерода.
Соссюр обратил внимание и на то, что молодые, растущие части растения, например новые побеги и распускающиеся цветки, дышат интенсивнее и потребляют кислорода больше, чем части растения, прекратившие рост.
Если, по Лавуазье, дыхание имеет сходство с процессом горения, то каким же образом органические вещества могут «гореть» при обычной температуре тела организма, да еще в водной среде, (ведь на 70 — 90% масса живых организмов состоит из воды)? Возникло предположение о том, что в живых клетках существуют механизмы, активирующие кислород. Швейцарский химик X. Ф. Шейнбайн, открывший озон, изучал причины быстрого потемнения пораненной поверхности растительных тканей, таких, как ткани яблок, картофеля, плодовых тел грибов. В 1845 г. он выступил со своей теорией окислительных процессов, согласно которой в живых клетках имеются соединения, способные легко окисляться в присутствии 02 и таким образом активировать молекулярный кислород. Если ткань прокипятить, то потемнения не происходит. Следовательно, потемнение тканей — каталитический окислительный процесс. Шейнбайн ошибочно полагал, что активация кислорода — это образование озона.
Исследования, начатые Шейнбайном, продолжил А. Н. Бах, который в 1897 г. разработал перекисную теорию биологического окисления, приложив ее к процессам дыхания. Несколько позже, в том же 1897 г., аналогичные взгляды высказал немецкий исследователь К. Энглер.
Суть перекисной теории биологического окисления Баха заключается в следующем. Молекулярный кислород имеет двойную связь и для того чтобы его активировать, необходимо эту двойную связь расщепить. Легко окисляющееся соединение А взаимодействует с кислородом и, разрывая двойную связь, образует пероксид А02 Таким образом, по мысли Баха, активация кислорода есть образование пероксида. В свою очередь пероксидное соединение, взаимодействуя с соединением В, окисляет его; затем эта реакция повторяется со вторым атомом кислорода и второй молекулой соединения В. Получается полностью восстановленное исходное соединение — акцептор кислорода А и полностью окисленное вещество В.
Много позднее, в 1955 г., две группы исследователей — О. Хаяиши с сотр. в Японии и Г. С. Мэзон с сотр. в США, используя современные методы, проанализировали возможность включения кислорода в органические соединения.
В настоящее время известно, что путь включения кислорода в органические соединения в соответствии с перекисной теорией биологического окисления Баха и Энглера не имеет отношения к дыханию, однако работы этих исследователей сыграли большую роль в изучении химизма дыхания, заложив основы современного понимания механизмов активации кислорода.
История современного учения о дыхании растений неразрывно связана с именем академика В.И. Палладина.
В годы первого петербургского периода работы Палладин исследовал ферментативную природу дыхательного процесса. Палладин показал, что и анаэробная, и аэробная фазы дыхания обеспечиваются специфическими ферментами, последовательно перерабатывающими продукты дыхания. Итоги работ этого периода изложены в монографии В.И. Палладина «Дыхание как сумма ферментативных процессов» (1907).
Одновременно с Палладиным проблемой дыхания занимались в целом ряде крупнейших научно-исследовательских институтов и лабораторий Западной Европы. Наибольшую популярность приобрели две новые школы – Виланда и Варбурга.
Т. Виланд развивал взгляды на роль дегидраз и водородных акцепторов, вполне аналогичные взглядам Палладина. Расхождение их теорий заключалось в том, что Виланд категорически отрицал какую бы то ни было роль оксидаз как специфических активаторов кислорода, считая молекулярный кислород способным самостоятельно отнимать водород от водородного акцептора. По мнению же Палладина, водородные акцепторы не могут самопроизвольно освобождаться от водорода, но требуют для этого участия оксидаз, которые поэтому являются обязательным фактором в реакции, выраженной во втором уравнении Палладина.
Противник Виланда, Варбург, считал, что молекулярный кислород не может вступить в организме в какой бы то ни было окислительный процесс, если в организме отсутствует система железоорганических соединений, типичным представителем которых он считал геминфермент. Варбург утверждал, что геминфермент активирует молекулярный кислород, т.е. как бы дает первый толчок к началу окислительных процессов, и без него никакой дыхательный процесс не может совершаться. Далее, по мнению Варбурга, окислительный импульс через промежуточные звенья (геминовые соединения) доходит до дыхательного субстрата и окисляет его. Резюмируя свои взгляды, Варбург утверждал, что дыхание осуществляется путем активации кислорода, а отнюдь не водорода. Но ведь Палладин как раз и говорил о той же необходимости активации молекулярного кислорода, защищая перед Виландом роль оксидаз в процессе дыхания.
Все различие в основных посылках Варбурга и Палладина заключается в том, что первый, работая по преимуществу с объектами животного происхождения, называл свой активатор молекулярного кислорода геминферментом, а Палладин, работавший с объектами растительного происхождения, сохранил за этим активатором ранее установившееся в науке название оксидазы. Но по существу оба говорили об одном и том же, протестуя против непримиримой позиции Виланда, отрицавшего необходимость энзиматической активации молекулярного кислорода.
Английский биохимик Д. Кейлин в 1925 г. доказал присутствие в клетках цитохромоксидазы, ускоряющей поглощение ими кислорода, и открыл другие цитохромы. Затем цитохромы были обнаружены у всех аэробов и было показано, что у этих организмов на завершающем этапе процесса дыхания осуществляется перенос на кислород электронов и протонов, в результате чего образуется Н20 (или Н202).
3.Каталитические системы дыхания
Окисление дыхательных субстратов в ходе дыхания осуществляется с участием ферментов. Ферменты как белковые катализаторы, помимо свойств, присущих неорганическим катализаторам, обладают рядом особенностей: высокой активностью, высокой специфичностью по отношению к субстратам и высокой лабильностью. Их пространственная организации зависящая от нее активность изменяются под действием внешних и внутренних факторов. Эти свойства обеспечивают возможность тонкой регуляции обмена веществ на уровне ферментов.
Типы окислительно-восстановительных реакций. Существуют четыре способа окисления, и все они связаны с отнятием электронов:
1) непосредственная отдача электронов, например:
![]()
2) Отнятие водорода:
![]()
3) присоединение кислорода:
![]()
4) образование промежуточного гидратированного соединения с последующим отнятием двух электронов и протонов:
![]()
Оксидоредуктазы.
Поскольку окисление одного вещества (донора электронов и протонов) сопряжено с восстановлением другого соединения (их акцептора), ферменты, катализирующие эти реакции, называют оксидоредуктазами. Все они относятся к I классу ферментов:
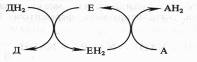
Донор (Д) отдает электроны и протоны, акцептор (А) принимает их, а энзим (Е) осуществляет реакцию переноса. Существуют три группы оксидоредуктаз:
а) анаэробные дегидрогеназы передают электроны различным промежуточным акцепторам, но не кислороду;
б) аэробные дегидрогеназы передают электроны различным акцепторам, в том числе кислороду;
в) оксидазы способны передавать электроны только кислороду.
Анаэробные дегидрогеназы. Это двухкомпонентные ферменты, коферментом которых может быть НАД+ (никотинамидадениндинуклеотид):
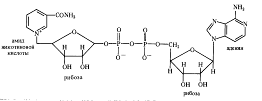
При окислении субстрата НАД+ превращается в восстановленную форму НАДH, а второй протон субстрата диссоциирует в среду (НАДH+ Н+). К анаэробным НАД-зависимым дегидрогеназам относятся такие ферменты, как алкогольдегидрогеназа, лактатдегидрогеназа, малатдегидрогеназа и др. Коферментом анаэробных дегидрогеназ может быть также НАДФ+ (никотинамидадениндинуклеотидфосфат), содержащий на одну фосфатную группировку больше, чем НАД + . НАДФ- зависимыми дегидрогеназами являются изоцитратдегидрогеназа, глюкозо-6-фосфатдегидрогеназа, 6-фосфоглюконатдегидрогеназа и др.
Субстратная специфичность фермента зависит от его белковой части. Многие НАД- и НАДФ-зависимые дегидрогеназы нуждаются в присутствии ионов двухвалентных металлов. Например, алкогольдегидрогеназа содержит ионы цинка.
Окисленные и восстановленные формы коферментов анаэробных дегидрогеназ могут взаимопревращаться в реакции, катализируемой ферментом НАД(Ф)-трансгидрогеназой:
НАДФH + НАД+ = НАДФ+ + НАДH
Анаэробные дегидрогеназы передают водород, т. е. электроны и протоны, различным промежуточным переносчикам и аэробным дегидрогеназам.
Аэробные дегидрогеназы. Это также двухкомнонентные ферменты, получившие название флавиновых (флавопротеины).
Помимо белков, в их состав входит прочно связанная с ними простетическая группа — рибофлавин (витамин В2).
Различают два кофермента этой группы: флавинмононуклеотид (ФМН), или желтый дыхательный фермент Варбурга, и флавинадениндинуклеотид (ФАД).
ФМН (рибофлавин-5-фосфат) содержит гетероциклическое азотистое основание — диметилизоаллоксазин, спирт рибит (производное рибозы) и фосфат:
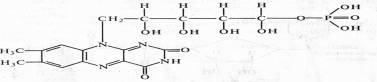
В ФАД кроме ФМН имеется еще один нуклеотид — аденозинмонофосфата:
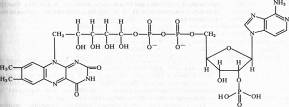
Активной группой в реакции присоединения и отдачи электронов и протонов в ФМН и ФАД служит изоаллоксазин. Взаимодействие с восстановленным переносчиком, например НАДH, происходит следующим образом:
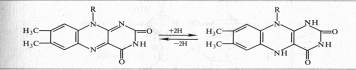
Примером дегидрогеназы, в состав которой входит ФАД, является сукцинатдегидрогеназа. Доноры электронов для аэробных дегидрогеназ — анаэробные дегидрогеназы, а акцепторы — хиноны, цитохромы, кислород.
Цитохромная система. Среди оксидаз очень важную роль играют железосодержащие ферменты и переносчики, относящиеся к цитохромной системе. В нее входят цитохромы " и цитохромоксидаза. Включаясь в определенной последовательности в процесс переноса электронов, они передают их от флавопротеинов на молекулярный кислород.
Все компоненты цитохромной системы содержат железопорфириновую простетическую группу.
При переносе электронов цитохромами железо обратимо окисляется и восстанавливается, отдавая или приобретая электрон и изменяя таким образом свою валентность. В дыхательной цепи направление транспорта электронов определяется величиной окислительно-восстановительного потенциала цитохромов.
В этой системе передавать электроны непосредственно на кислород способна только цитохромоксидаза (цит. а + а3). Из всех известных оксидаз она имеет наибольшее сродство к кислороду. Ингибиторами цитохромоксидазы являются СО, цианид, азид. Б растительных митохондриях кроме цитохромоксидазы функционирует оксидаза, не подавляемая цианидом и названная альтернативной оксидазой. Например, в митохондриях початков ароидных активность цианидустойчивой оксидазы в 10 раз превышает активность цитохромоксидазы.
Пероксидаза и каталаза. К пероксидазам относят целую группу ферментов, использующих в качестве окислителя пероксид водорода: классическую пероксидазу, НАД-пероксидазу, НАДФ-пероксидазу, пероксидазу жирных кислот, глутатионпероксидазу, цитохромпероксидазу и др. Все они работают по следующей схеме, где А — субстраты:
![]()
В последние 2 — 3 десятилетия показана полифункциональность пероксидаз. Помимо пероксидазной, у них имеется оксидазная функция, т. е. способность переносить электроны в отсутствие пероксидного кислорода на молекулярный кислород. Пероксидаза может также функционировать как анаэробная дегидрогеназа, например НАДH-дегидрогеназа, передающая электроны от восстановленных пиридиновых нуклеотидов на разные акцепторы.
Пероксид водорода, помимо пероксидазы, расщепляется также каталазой, в результате чего образуется молекулярный кислород. В реакции участвуют две молекулы пероксида, одна из которых функционирует как донор, а другая — как акцептор электронов.
Простетической группой пероксидазы и каталазы служит гем, в состав которого входит атом железа.
Оксигеназы. Наряду с оксидазами, которые используют молекулярный кислород как акцептор электронов, в клетках широко представлены оксигеназы, активирующие кислород, в результате чего он может присоединяться к органическим соединениям. Ферменты, внедряющие в субстрат два атома кислорода, называют диоксигеназами, а присоединяющие один атом кислорода — монооксигеназами или гидроксилазами. В качестве доноров электронов оксигеназы используют НАД(Ф)H, ФАДH2 и др.
Оксигеназы присутствуют во всех типах клеток. Они участвуют в гидроксилировании многих эндогенных соединений в частности аминокислот, фенолов, стеринов и др., а также в детоксикации чужеродных токсических веществ (ксенобиотиков).
4.Основные пути диссимиляции углерода
Существуют два основных пути окисления углеводов: 1) дихотомический (гликолитический) и 2) апотомический (пентозофосфатный). Белки, жиры и органические кислоты окисляются в глиоксилатном цикле.
Относительная роль этих путей дыхания может меняться в зависимости от типа растений, возраста, фазы развития, а также в зависимости от условий внешней среды. Процесс дыхания растений осуществляется во всех внешних условиях, в которых возможна жизнь. Растительный организм не имеет приспособлений к регуляции температуры, поэтому процесс дыхания осуществляется при температуре от – 50 до +50°С. Нет приспособлений у растений и к поддержанию равномерного распределения кислорода по всем тканям. Именно необходимость осуществления процесса дыхания в разнообразных условиях привела к выработке в процессе эволюции разнообразных путей дыхательного обмена и к ещё большему разнообразию ферментативных систем, осуществляющих отдельные этапы дыхания. При этом важно отметить взаимосвязь всех процессов обмена в организме. Изменение пути дыхательного обмена приводит к глубоким изменениям во всем метаболизме растительных организмов.
4.1 Дихотомический путь
Это основной путь распада органических веществ для всех живых организмов. Выделяют 2 этапа дихотомического пути: гликолиз и цикл Кребса.
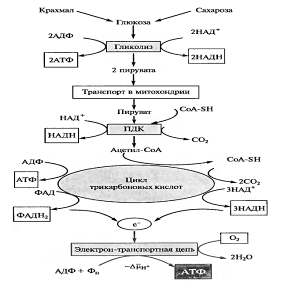
Рис. 1 Основные этапы дыхания
4.1.1 Гликолиз. Механизмы регуляции цикла. Энергетическая эффективность процесса, значение. Связь с другими процессами
Гликолиз — процесс анаэробного распада глюкозы, идущий Гликолиз с освобождением энергии, конечным продуктом которого является пировиноградная кислота. Гликолиз — общий начальный этап аэробного дыхания и всех видов брожения. Реакции гликолиза протекают в растворимой части цитоплазмы (цитозоле) и в хлоропластах. В цитозоле гликолитические ферменты, по-видимому, организованы в мультиэнзимные комплексы с участием актиновых филаментов цитоскелета, с которыми гликолитические ферменты обратимо связываются с разной степенью прочности. Такое связывание обеспечивает векторность процесса гликолиза.
Английский биохимик А. Гарден и ученик К. А. Тимирязева Л. А. Иванов в 1905 г. независимо показали, что в процессе спиртового брожения наблюдается связывание неорганического фосфата и превращение его в органическую форму. Гарден установил, что глюкоза подвергается анаэробному распаду только после ее фосфорилирования. Полностью весь процесс гликолиза расшифровали немецкие биохимики Г. Эмбден, О. Ф. Мейергоф и советский биохимик Я. О. Парнас, с именами которых связывают название этого катаболического
Цепь реакций, составляющих суть гликолиза, можно разбить на три этапа:
I. Подготовительный этап — фосфорилирование гексозы и ее расщепление на две фосфотриозы.
II. Первое субстратное фосфорилирование, которое начинается с 3-фосфоглицеринового альдегида и кончается 3-фосфоглицериновой кислотой. Окисление альдегида до кислоты связано с освобождением энергии. В этом процессе на каждую фосфотриозу синтезируется одна молекула АТФ.
III. Второе субстратное фосфорилирование, при котором 3-фосфоглицериновая кислота за счет внутримолекулярного окисления отдает фосфат с образованием АТФ.
Поскольку глюкоза стабильное соединение, на ее активацию необходима затрата энергии, что осуществляется в процессе образования фосфорных эфиров глюкозы в ряде подготовительных реакций. Глюкоза (в пиранозной форме) фосфорилируется АТФ с участием гексокиназы (1), превращаясь в глюкозо-6-фосфат, который изомеризуется в фруктозо-6-фосфат с помощью глюкозофосфатизомеразы (2).
Этот - переход необходим для образования более лабильной фуранозной формы молекулы гексозы. Фруктозо-6-фосфат фосфорилируется вторично фосфофрукгокиназой с использованием еще одной молекулы АТФ (3).
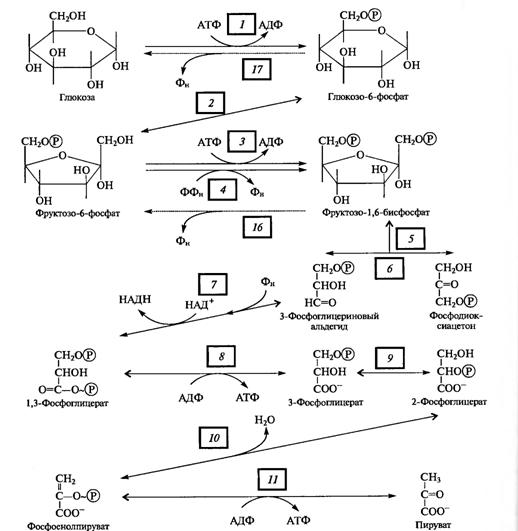
Рис. 2. Реакции гликолиза
Фруктозо-1,6-дифосфат — лабильная фуранозная форма с симметрично расположенными фосфатными группами. Обе эти группы несут отрицательный заряд, отталкиваясь друг от друга электростатически. Такая структура легко расщепляется альдолазой на две фосфотриозы. Следовательно, смысл подготовительного этапа состоит в активации молекулы гексозы за счет двойного фосфорилирования и перевода в фуранозную форму с последующим распадом на 3-фосфоглицериновый альдегид (3-ФГА) и фосфодиоксиацетон (ФДА) (5), причем бывший 6-й атом углерода в молекуле глюкозы и фруктозы (фосфорилированный) становится 3-м в 3-ФГК, а 1-й атом углерода фруктозо-1,6-дифосфата остается 1-м углеродом (фосфорилированным) в ФДА. 3-ФГА и ФДА легко превращаются друг в друга с участием триозофосфатизомеразы (6). Из-за расщепления молекулы гексозы на две триозы гликолиз иногда называют дихотомическим путем окисления глюкозы.
С 3-ФГА начинается II этап гликолиза — первое субстратное фосфорилирование. Фермент дегидрогеназа фосфоглицеринового альдегида (НАД-зависимый SH-фермент) (7) образует с 3-ФГА фермент-субстратный комплекс, в котором происходит окисление субстрата и передача электронов и протонов на НАД+. В ходе окисления фосфоглицеринового альдегида до фосфоглицериновой кислоты в фермент-субстратном комплексе возникает меркаптанная высокоэнергетическая связь (т. е. связь с очень высокой свободной энергией гидролиза). Далее осуществляется фосфоролиз этой связи, в результате чего SH-фермент отщепляется от субстрата, а к остатку карбоксильной группы субстрата присоединяется неорганический фосфат, причем ацилфосфатная связь сохраняет значительный запас энергии, освободившейся в результате окисления 3-ФГА. Высокоэнергетическая фосфатная группа с помощью фосфоглицераткиназы передается на АДФ и образуется АТФ (8). Так как в данном случае высокоэнергетическая ковалентная связь фосфата формируется прямо на окисляемом субстрате, такой процесс получил название субстратного фосфорилирования. Таким образом, в результате II этапа гликолиза образуются АТФ и восстановленный НАДH.
Последний этап гликолиза — второе субстратное фосфорилирование. З-Фосфоглицериновая кислота с помощью фосфоглицератмутазы превращается в 2-фосфоглицериновую кислоту (9). Далее фермент енолаза катализирует отщепление молекулы воды от 2-фосфоглицериновой кислоты (10). Эта реакция сопровождается перераспределением энергии в молекуле, в результате чего образуется фосфоенолпируват — соединение, содержащее высокоэнергетическую фосфатную связь. Таким образом, в этом случае высокоэнергетическая фосфатная связь формируется на основе того фосфата, который имелся в самом субстрате. Этот фосфат при участии пируваткиназы (11) передается на АДФ и образуется АТФ, а енолпируват самопроизвольно переходит в более стабильную форму — пируват — конечный продукт гликолиза.
Энергетический выход гликолиза. При окислении одной молекулы глюкозы образуются две молекулы пировиноградной кислоты. При этом за счет первого и второго субстратного фосфорилирования образуются четыре молекулы АТФ. Однако две молекулы АТФ тратятся на фосфорилирование гексозы на I этапе гликолиза. Таким образом, чистый выход гликолитического субстратного фосфорилирования составляет две молекулы АТФ.
Кроме того, на II этапе гликолиза на каждую из двух молекул фосфотриоз восстанавливается по одной молекуле НАДH. Окисление одной молекулы НАДH в электронтранспортной цепи митохондрий в присутствии 02 сопряжено с синтезом трех молекул АТФ, а в расчете на две триозы (т. е. на одну молекулу глюкозы) - шесть молекул АТФ. Таким образом, всего в процессе гликолиза (при условии последующего окисления НАДН) образуются восемь молекул АТФ. Поскольку свободная энергия гидролиза одной молекулы АТФ во внутриклеточных условиях составляет около 41,868 кДж/моль (10 ккал), восемь молекул АТФ дают 335 кДж/моль, или 80 ккал. Таков полный энергетический выход гликолиза в аэробных условиях.
Обращение гликолиза. Возможность обращения гликолиза определяется обратимостью действия большинства ферментов, катализирующих его реакции. Однако реакции фосфорилирования глюкозы и фруктозы, а также реакция образования пировиноградной кислоты из фосфоенолпирувата, осуществляемые с помощью киназ, необратимы. На этих участках процесс обращения идет благодаря использованию обходных путей. Там, где функционируют гексокиназа и фруктокиназа, происходит дефосфорилирование — отщепление фосфатных групп фосфатазами.
Превращение пирувата в фосфоенолпируват также не может осуществиться путем прямого обращения пируваткиназной реакции вследствие большого перепада энергии. Первая реакция обращения гликолиза на этом участке катализируется митохондриальной пируваткарбоксилазой в присутствии АТФ и ацетил-СоА (последний выполняет функции активатора). Образующаяся щавелевоуксусная кислота (ЩУК), или оксалоацетат, восстанавливается затем в митохондриях до малата при участии НАД-зависимой малатдегидрогеназы (МДГ). Затем малат транспортируется из митохондрий в цитоплазму, где окисляется НАД-зависимой цитоплазматической малатдегидрогеназой снова до ЩУК. Далее под действием ФЕП-карбоксикиназы из оксалоацетата образуется фосфоенолпируват. Фосфорилирование в этой реакции осуществляется за счет АТФ.
Значение гликолиза в клетке. В аэробных условиях гликолиз выполняет ряд функций: 1) осуществляет связь между дыхательными субстратами и циклом Кребса; 2) поставляет на нужды клетки две молекулы АТФ и две молекулы НАДH при окислении каждой молекулы глюкозы (в условиях аноксии гликолиз, по-видимому, служит основным источником АТФ в клетке); 3) производит интермедиа, необходимые для синтетических процессов в клетке (например, фосфоенолпируват, необходимый для образования фенольных соединений и лигнина); 4) в хлоропластах гликолитические реакции обеспечивают прямой путь для синтеза АТФ, независимый от поставок НАДФH; кроме того, через гликолиз в хлоропластах запасенный крахмал метаболизируется в триозы, которые затем экспортируются из хлоропласта.
Регуляция гликолиза.
Интенсивность гликолиза контролируется в нескольких участках. Вовлечение глюкозы в процесс гликолиза регулируется на уровне Фермента гексокиназы по типу обратной связи: избыток продукта реакции (глюкозо-6-фосфата) аллостерически подавляет деятельность фермента.
Второй участок регуляции скорости гликолиза находится на уровне фосфофруктокиназы. Фермент аллостерически ингибируется высокой концентрацией АТФ и активируется неорганическим фосфатом и АДФ. Ингибирование АТФ предотвращает развитие реакции в обратном направлении при высокой концентрации фруктозо-6-фосфата. Кроме того, фермент подавляется продуктом цикла Кребса — цитратом и через положительную обратную связь активируется собственным продуктом — фруктозо-1,6-дифосфатом (самоусиление).
Высокие концентрации АТФ подавляют активность пируваткиназы, снижая сродство фермента к фосфоенолпирувату. Пируваткиназа подавляется также ацетил-СоА.
Наконец, пируватдегидрогеназный комплекс, участвующий в образовании ацетил-СоА из пирувата, ингибируется высокими концентрациями АТФ, а также НАДH и собственным продуктом — ацетил-СоА.
4.1.2 Цикл Кребса. Механизмы регуляции цикла. Энергетическая эффективность процесса, значение
В анаэробных условиях пировиноградная кислота (пируват) подвергается дальнейшим превращениям в ходе спиртового, молочнокислого и других видов брожений, при этом НАДH используется для восстановления конечных продуктов брожения, регенерируя в окисленную форму. Последнее обстоятельство поддерживает процесс гликолиза, для которого необходим окисленный НАД + . В присутствии достаточного количества кислорода пируват полностью окисляется до С02 и Н20 в дыхательном цикле, получившем название цикла Кребса, цикла ди- или трикарбоновых кислот. Все участки этого процесса локализованы в мАТФиксе или во внутренней мембране митохондрий.
Последовательность реакций в цикле Кребса. Участие органических кислот в дыхании давно привлекало внимание исследователей. Еще в 1910 г. шведский химик Т. Тунберг показал, что в животных тканях содержатся ферменты, способные отнимать водород от некоторых органических кислот (янтарной, яблочной, лимонной). В 1935 г. А. Сент-Дьердьи в Венгрии установил, что добавление к измельченной мышечной ткани небольших количеств янтарной, фумаровой, яблочной или щавелевоуксуснсй кислот резко активирует поглощение тканью кислорода.
Учитывая данные Тунберга и Сент-Дьердьи и исходя из собственных экспериментов по изучению взаимопревращения различных органических кислот и их влияния на дыхание летательной мышцы голубя, английский биохимик Г. А. Кребс в 1937 г. предложил схему последовательности окисления ди- и трикарбоновых кислот до С02 через «цикл лимонной кислоты» да счет отнятия водорода. Этот цикл и был назван его именем.
Непосредственно в цикле окисляется не сам пируват, а его производное — ацетил-СоА. Таким образом, первым этапом на пути окислительного расщепления ПВК является процесс образования активного ацетила в ходе окислительного декарбоксилирования. Окислительное декарбоксилирование пирувата осуществляется при участии пируватдегидрогеназного мультиферментного комплекса. В состав его входят три фермента и пять коферментов. Коферментами служат тиаминпирофосфат (ТПФ) — фосфорилированное производное витамина Вь липоевая кислота, коэнзим A, ФАД и НАД+. Пируват взаимодействует с ТПФ (декарбоксилазой), при этом отщепляется С02 и образуется гидроксиэтильное производное ТПФ (рис. 3). Последнее вступает в реакцию с окисленной формой липоевой кислоты. Дисульфидная связь липоевой кислоты разрывается и происходит окислительно-восстановительная реакция: гидроксиэтильная группа, присоединенная к одному атому серы, окисляется в ацетильную (при этом возникает высокоэнергетическая тиоэфирная связь), а другой атом серы липоевой кислоты восстанавливается. Образовавшаяся ацетиллипоевая кислота взаимодействует с коэнзимом А, возникают ацетил- СоА и восстановленная форма липоевой кислоты. Водород липоевой кислоты переносится затем на ФАД и далее на НАД + . В результате окислительного декарбоксилирования пирувата образуются ацетил-СоА, С02 и НАДH.
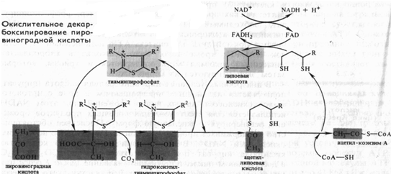
Рис. 3. Окислительное декарбоксилирование ПВК
Дальнейшее окисление ацетил-СоА осуществляется в ходе циклического процесса.
Цикл Кребса начинается с взаимодействия ацетил-СоА с енольной формой щавелевоуксусной кислоты. В этой реакции под действием фермента цитратсинтазы образуется лимонная кислота (2). Следующий этап цикла включает две реакции и катализируется ферментом аконитазой, или аконитатгидратазой (3). В первой реакции в результате дегидратации лимонной кислоты образуется цис-аконитовая. Во второй реакции аконитат гидратируется и синтезируется изолимонная кислота. Изолимонная кислота под действием НАД- или НАДФ-зависимой изоцитратдегидрогеназы (4) окисляется в нестойкое соединение — щавелевоянтарную кислоту, которая тут же декарбоксилируется с образованием α-кетоглутаровой кислоты (α-оксоглутаровой кислоты).
α-Кетоглутарат, подобно пирувату, подвергается реакции окислительного декарбоксилирования. α-Кетоглутаратдегидрогеназный мультиэнзимный комплекс (5) сходен с рассмотренным выше пируватдегидрогеназным комплексом. В ходе реакции окислительного декарбоксилирования α-кетоглутарата выделяется С02, образуются НАДH и сукцинил-СоА.
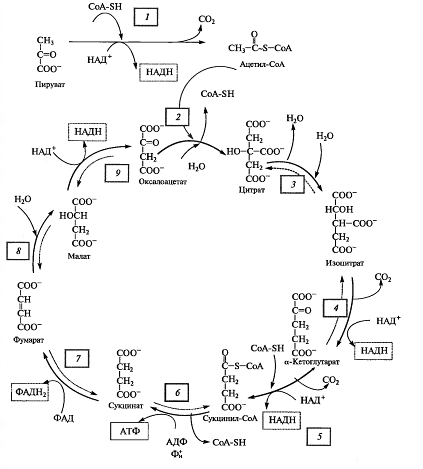
Рис. 4. Цикл Кребса
Подобно ацетил-СоА, сукцинил-СоА является высокоэнергетическим тиоэфиром. Однако если в случае с ацетил-СоА энергия тиоэфирной связи расходуется на синтез лимонной кислоты, энергия сукцинил-CoA может трансформироватся в образование фосфатной связи АТФ. При участии сукцинил- СоА-синтетазы (6) из сукцинил-СоА, АДФ и Н3Р04 образуются янтарная кислота (сукцинат), АТФ, регенерирует молекула СоА. АТФ образуется в результате субстратного фосфорилирования.
На следующем этапе янтарная кислота окисляется до фумаровой. Реакция катализируется сукцинатдегидрогеназой (7), коферментом которой является ФАД. Фумаровая кислота под действием фумаразы или фумаратгидратазы (8), присоединяя Н20, превращается в яблочную кислоту (малат). И, наконец, на последнем этапе цикла яблочная кислота с помощью НАД- зависимой малатдегидрогеназы (9) окисляется в щавелевоуксусную. ЩУК, которая самопроизвольно переходит в енольную форму, реагирует с очередной молекулой ацетил-СоА и цикл повторяется снова.
Следует отметить, что большинство реакций цикла обратимы, однако ход цикла в целом практически необратим. Причина этого в том, что в цикле есть две сильно экзергонические реакции — цитратсинтазная и сукцинил-СоА-синтетазная.
На протяжении одного оборота цикла при окислении пирувата происходит выделение трех молекул С02, включение трех молекул Н2О и удаление пяти пар атомов водорода. Роль Н2О в цикле Кребса подтверждает правильность уравнения Палладина, который постулировал, что дыхание идет с участием Н2О, кислород которой включается в окисляемый субстрат, а водород с помощью «дыхательных пигментов» (по современным представлениям — коферментов дегидрогеназ) переносится на кислород .
Выше отмечалось, что цикл Кребса был открыт на животных объектах. Существование его у растений впервые доказал английский исследователь А. Чибнелл (1939). В растительных тканях содержатся все кислоты, участвующие в цикле; обнаружены все ферменты, катализирующие превращение этих кислот; показано, что малонат — ингибитор сункцинатдегидрогеназы — тормозит окисление пирувата и резко снижает поглощение 02 в процессах дыхания у растений. Большинство ферментов цикла Кребса локализовано в мАТФиксе митохондрий, аконитаза и сукцинатдегидрогеназа — во внутренней мембране митохондрии.
Энергетический выход цикла Кребса, его связь с азотным обменом. Цикл Кребса. играет чрезвычайно важную роль в обмене веществ растительного организма. Он служит конечным этапом окисления не только углеводов, но также белков, жиров и других соединений. В ходе реакций цикла освобождается основное количество энергии, содержащейся в окисляемом субстрате, причем большая часть этой энергии не теряется для организма, а утилизируется при образовании высокоэнергетических конечных фосфатных связей АТФ.
Каков же энергетический выход цикла Кребса? В ходе окисления пирувата имеют место 5 дегидрирований, при этом получаются 3НАДH, НАДФH (в случае изоцитратдегидрогеназы) и ФАДH2. Окисление каждой молекулы НАДH (НАДФH) при участии компонентов электронтранспортной цепи митохондрий дает по 3 молекулы АТФ, а окисление ФАДH2 — 2АТФ. Таким образом при полном окислении пирувата образуются 14 молекул АТФ. Кроме того, 1 молекула АТФ синтезируется ; в цикле Кребса в ходе субстратного фосфорилирования. Следовательно, при окислении одной молекулы пирувата может образоваться 15 молекул АТФ. А поскольку в процессе гликолиза из молекулы глюкозы возникают две молекулы пирувата, их окисление даст 30 молекул АТФ.
Итак, при окислении глюкозы в процессе дыхания при функционировании гликолиза и цикла Кребса в общей сложности образуются 38 молекул АТФ (8 АТФ связаны с глико- лизом). Если принять, что энергия третьей сложноэфирнои фосфатной связи АТФ равняется 41,87 кДж/моль (10 ккал/моль), то энергетический выход гликолитического пути аэробного дыхания составляет 1591 кДж/моль (380 ккал/моль).
Значение цикла Кребса не ограничивается его вкладом в энергетический обмен клетки. Не менее важную роль играет то обстоятельство, что многие промежуточные продукты цикла используются при синтезе различных соединений. Из кетокислот в ходе реакций переаминирования образуются аминокислоты. Для синтеза липидов, полиизопренов, углеводов и ряда других соединений используется ацетил-СоА.
Регуляция цикла Кребса. Дальнейшее использование образующегося из пирувата ацетил-СоА зависит от энергетического состояния клетки. При малой энергетической потребности клетки дыхательным контролем тормозится работа дыхательной цепи, а следовательно, реакций ЦТК и образования интермедиатов цикла, в том числе оксалоацетата, вовлекающего ацетил-СоА в цикл Кребса. Это приводит к большему использованию ацетил-СоА в синтетических процессах, которые также потребляют энергию.
Особенностью регуляции ЦТК является зависимость всех четырех дегидрогеназ цикла (изоцитратдегидрогеназы, α-кетоглутаратдегидрогеназы, сукцинатдегидрогеназы, малатдегидрогеназы) от отношения [НАДH]/[НАД+]. Активность цитратсинтазы тормозится высокой концентрацией АТФ и собственным продуктом — цитратом. Изоцитратдегидрогеназа ингибируется НАДH и активируется цитратом. α-Кето- глутаратдегидрогеназа подавляется продуктом реакции — сукцинил-СоА и активируется аденилатами. Окисление сукцината сукцинатдегидрогеназой тормозится оксалоацетатом и ускоряется АТФ, АДФ и восстановленным убихиноном (QH2). Наконец, малатдегидрогеназа ингибируется оксалоацетатом и у ряда объектов — высоким уровнем АТФ. Однако степень участия величины энергетического заряда, или уровня адениновых нуклеотидов, в регуляции активности цикла Кребса у растений до конца не выяснена.
Регулирующую роль может играть также альтернативный путь транспорта электронов в растительных митохондриях. В условиях высокого содержания АТФ, когда активность основной дыхательной цепи снижена, окисление субстратов через альтернативную оксидазу (без образования АТФ) продолжается, что поддерживает на низком уровне отношение НАДH/НАД+ и снижает уровень АТФ. Все это позволяет циклу Кребса функционировать.
4.2 Пентозофосфатный путь. Механизмы регуляции цикла. Энергетическая эффективность процесса, значение. Связь с другими процессами
В клетках растений наряду с гликолизом и циклом Кребса, являющимся главным поставщиком свободной энергии в процессах дыхания, существует и другой важнейший способ катаболизма гексоз — пентозофосфатный путь (ПФП), в котором участвуют пятиуглеродные сахара (пентозы). Этот путь дыхания известен также как гексозомонофосфатный цикл, пентозный шунт или апотомическое окисление. Окисление глюкозы (глюкозо-6-фосфата) по этому пути связано с отщеплением первого (альдегидного) атома углерода в виде С02 (отсюда и название — апотомический путь).
Пентозофосфатный путь дыхания открыт в 1935—1938 гг. в результате исследований О. Варбурга, Ф. Диккенса, В. А. Энгельгардта и позднее Ф. Липмана. Установлено, что все реакции ПФП протекают в растворимой части цитоплазмы клетки, а также в пропластидах и хлоропластах. ПФП дыхания особенно активен в тех клетках и тканях растений, в которых интенсивно идут синтетические процессы, такие, как синтез липидных компонентов мембран, нуклеиновых кислот, клеточных стенок, фенольных соединений.
В ПФП АТФ используется только для образования исходного продукта. ПФП, как и цикл Кребса, — циклический процесс, поскольку окисление глюкозы сопровождается регенерацией исходного субстрата ПФП — глюкозо-6-фосфата.
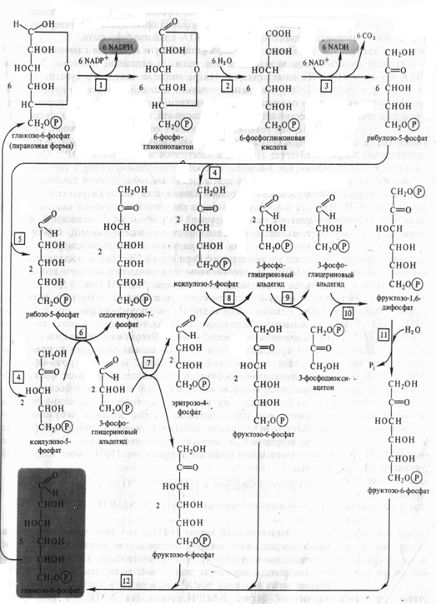
Рис. 5. Пентозофосфатный цикл
Этапы пентозофосфатного пути окисления глюкозы. В ПФП можно выделить два этапа: 1) окисление глюкозы, 2) рекомбинацию Сахаров для регенерации исходного субстрата.
Первый, окислительный, этап апотомического пути включает последовательные реакции, катализируемые дегидрогеназнодекарбоксилрующей системой, состоящей из трех ферментов. Первая реакция представляет собой Дегидрирование глюкозо- 6-фосфата глюкозо-6-фосфатдегидрогеназой (1). Этот фермент в качестве акцептора электронов использует НАДФ+. Он дегидрирует 1-й атом углерода глюкозо-6-фосфата с образованием лактона 6-фосфоглюконовой кислоты. Лактон самопроизвольно или под действием глюконолактоназы (2) гидролизуется, образуя 6-фосфоглюконовую кислоту. В следующей окислительной реакции, катализируемой НАДФ- и Мп2 +-зависимой фосфо- глюконатдегидрогеназой (3) (декарбоксилирующей), 6-фосфоглюконовая кислота дегидрируется и декарбоксилируется. В результате образуются рибулозо-5-фосфат и восстановленный НАДФH. Таким образом, при окислении каждого атома углерода образуются две молекулы НАДФH (рис. 5).
Второй этап связан с регенерацией исходного метаболита — глюкозо-6-фосфата. Из рибулозо-5-фосфата под действием эпимеразы (4) образуется ксилулозо-5-фосфат, а под действием изомеразы (5) — рибозо-5-фосфат. Рекомбинации сахаров с участием транскетолазы (6,8) и трансальдолазы (7) приводят к появлению 3-ФГА и седогептулозо-7-фосфата, затем эритрозо-4-фосфата (7) и фруктозо-6-фосфата(8); в результате образуются фруктозо-6- фосфаты, которые изомеризуются в глюкозо-6-фосфат (12).
Как видно из рис.5, 6 молекул глюкозо-6-фосфата, участвуя в ПФП дыхания, дают 6 молекул рибулозо-5-фосфата и 6С02, после чего из 6 молекул рибулозо-5-фосфата регенерируют 5 молекул глюкозо-6-фосфата. Для каждого оборота цикла суммарное уравнение ПФП имеет следующий вид:
6 Глюкозо-6-фосфат + 12НАДФ + + 7Н20 -->5Глюкозо-6-фосфат + 6С02 + 12НАДФH + 12Н+ + Н3Р04
Энергетический выход ПФП и его роль в обмене веществ.
Универсальным донором водорода для электронтранспортной цепи дыхания служит НАДH, содержание которого в растительных тканях всегда значительно выше, чем НАДФH. В нормальных условиях НАДФ+ находится в клетках в восстановленной форме НАДФH, тогда как НАД+ — в окисленной. Доказано, что НАДФH окисляется медленнее, чем НАДH. Если при окислении субстрата образуется НАДФH, как, например, при апотомическом окислении глюкозо-6-фосфата, то атомы водорода перед поступлением в электронтранспортную цепь должны быть переданы на. НАД+ (трансгидрогеназцая реакция). Если бы все 12 пар протонов от НАДФH, которые образуются при полном окислении молекулы глюкозо-6-фосфата по ПФП, были бы переданы через ЭТЦ на 02, то получилось бы 3 АТФ х 12 = 36 АТФ, что составляет 41,868 кДж х х 36 = 1507 кДж/моль. Практически это не уступает энергетическому выходу дихотомического пути дыхания (гликолиз и цикл Кребса), в котором образуется 1591 кДж/моль (38 АТФ,)1
Однако основное назначение ПФП состоит в участии не столько в энергетическом, сколько в пластическом обмене клеток. Это участие в пластическом обмене включает несколько аспектов:
1. НАДФH используется главным образом в различных синтетических реакциях.
2.В ходе пентозофосфатного цикла синтезируются пентозы, входящие в состав нуклеиновых кислот и различных нуклеотидов (пиридиновых, флавиновых, адениловых и др.). Для животных и других гетеротрофных организмов ПФП — единственный способ образования пентоз (рибоз и дезоксирибоз) в клетке. Рибозы необходимы для синтеза АТФ, GTP, UTP и других нуклеотидов. Коферменты НАД+, НАДФ+, ФАД, коэнзим А — тоже нуклеотиды и в их состав входит рибоза.
3.ПФП имеет большое значение как источник образования углеводов с различным числом углеродных атомов в цепи (от С3 до Су). Эритрозо-4-фосфат, возникающий в ПФП, необходим для синтеза шикимовой кислоты — предшественника многих ароматических соединений, таких, как ароматические аминокислоты, витамины, дубильные и ростовые вещества, лигнин клеточных стенок и др.
4.Компоненты ПФП (рибулозо-1,5-дифосфат, НАДФH) принимают участие в темновой фиксации С02. По существу, ПФП представляет собой обращенный фотосинтетический (восстановительный) цикл Кальвина. Только две из 15 реакций цикла Кальвина специфичны для фотосинтеза, остальные участвуют в окислительном ПФП дыхания и гликолизе.
В хлоропластах окислительный ПФП функционирует в темноте, предотвращая резкое изменение концентрации НАДФH в отсутствие света. Кроме того, триозофосфаты этого цикла в хлоропластах превращаются в 3-ФГК, что важно для поддержания в них уровня АТФ в темноте.
Окисление глюкозы по ПФП осуществляется в результате 12 реакций, тогда как в дихотомический (гликолитический) путь через ПВК и далее через цикл ди- и трикарбоновых кислот включаются более 30 различных реакций.
Не следует, однако, думать, что окисление глюкозо-6-фосфата по схеме, представленной на рис. 5, идет во всех клетках до конца. Очень часто на одном из этапов ПФП переходит в гликолитический. Таким этапом может быть, в частности, транскетолазная реакция (рис. 5, реакция 8), в результате которой ксилулозо-5-фосфат и эритрозо-4-фосфат превращаются во фруктозо-6-фосфат и 3-ФГА — субстраты, общие для гликолиза и ПФП.
4.3 Глиоксилатный цикл. Механизмы регуляции цикла. Энергетическая эффективность процесса, значение
Этот цикл в 1957 г. был впервые описан у бактерий и плесневых грибов Г. Л. Корнбергом и Г. А. Кребсом. Затем оказалось; что он активно функционирует в про- растающих семенах масличных растений и в других растительных объектах, где запасные жиры превращаются в сахара (глюконеогенез). Глиоксилатный цикл локализован не в митохондриях, как цикл Кребса, а в специализированных микротелах — глиоксисомах. В клетках животных этот цикл отсутствует.
В глиоксилатном цикле из ЩУК и ацетил-СоА синтезируется лимонная кислота, образуются цис-аконитовая и изолимонная (изоцитрат), как и в цикле Кребса . Затем изолимонная кислота под действием изоцитрат-лиазы распадается на глиоксиловую и янтарную кислоты. Глиоксилат с участием малатсинтазы взаимодействует со второй молекулой ацетил-СоА, в результате чего синтезируется яблочная кислота, которая окисляется до ЩУК.
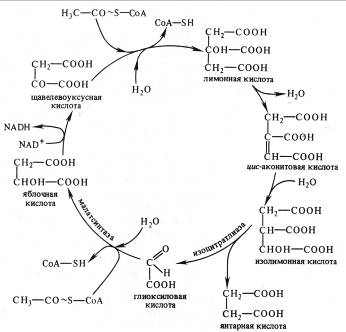
Рис. 6. Глиоксилатный цикл
Таким образом, в отличие от цикла Кребса в глиоксилатном цикле в каждом обороте участвует не одна, а две молекулы ацетил-СоА и этот активированный ацетил используется не для окисления, а для синтеза янтарной кислоты. Янтарная кислота выходит из глиоксисом, превращается в ЩУК и участвует, в глюконеогенезе (обращенном гликолизе) и других процессах биосинтеза. Глиоксилатный цикл позволяет утилизировать запасные жиры, при распаде которых образуются молекулы ацетил-СоА.
Регуляция ПФП и глиоксилатного цикла. Пентозофосфатный путь окисления регулируется концентрацией НАДФ + , так как содержит две НАДФ-зависимые дегидрогеназы (глюкозо-6- фосфатдегидрогеназу и 6-фосфоглюконатдегидрогеназу). Он регулируется также уровнем синтезов в клетке, потребляющих НАДФH (например, синтезом аминокислот и белков). Их высокий уровень приводит к увеличению содержания окисленного НАДФ + , что стимулирует ПФП.
В регуляции соотношения между ПФП и гликолизом принимает участие ряд интермедиатов: неорганический фосфат, 6-фосфоглюконовая кислота, эритрозо-4-фосфат. Недостаток неорганического фосфата подавляет гликолиз и активирует ПФП. 6-Фосфоглюконовая кислота служит ингибитором гликолитического фермента фосфофруктокиназы (глюкозофосфатизомеразы), что способствует функционированию ПФП. Эритрозо-4-фосфат, являясь субстратом транскетолазной и трансальдолазной реакций, может тормозить активность ферментов гликолиза и тем самым переключать превращения углеводов с гликолитического на пентозофосфатный путь.
Активность глиоксилатного цикла снижается при повышении концентрации оксалоацетата, который ингибирует сукцинатдегидрогеназу ЦТК. Другой ингибитор цикла — фосфоенолпируват подавляет активность изоцитратлиазы.
5. Цепь переноса водорода и электрона (дыхательная цепь). Комплексы переноса электронов. Окислительное фосфорилирование. Хемиосмотическая теория окисления и фосфорилирования. Механизмы сопряжения процесса транспорта электронов с образованием АТФ
Цикл Кребса, глиоксилатный и пентозофосфатный пути функционируют только в условиях достаточного количества кислорода. В то же время 02 непосредственно не участвует в реакциях этих циклов. Точно так же в перечисленных циклах не синтезируется АТФ (за исключением АТФ, образующегося в цикле Кребса в результате субстратного фосфорилирования на уровне сукцинил-СоА).
Кислород необходим для заключительного этапа дыхательного процесса, связанного с окислением восстановленных коферментов НАДH и ФАДH2 в дыхательной электронтранспортной цепи (ЭТЦ) митохондрий. С переносом электронов по ЭТЦ сопряжен и синтез АТФ.
Дыхательная ЭТЦ, локализованная во внутренней мембране митохондрий, служит для передачи электронов от восстановленных субстратов на кислород, что сопровождается трансмембранным переносом ионов Н + . Таким образом, ЭТЦ митохондрий (как и тилакоидов) выполняет функцию окислительно-восстановительнои Н -помпы. ,
Б. Чане и др. (США) в 50-х годах, используя значения окислительно-восстановительных потенциалов известных в то время переносчиков е-, спектрофотометрические данные о временной последовательности их восстановления и результаты ингибиторного анализа, расположили компоненты ЭТЦ митохондрий в следующем порядке:
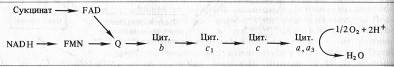
Пара электронов от НАДH или сукцината передается по ЭТЦ до кислорода, который, восстанавливаясь и присоединяя два протона, образует воду.
Д. Грин (1961) пришел к выводу, что все переносчики электронов в митохондриальной мембране сгруппированы в четыре комплексу, что было подтверждёно дальнейшими исследованиями.
Согласно современным данным дыхательная цепь митохондрий включает в себя четыре основных мультиэнзимных комплекса и два небольших по молекулярной массе компонента — убихинон и цитохром с
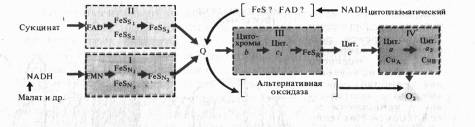
Рис.7. Дыхательная электронтранспортная цепь растительных митохондрий
Комплекс I осуществляет перенос электронов от НАДH к убихинону Q. Его субстратом служат молекулы вдутримитохондриального НАДH, восстанавливающиеся в цикле Кребса. Всостав комплекса входит флавиновая ФМН-зависимая НАДH: убихи- нон-оксидоредуктаза, содержащая три железосерных центра (FeSN1-3). При встраивании в искусственную фосфолипидную мембрану этот комплекс функционирует как протонная помпа.
Комплекс II катализирует окисление сукцината убихиноном. Эту функцию осуществляют флавиновая (ФАД-зависимая) сукцинат : убихинон-оксидоредуктаза, в состав которой также входят три железосерных центра (Fes1_3).
Koмплекс III переносит электроны от восстановленного убихинона к цитохрому с, т. е. функционирует как убихинол: цитохром Т-оксидредуктаза. В своем составе он содержит цитохромы b556 и b560, цитохром с, и железосерный белок Риске. По структуре и функции этот комплекс сходен с цитохромным комплексом b6 — f тилакоидов хлоропластов. В присутствии убихинона комплекс III осуществляет активный трансмембранный перенос протонов.
В терминальном комплексе IV электроны переносятся от цитохрома с к кислороду. _т. е. этот комплекс является цитохромом с: кислород-оксидоредуктазой (цитохромоксидазой). В его состав входят четыре редокс-компонента: цитохромы а и а3 и два атома меди. Цитохром а3 и Сив способны взаимодействовать с 02, на который передаются электроны с цитохрома а — СиА. Транспорт электронов через комплекс IV сопряжен с активным транспортом ионов Н +.
В последние годы в результате изучения пространственного расположения компонентов ЭТЦ во внутренней мембране митохондрии показано что комплексы I, III и IV пересекают мембрану. На внутренней стороне мембраны, обращенной к матриксу, два электрона и два протона от НАДH поступают на флавинмононуклеотид комплекса I.
Электроны передаются на FeS-центры. Пара электронов от FeS-центров захватывается двумя молекулами окисленного убихинона, которые принимают два иона Н + , образуя семихиноны (2QH) и диффундируя к комплексу III. На эти семихиноны поступает еще пара электронов от цитохрома Ь560 комплекса III, что делает возможной реакцию семихинонов с еще двумя протонами из мАТФикса с образованием 2QH2. Полностью восстановленный убихинон (убихинол) отдает 2е~ цитохрому Ь556 и 2е~ FeSR — цитохрому с,. В результате освобождаются четыре иона Н+, выходящие в межмембранное пространство митохондрии. Окисленные молекулы убихинона вновь диффундируют к комплексу I и готовы принимать от него (или от комплекса II) новые электроны и протоны. Таким образом, цитохромы Ь служат донорами двух электронов для переноса двух дополнительных протонов через липидную фазу мембраны на каждые два электрона, поступающие из комплекса I.
Водорастворимый цитохром с на наружной стороне мембраны, получив 2е~ от FeSR — цитохрома ciy передает их на цитохром а — Сид комплекса IV. Цитохром а3 — Сив, связывая кислород, переносит на него эти электроны, в результате чего с участием двух протонов образуется вода. Как уже отмечалось, цитохромоксидазный комплекс способен также переносить ионы Н+ через митохондриальную мембрану.
Таким образом, из матрикса митохондрии при транспорте каждой пары электронов от НАДH к 1/2 02 в трех участках ЭТЦ (комплексы I, III, IV) через мембрану наружу переносятся по крайней мере шесть протонов. Как будет показано далее, именно в этих трех участках окислительные процессы в ЭТЦ сопрягаются с синтезом АТФ. Передача 2е~ от сукцината на убихинон в комплексе II не сопровождается трансмембранным переносом протонов. Это приводит к тому, что при использовании сукцината в качестве дыхательного субстрата в ЭТЦ остаются лишь два участка, в которых функционирует протонная помпа.
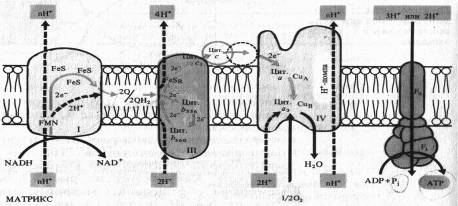
Рис. 8. Предполагаемое расположение компонентов цепи переноса электронов во внутренней мембране митохондрий в соответствии с хемиосинтетической теорией Митчелла
Особенностью растительных митохондрий (отличающей их от митохондрий животных) является способность окислять экзогенный НАДH, т. е. НАДH, поступающий из цитоплазмы. Это окисление осуществляется по крайней мере двумя флавиновыми НАДH-дегидрогеназами, из которых одна локализована на наружной стороне внутренней мембраны митохондрий, а другая — в их наружной мембране. Первая из них передает электроны в ЭТЦ митохондрий на убихинон, а вторая — на цитохром с. Для функционирования НАДH- дегидрогенэзы на наружной стороне внутренней мембраны необходимо присутствие кальция.
Другое существенное отличие растительных митохондрий состоит в том, что во внутренней мембране помимо основного (цитохромного) пути переноса электронов имеется альтернативный путь переноса е~, устойчивый к действию цианида.
Перенос электронов от НАДH к молекулярному кислороду через ЭТЦ митохондрий сопровождается потерей свободной энергии. Какова судьба этой энергии? Еще в 1931 г. В. А. Энгельгардт показал, что при аэробном дыхании накапливается АТФ. Он первый высказал идею о сопряжении между фосфорилированием АДФ и аэробным дыханием. В 1937—1939 гг. биохимики В. А. Белицер в СССР и Г. Калькар в США установили, что при окислении промежуточных продуктов цикла Кребса, в частности янтарной и лимонной кислот, суспензиями животных тканей исчезает неорганический фосфат и образуется АТФ. В анаэробных условиях или при подавлении дыхания цианидом такого фосфорилирования не происходит. Процесс фосфорилирования АДФ с образованием АТФ, сопряженный с переносом электронов по ЭТЦ митохондрий, получил название окислительного фосфорилирования.
По поводу механизма окислительного фосфорилирования существуют три теории: химическая, механохимическая (конформационная) и хемиосмотическая.
Химическая и механохимическая гипотезы сопряжения. Согласно химической гипотезе в митохондриях имеются интермедиаторы белковой природы (X, Y, Z), образующие комплексы с соответствующими восстановленными переносчиками. В результате окисления переносчика в комплексе возникает высокоэнергетическая связь. При распаде комплекса к интермедиатору с высокоэнергетической связью присоединяется неорганический фосфат, который затем передается на АДФ:
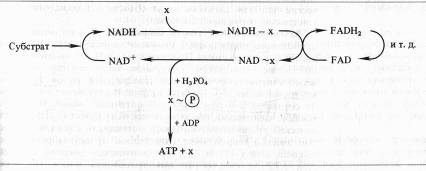
Однако несмотря на упорные поиски, не удалось выделить или как-то иначе доказать реальное существование постулированных высокоэнергетических интермедиаторов типа X ~ P. Гипотеза химического сопряжения не объясняет, почему окислительное фосфорилирование обнаруживается только в препаратах митохондрий с ненарушенными мембранами. И, наконец, с позиций этой гипотезы не находит объяснения способность митохондрий подкислять внешнюю среду и изменять свой объем в зависимости от степени их энергизации.
Способность митохондриальных мембран к конформационным изменениям и связь этих изменений со степенью энергизации митохондрий послужила основой для создания механохимических гипотез образования АТФ в ходе окислительного фосфорилирования. Согласно этим гипотезам энергия, высвобождающаяся в процессе переноса электронов, непосредственно используется для перевода белков внутренней мембраны митохондрий в новое, богатое энергией конформационное состояние, приводящее к образованию АТФ. Одна из гипотез подобного рода, выдвинутая американским биохимиком П. Д. Бойером (1965), может быть представлена в виде следующей схемы:
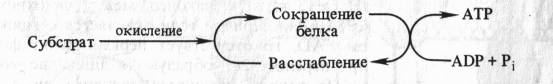
Автор предположил, что запасание энергии происходит путем конформационных изменений ферментов ЭТЦ аналогично тому, как это наблюдается в белках мышц. Актомиозиновый комплекс сокращается, гидролизуя АТФ. Если сокращение белкового комплекса достигается за счет другой формы энергии (за счет окисления), то расслабление, возможно, будет сопровождаться синтезом АТФ.
Таким образом, согласно механохимическим гипотезам, энергия окисления превращается сначала в механическую энергию, а затем в энергию высокоэнергетической связи АТФ. Однако, подобно химической теории сопряжения, механохимические гипотезы также не могут объяснить подкисление митохондриями окружающей среды.
Хемиосмотическая теория сопряжения. В настоящее время наибольшим признанием пользуется хемиосмотическая теория английского биохимика П. Митчелла (1961). Он высказал предположение, что поток электронов через систему молекул-переносчиков сопровождается транспортом ионов Н+ через внутреннюю мембрану митохондрий. В результате на мембране создается электрохимический потенциал ионов Н + , включающий химический, или осмотический, градиент и электрический градиент (мембранный потенциал). Согласно хемиосмотической теории электрохимический трансмембранный потенциал ионов Н+ и является источником энергии для синтеза АТФ за счет обращения транспорта ионов Н+ через протонный канал мембранной Н + -АТФазы.
Теория Митчелла исходит из того, что переносчики перешнуровывают мембрану, чередуясь таким образом, что в од сторону возможен перенос и электронов, и протонов, а в об ратную — только электронов. В результате ионы Н+ накапливаются на одной стороне мембраны.
Между двумя сторонами внутренней митохондриальной мембраны в результате направленного движения протонов против концентрационного градиента возникает электрохимический потенциала Энергия, запасенная таким образом, используется для синтеза АТФ как результат разрядки мембраны при обратном (по концентрационному градиенту) транспорте протонов через АТФазу, которая работает в этом случае как АТФ-синтетаза.
За прошедший период хемиосмотическая гипотеза Митчелла получила целый ряд экспериментальных подтверждений. Одним из доказательств роли протонного градиента в образовании АТФ при окислительном фосфорилировании может служить разобщающее действие на этот процесс некоторых веществ. Известно, что 2,4-динитрофенол (2,4-ДНФ) подавляет синтез АТФ, но стимулирует транспорт электронов (поглощение 02), т. е. разобщает дыхание (окисление) и фосфорилирование. Митчелл предположил, что такое действие 2,4-ДНФ связано с тем, что он переносит протоны через мембрану (т. е. является протонофором) и поэтому разряжает ее. Это предположение полностью подтвердилось. Оказалось, что разные по своей химической природе вещества, разобщающие окисление и фосфорилирование, сходны в том, что, во-первых, они растворимы в липидной фазе мембраны, а, во-вторых, это слабые кислоты, т. е. легко приобретают и теряют протон в зависимости от рН среды. В. П. Скулачев на искусственных фосфолипидных мембранах показал, что чем легче вещество переносит протоны через мембрану, тем сильнее разобщает эти процессы. Другое экспериментальное подтверждение роли протонного градиента в фосфорилировании было получено Митчеллом, который сообщил о синтезе АТФ в митохондриях в результате замены щелочной инкубационной среды на кислую (т. е. в условиях искусственно созданного трансмембранного градиента ионов Н+).
В 1973 г. Э. Рэкеру (США) удалось получить липосомы (везикулы из фосфолипидов), в которые была встроена АТФаза, выделенная из митохондрий сердца быка, и хромопротеин галофильной бактерии Halobacterium halobium — бактериородопсин, обусловливающий создание протонного градиента за счет энергии света. Фосфолипиды для реконструкции мембран этих липосом были выделены из растений (соевые бобы). Полученные таким образом гибридные пузырьки на свету осуществляли фосфорилирование.
6.АТФ как основная энергетическая валюта клетки, её структура и функции. Механизмы синтеза АТФ
Процессы обмена вещества включают в себя реакции, идущие с потреблением энергии, и реакции с выделением энергии. В некоторых случаях эти реакции сопряжены. Однако часто реакции, в которых энергия выделяется, отделены в пространстве и во времени от реакций, в которых она потребляется. В процессе эволюции у растительных и животных организмов выработалась возможность хранения энергии в форме соединений, обладающих богатыми энергией-связями. Среди них центральное место занимает аденозинтрифосфат (АТФ). АТФ представляет собой нуклеотидфосфат, состоящий из азотистого основания (аденина), пентозы (рибозы) и трех молекул фосфорной кислоты. Две концевые молекулы фосфорной кислоты образуют макроэргические, богатые энергией связи. В клетке АТФ содержится главным образом в виде комплекса с ионами магния. Аденозинтрифосфат в процессе дыхания образуется из аденозиндифосфата и остатка неорганической фосфорной кислоты (Фн) с использованием энергии, освобождающейся при окислении различных органических веществ:
АДФ + ФН --> АТФ + Н2О
При этом энергия окисления органических соединении превращается в энергию фосфорной связи.
В 1939—1940 гг. Ф. Липман установил, что АТФ служит главным нереносчиком энергии в клетке. Особые свойства этого вещества определяются тем, что конечная фосфатная группа легко переноситься с АТФ на другие соединения или отщепляется с выделением энергии, которая может быть использована на физиологические функции. Эта энергия представляет собой разность между свободной энергией АТФ и свободной энергией образующихся продуктов (AG). AG — это изменение свободной энергии системы или количество избыточной энергии, которая освобождается при реорганизации химических связей. Распад АТФ происходит по уравнению AТФ + Н20 = АДФ + ФН, при этом происходит как бы разрядка аккумулятора, при рН 7 выделяется AG = —30,6 кДж. Этот процесс катализируется ферментом аденозинтрифосфатазой - (АТФ-аза) Равновесие гидролиза АТФ смещено в сторону завершения peaкции, что и обусловливает большую отрицательную величину свободной энергии гидролиза. Это связано с тем, что при диссоциации. Четырех гидроксильных группировок при рН 7 АТФ имеет четыре отрицательных заряда. Близкое расположение зарядов друг к другу способствует их отталкиванию и, следовательно, отщеплению фосфатных группировок. В результате гидролиза образуются соединения с одноименным зарядом (АДФ3~ и НР04~), которые отживаются друг от друга, что препятствует их соединению. Уникальные свойства АТФ объясняются не только тем, что при ее гидролизе выделяется большое количество энергии, но и тем, что она обладает способностью отдавать концевую фосфатную группу вместе с запасом энергии на другие органические соединения. Энергия, заключенная в макроэргической фосфорной связи, используется на физиологическую деятельность клетки. Вместе с тем по величине свободной энергии гидролиза — 30,6 кДж/моль АТФ занимает промежуточное положение. Благодаря этому система АТФ — АДФ может служить носчиком фосфатных групп от фосфорных соединений с более высокой энергией гидролиза, например фосфоенолпируват (53,6 К/моль), к соединениям с более низкой энергией гидролиза, пример сахарофосфатам (13,8 кДж/моль). Таким образом, система АДФ является как бы промежуточной или сопрягающей.
Механизм синтеза АТФ. Сопряжение диффузии протонов назад через внутреннюю мембрану митохондрии с синтезом АТФ осуществляется с помощью АТФазного комплекса, получившего название фактора сопряжения F,. На электронно- микроскопических снимках эти факторы выглядят глобулярными образованиями грибовидной формы на внутренней мембране митохондрий, причем их «головки» выступают в матрикс. F1 — водорастворимый белок, состоящий из 9 субъединиц пяти различных типов. Белок представляет собой АТФазу и связан с мембраной через другой белковый комплекс F0, который перешнуровывает мембрану. F0 не проявляет каталитической активности, а служит каналом для транспорта ионов Н+ через мембрану к Fx.
Механизм синтеза АТФ в комплексе Fi~ F0 до конца не выяснен. На этот счет имеется ряд гипотез.
Одна из гипотез, объясняющих образование АТФ посредством так называемого прямого механизма, была предложена Митчеллом.
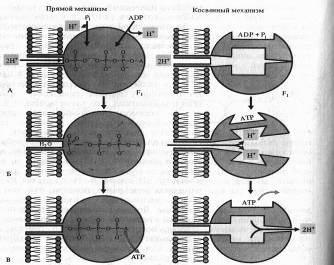
Рис. 9. Возможные механизмы образования АТФ в комплексе F1 – F0
По этой схеме на первом этапе фосфорилирования фосфатный ион и АДФ связываются с г компонентом ферментного комплекса (А). Протоны перемещаются через канал в F0-компоненте и соединяются в фосфате с одним из атомов кислорода, который удаляется в виде молекулы воды (Б). Атом кислорода АДФ соединяется с атомом фосфора, образуя АТФ, после чего молекула АТФ отделяется от фермента (В).
Для косвенного механизма возможны различные варианты. АДФ и неорганический фосфат присоединяются к активному центру фермента без притока, свободной энергии. Ионы Н + , перемещаясь по протонному каналу по градиенту своего электрохимического потенциала, связываются в определенных участках Fb вызывая конформационныё. изменения фермента (П. Бойер), в результате чего из АДФ, и Рi синтезируется АТФ. Выход протонов в матрикс сопровождается возвратом АТФ-синтетазного комплекса в исходное конформационное состояние и освобождением АТФ.
В энергизованном виде F1 функционирует как АТФ-синтетаза. При отсутствии сопряжения между электрохимическим потенциалом ионов Н+ и синтезом АТФ энергия, освобождающаяся в результате обратного транспорта ионов Н+ в матриксе, может превращаться в теплоту. Иногда это приносит пользу, так как повышение температуры в клетках активирует работу ферментов.
7. Митохондрии как органоиды дыхания. Их структура и функции
Митохондрии — «силовые» станции клетки, в них локализована большая часть реакций дыхания (аэробная фаза). В митохондриях происходит аккумуляция энергии дыхания в аденозинтрифосфате (АТФ). Энергия, запасаемая в АТФ, служит основным источником для физиологической деятельности клетки. Митохондрии обычно имеют удлиненную палочковидную форму длиной 4—7 мкм и диаметром 0,5-2 мкм. Число митохондрий в клетке может быть различным, от 500 до 1000. Однако в некоторых организмах (дрожжах) имеется лишь одна гигантская митохондрия. Химический состав митохондрий несколько колеблется. В основном это белковолипоидные органеллы. Содержание белка в них составляет 60—65%. В состав мембран митохондрий входят 50% структурных белков и 50% ферментативных, около 30% липидов. Очень важно, что митохондрии содержат нуклеиновые кислоты: РНК—1% и ДНК—0,5%. В митохондриях имеется не только ДНК, но и вся система синтеза белка, втом числе и рибосомы. Митохондрии окружены двойной мембраной? Толщина мембран составляет 6—10 нм. Между мембранами — перимитохондрлальное пространство, равное 10 нм; оно заполнено жидкостью типа сыворотки. Внутреннее пространство митохондрий заполняет матрикс в виде студнеобразной полужидкой массы. В матриксе сосредоточены ферменты цикла Кребса.
Внутренняя мембрана дает выросты — кристы, расположенные перпендикулярно продольной оси органеллы и перегораживающие все внутреннее пространство митохондрий на отдельные отсеки. Однако, поскольку выросты-перегородки неполные, между этими отсеками сохраняется связь. Мембраны митохондрий обладают большой прочностью и гибкостью. Во внутренней мембране локализована дыхательная цепь (цепь переноса электронов). На внутренней мембране митохондрий расположены грибовидные частицы. Они расположены через правильные промежутки. Каждая митохондрия содержит 104—105 таких грибовидных частиц. Установлено, что в головке грибовидных частиц содержится фермент АТФ-синтетаза, катализирующий образование АТФ аа_счет Энергий, выделяющейся в аэробной фазе дыхания.
Митохондрии способны к движению. Это имеет большое значение в жизни клетки, так как митохондрии передвигаются к тем местам, где идет усиленное потребление энергии. Они могут ассоциировать друг с другом как путем тесного сближения, так и при помощи связующих тяжей. Наблюдаются также контакты митохондрий с эндоплазматической сетью, ядром, хлоропластами. Известно, что митохондрии способны к набуханию, я при потере воды — к сокращению.
В растущих клетках митохондриальный матрикс становится менее плотным, количество крист растет — это коррелирует с увеличением интенсивности дыхания. В процессе дыхания ультраструктура митохондрий меняется. В том случае, если в митохондриях протекает активный процесс преобразования энергии окисления в энергию АТФ, внутренняя часть митохондрий становится более компактной.
Митохондрии имеют свой онтогенез. В меристематических клетках можно наблюдать инициальные частицы, которые представляют собой округлые образования, окруженные двойной мембраной. Диаметр таких инициальных частиц составляет 50 нм. По мере роста клетки инициальные частицы увеличиваются в размере, удлиняются и их внутренняя мембрана образует выросты, перпендикулярные оси митохондрий. Вначале образуются промитохондрии. Они еще не достигают окончательного размера и имеют мало крист. Из промитохондрий образуются митохондрии. Сформировавшиеся митохондрии делятся путем перетяжки или почкованием. Свойства митохондрий (белки, структура) закодированы частично в ДНК митохондрий, а частично в ядре. Сопоставление размеров митохондриальной ДНК с числом и размером митохондриальных белков показывает, что в ней заложено информации почти для половины белков. Это и позволяет считать митохондрии полуавтономными, т. е. не полностью зависящими от ядра. Они имеют собственную ДНК и собственную белоксинтезирующую систему, и именно с ними и с пластидами связана так называемая цитоплазматическая наследственность. В большинстве случаев это наследование по материнской линии, так как инициальные частицы митохондрий локализованы в яйцеклетке. Таким образом, митохондрии всегда от митохондрий.
Широко обсуждается вопрос, как рассматривать митохондрии и хлоропласты с эволюционной точки зрения. Еще в 1921 г. русский ботаник Б. М. Козо-Полянский высказал мнение, что клетка — это симбиотрофная система, в которой сожительствует несколько организмов. В настоящее время эта гипотеза имеет много сторонников. Согласно гипотезе симбиогенеза, митохондрии — это в прошлом самостоятельные организмы. По мнению Марголис, это могли быть эубактерии, содержащие ряд дыхательных ферментов. На определенном этапе эволюции они внедрились в примитивную содержащую ядро клетку. Оказалось, что ДНК митохондрий и хлоропластов по своей структуре резко отличается от ядерной ДНК высших растений и сходна с бактериальной ДНК (кольцевое строение). Сходство обнаруживается и в величине рибосом. Однако доказательств еще недостаточно и окончательного вывода по этому вопросу пока сделать невозможно.
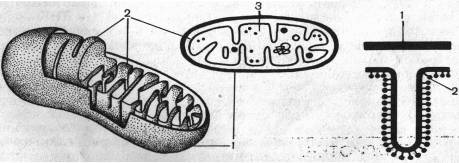
1- наружная мембрана, 2- внутренняя мембрана, 3- матрикс.
Рис. 10. Схема строения митохондрий
8. Генетическая связь дыхания и брожения. Связь дыхания и фотосинтеза. Взаимосвязь дыхания с другими процессами обмена
Соссюр, работая с зелеными растениями в темноте, обнаружил, что они выделяют С02 даже в бескислородной среде. Л. Пастер нашел, что в темноте в отсутствие кислорода в растительных тканях наряду с выделением С02 образуется спирт, т. е. идет спиртовое брожение. Он пришел к выводу, что в растительных тканях, так же как и у бактерий, возможно спиртовое брожение.
Немецкий физиолог Э. Ф. Пфлюгер (1875), изучая дыхание животных объектов, показал, что лягушки, помещенные в среду без кислорода, некоторое время остаются живыми и при этом выделяют С02. Пфлюгер назвал это дыхание интрамолекулярным, т. е. дыханием за счет внутримолекулярного окисления субстрата. Предполагалось, что интрамолекулярное дыхание — начальный этап нормального аэробного дыхания. Эту точку зрения поддержал Б. Пфеффер — немецкий физиолог растений, который распространил ее на растительные организмы. На основе этих работ Пфеффером и Пфлюгером были предложены следующие два уравнения, описывающие механизм дыхания:
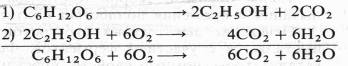
На первом, анаэробном, этапе происходит спиртовое брожение, образуются две молекулы этанола и две молекулы С02. Затем в присутствии кислорода спирт, взаимодействуя с ним, окисляется до С02 и Н20.
С. П. Костычев (1910) пришел к выводу, что это уравнение не соответствует действительности. Он экспериментально доказал, что этанол не может быть промежуточным продуктом нормального аэробного дыхания у растений по двум причинам: во-первых, он ядовит для растений и не может накапливаться, во-вторых, этанол окисляется растительными тканями значительно хуже, чем глюкоза. Костычев предложил свою формулу связи анаэробной и аэробной частей дыхания и различных видов брожения.
В опытах Костычева и его сотрудников (1912—1928) было показано, что если растительные ткани кратковременно выдержать в бескислородной среде, а затем дать кислород, то наблюдается резкое усиление дыхания, т.е. в ходе анаэробной фазы накапливаются промежуточные продукты, которые в присутствии кислорода быстро используются. Ингибиторы, блокирующие брожение, например NaF, блокируют и аэробное дыхание. Ингибиторный анализ (применение ингибиторов специфического действия), выделение и идентификация продуктов окислительного распада глюкозы привели Костычева к выводу о том, что промежуточным продуктом может быть уксусный альдегид. Благодаря работам немецкого биохимика К. Нейберга, Костычева и других стало очевидным, что дыхание и все виды брожения связаны между собой через пировиноградную кислоту (ПВК):
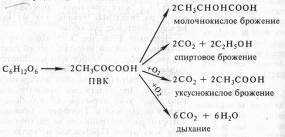
Таким образом, теория Костычева о генетической связи дыхания и брожения полностью подтвердилась.
Взаимосвязь дыхания с другими процессами обмена.
Дыхание тесно связано с другими процессами метаболизма. Необходимо подчеркнуть, что, несмотря на противоположную направленность двух центральных процессов растительного организма —.фотосинтеза и дыхания и на их рассредоточенность в разных органеллах клетки, между ними существует тесная взаимосвязь. Прежде всего для протекания процесса дыхания органические вещества (субстраты). Таким субстратами в первую очередь являются углеводы, которые у зеленых растений образуются в процессе фотосинтеза. Вместе с тем превращение веществ в процессе фотосинтеза и дыхания идет через ряд сходных промежуточных продуктов. Особенно много сходного в превращениях между фотосинтетическим циклом Кальвина и реакциями пентозофосфатного пути дыхательного обмена. Как в том, так и в другом случае происходят взаимные превращения Сахаров с разной длиной углеродной цепочки (3, 4, 5, 6 и 7 углеродных атомов). По-видимому, несмотря на различное распределение (компартментацию) этих метаболитов в клетке, между ними существует обмен. Иначе го вор я, промежуточные. продукты дыхания могут быть использованы в процессе фотосинтеза. Одновременно возможен и обратный процесс. Много общего в энергетике фотосинтеза и дыхания в процессах фотосинтетического и окислительного фосфорилирования. Между этими двумя процессами возможен обмен энергетическими эквивалентами. АТФ, образовавшаяся на свету при фотосинтетическом фосфорилировании, может служить основным источником энергии для различных биосинтетических процессов, заменяя АТФ, образовавшуюся в процессе дыхания. С другой стороны, АТФ и НАДФ-Н, образовавшиеся в процессе дыхания, могут быть использованы для реакций цикла Кальвина. Имеются наблюдения, что на свету основными органеллами, поставляющими АТФ, являются хлоропласты.
Многие промежуточные продукты процесса дыхания являются основой биосинтеза важнейших соединений. Уже на протяжении первой, анаэробной фазы дыхания (гликолиз) триозофосфат, преобразуясь в глицерин, может служить источником для синтеза жиров. Пировиноградная кислота путем аминирования может дать аланин. Не менее важное значение имеют и промежуточные продукты цикла Кребса. Например, α-кетоглютаровая и щавелевоуксусная кислоты в процессе аминирования дают аминокислоты — глутаминовую и аспарагиновую. Благодаря реакции переаминирования эти кислоты могут быть источником аминогруппы для других аминокислот и, таким образом, являться важнейшими промежуточными продуктами для синтеза как белка, так и пуриновых и пиримидиновых азотистых оснований. Янтарная кислота, образовавшаяся в цикле Кребса, дает основу для образования порфиринового ядра хлорофилла. Ацетил-КоА служит основой для образования жирных кислот. Поскольку имеется ряд реакций и процессов, благодаря которым отдельные компоненты извлекаются из цикла Кребса, должны быть и обратные процессы, поставляющие их в цикл. Если бы этого не было, скорость превращения в аэробной фазе дыхания заметно бы снизилось. Такими реакциями является окислительное дезаминирование аминокислот, приводящее к образованию органических кислот. Имеет значение также реакция карбоксилирования пировиноградной кислоты или ее фосфорилированой формы, в результате чего образуется щавелевоуксусная кислота. Основной процесс, при котором образуются пентозы в растении,— то пентозофосфатный путь дыхательного обмена. Пентозы входят в состав нуклеотидов, нуклеиновых кислот и ряда коферментов, в том числе таких важных, как никотинамидные (НАД и НАДФ), флавиновые (ФМН, ФАД). Пентозофосфатный путь дыхания является также источником образования эритрозо-4-фосфата. Эритрозофосфат, взаимодействуя с фосфоенолпируватом, образует шикимовую кислоту. Шикимовая кислота — материал для образования ряда ароматических аминокислот, например триптофана, а из трипсина образуется один из главных гормонов роста растений — ауксин (Р-индолилуксусная кислота).
Рассмотренные связи дыхания и других процессов метаболизма растения не являются постоянными, раз навсегда данными. Они возникают и нарушаются под влиянием как внутренних особенностей растения, так и внешних условий. При неблагоприятных условиях эти нарушения могут быть значительными и даже летальными.
9. Количественные показатели газообмена
Интенсивность дыхания – количество поглощенного кислорода (выделенного углекислого газа) за 1 час 1 граммом растительного материала.
Дыхательный коэффициент - отношение объёма выделяемого из организма углекислого газа к объёму поглощаемого за то же время кислорода. Зависит от химической природы дыхательного субстрата, содержания CO2 и O2 в атмосфере и др. факторов, характеризуя, т. о., специфику и условия дыхания. При использовании клеткой для дыхания углеводов (проростки злаков) ДК равен примерно 1, жиров и белков (прорастающие семена масличных и бобовых) — 0,4—0,7. При недостатке О2 и затруднённом его доступе (семена с твёрдой оболочкой) ДК равен 2—3 и более; высокий ДК характерен также для клеток точек роста.
Р/О – отношение количества образующегося АТФ к количеству поглощенного кислорода за единицу времени единицей растительной массы. Показывает насколько активно идут процессы в ЭТЦ митохондрий, насколько энергетически эффективно дыхание.
10.Регуляция процесса дыхания. Зависимость дыхания от внутренних факторов
Дыхательный контроль. Возрастание функциональной активности клеток сопровождается усилением дыхания. В значительной степени это достигается благодаря механизму дыхательного контроля, или акцепторного контроля дыхания. Дыхательным .контролем называют зависимость скорости потребления 02 митохондриями от концентрации АДФ, который служит акцептором фосфата при окислительном фосфорилировании. В условиях полного сопряжения транспорта электронов по ЭТЦ с синтезом АТФ интенсивность дыхательного процесса в митохондриях зависит от концентрации АДФ или, точнее, от отношения действующих масс АТФ-системы: [ATP]/[АДФ] [PJ. Причем неорганический фосфат обычно присутствует в достаточном количестве и не является ограничивающим фактором. В клетке, находящейся в состоянии покоя, это отношение достаточно велико, так как почти весь АДФ фосфорилирован. При увеличении функциональной активности клеток АТФ расходуется на энергозависимые процессы, в результате чего возрастает концентрация АДФ, а это в свою очередь приводит к повышению скорости переноса электронов и интенсивности окислительного фосфорилирования. Важно подчеркнуть, что в данном случае уровень АДФ регулирует интенсивность транспорта электронов и окислительное фосфорилирование не как аллостерический фактор, а как субстрат фосфорилирования.
Более полно состояние адениннуклеотидной системы выражается отношением, получившим название энергетического заряда:
[АТФ] + у2 [АДФ] [АТФ] + [АДФ] + [AMP] '
который характеризует меру заполнения всей адениннуклеотидной системы высокоэнергетическими фосфатными группами.
Эффект Пастера. Уровень 02 в тканях влияет не только на интенсивность дыхания, но определяет и величину расходования дыхательных субстратов, на что впервые обратил внимание Л.
Пастер. В его опытах с дрожжами в присутствии 02 снижались распад глюкозы и интенсивность брожения (уменьшалось количество спирта и выделяемого С02), но одновременно наблюдался интенсивный рост биомассы дрожжей вследствие усиления использования Сахаров на синтетические процессы. Торможение распада Сахаров и более эффективное их использование в присутствии кислорода получило название «эффекта Пастера».
Механизм эффекта Пастера состоит в том, что в присутствии 02 интенсивно идущий процесс окислительного фосфорилирования конкурентно уменьшает количество молекул АДФ, вступающих в гликолиз (на нужды субстратного фосфорилирования). По этой причине, а также из-за тормозящего действия АТФ (синтез которого резко возрастает в аэробных условиях) на фосфофруктокиназу, скорость процессов гликолиза в присутствии 02 снижается. Избыток АТФ может способствовать и ресинтезу глюкозы из части молекул пирувата, образующегося в ходе гликолиза. Без кислорода не функционируют цикл Кребса и ПФП и, следовательно, клетки не получают многих промежуточных соединений, необходимых для синтеза клеточных структур. В присутствии 02 все эти циклы работают. Увеличение концентрации молекул АТФ в условиях аэробиоза также способствует синтетическим процессам.
Изменение интенсивности дыхания в онтогенезе. У светолюбивых растений более высокая интенсивность дыхания по сравнению с теневыносливыми. Растения северных широт дышат более интенсивно, чем южные, особенно при пониженной температуре. Наиболее высока интенсивность дыхания у молодых активно растущих тканей и органов. После окончания роста дыхание листьев снижается до уровня, равного половине максимального и затем долго не меняется. При пожелтении листьев и в период, предшествующий полному созреванию плодов, у этих органов наблюдается активация синтеза этилена с последующим кратковременным усилением дыхания, которое называют климактерическим подъемом дыхания. Этилен увеличивает проницаемость мембран и гидролиз белков, что приводит к повышению содержания субстратов дыхания. Однако это дыхание не сопровождается образованием АТФ.
11.Зависимость процесса дыхания от факторов внешней среды
Температура. Дыхание у некоторых растений идет и при температуре ниже 0оС. Так, хвоя ели дышит при –25оС. Интенсивность дыхания, как всякой ферментативной реакции, возрастает при повышении температуры до определенного предела (35-40оС).
Кислород необходим для осуществления дыхания, так как он является конечным акцептором электронов в дыхательной электронтранспортной цепи. Увеличение содержания кислорода в воздухе до 8-10 % сопровождается повышением интенсивности дыхания. Дальнейшее увеличение концентрации кислорода существенно не влияет на дыхание. Однако в атмосфере чистого кислорода дыхание растений снижается, а при длительном его действии растение погибает. Гибель растения обусловлена усилением в клетках свободнорадикальных реакций и повреждением мембран вследствие окисления их липидов.
Углекислый газ является конечным продуктом дыхания. При высокой концентрации газа дыхание растений снижается по следующим причинам: 1) ингибируются дыхательные ферменты, 2) закрываются устьица, что препятствует доступу кислорода к клеткам.
Содержание воды. Водный дефицит растущих тканей увеличивает интенсивность дыхания из-за активации распада сложных углеводов (например, крахмала) на более простые, которые являются субстратом дыхания. Однако при этом нарушается сопряжение окисления и фосфорилирования. Дыхание в этом случае представляет бесполезную трату вещества. Иная закономерность характерна для органов, находящихся в состоянии покоя. Повышение содержания воды в семенах приводит к резкому увеличению интенсивности дыхания.
Свет. Трудно выявить влияние света на дыхание зеленых растений, так как одновременно с дыханием осуществляется противоположный процесс – фотосинтез. Освещенность, при которой интенсивность фотосинтеза равна интенсивности дыхания по уровню поглощенного и выделенного углекислого газа, называют компенсационным пунктом. Дыхание незеленых тканей активируется светом коротковолновой части спектра, так как максимумы поглощения флавинов и цитохромов расположены в области 380-600 нм.
Минеральные вещества. Такие элементы как фосфор, сера, железо, медь, марганец необходимы для дыхания, являясь составной частью ферментов или как фосфор промежуточным продуктом. При повышении концентрации солей в питательном растворе, на котором выращивают проростки, их дыхание активируется (эффект «солевого дыхания»).
Механическое повреждение усиливает дыхание из-за быстрого окисления фенольных и других соединений, которые выходят из поврежденных вакуолей и становятся доступными для оксидаз.
Список использованной литературы
1. Алехина Н.Д., Балнокин Ю.В., Гавриленко В.Ф. и др. под ред. Ермакова И.П. Физиология растений. – М.: Академия, 2004
2. Грин Н., Стаут Т., Тейлор Д. Биология т.2. – М.: Мир, 1990
3. Малиновский В.И. Физиология растений. – Владивосток: Изд-во ДВГУ, 2004
4. Полевой В.В. Физиология растений. – М.: Высшая школа, 1983
5. Рубин Б.А., Ладыгина М.Е. Физиология и биохимия дыхания растений. – М.: Наука, 1974
6. Якушкина Н.И. Физиология растений. – М.: Просвещение, 1993
Перепечатка материалов без ссылки на наш сайт запрещена